Սպիտակուցի բանաձևը քիմիայում. Սպիտակուցներ. կառուցվածքը և գործառույթները: Սպիտակուցների հատկությունները. Սպիտակուցների քիմիական հատկությունները, որակական ռեակցիաները, ռեակցիայի հավասարումները
Սկյուռիկներ- բնական պոլիպեպտիդներ հսկայական մոլեկուլային քաշով: Նրանք բոլոր կենդանի օրգանիզմների մասն են կազմում և կատարում են տարբեր կենսաբանական գործառույթներ։
Սպիտակուցի կառուցվածքը.
Սպիտակուցներն ունեն կառուցվածքի 4 մակարդակ.
- սպիտակուցի առաջնային կառուցվածքը- ամինաթթուների գծային հաջորդականությունը պոլիպեպտիդային շղթայում՝ ծալված տարածության մեջ.
- սպիտակուցի երկրորդական կառուցվածքը- պոլիպեպտիդային շղթայի կոնֆորմացիա, քանի որ ոլորում տարածության մեջ ջրածնային կապերի պատճառով Ն.Հ.Եվ COխմբերով։ Տեղադրման 2 եղանակ կա. α -պարույր և β - կառուցվածքը.
- սպիտակուցի երրորդական կառուցվածքըպտտման եռաչափ պատկերն է α - պարույր կամ β - կառուցվածքները տարածության մեջ.

Այս կառուցվածքը ձևավորվում է -S-S- դիսուլֆիդային կամուրջներով ցիստեինի մնացորդների միջև: Հակառակ լիցքավորված իոնները մասնակցում են նման կառուցվածքի ձևավորմանը։
- սպիտակուցային չորրորդական կառուցվածքըձևավորվում է տարբեր պոլիպեպտիդային շղթաների փոխազդեցության պատճառով.

Սպիտակուցի սինթեզ.
Սինթեզը հիմնված է պինդ փուլային մեթոդի վրա, որի դեպքում առաջին ամինաթթուն ամրացվում է պոլիմերային կրիչի վրա, և դրան հաջորդաբար ավելացվում են նոր ամինաթթուներ։ Այնուհետև պոլիմերը առանձնացվում է պոլիպեպտիդային շղթայից:
Սպիտակուցի ֆիզիկական հատկությունները.
Սպիտակուցի ֆիզիկական հատկությունները որոշվում են նրա կառուցվածքով, ուստի սպիտակուցները բաժանվում են գնդաձեւ(լուծվում է ջրում) և fibrillar(ջրի մեջ չլուծվող):
Սպիտակուցների քիմիական հատկությունները.
1. Սպիտակուցների դենատուրացիա(երկրորդային և երրորդական կառուցվածքի ոչնչացում՝ առաջնայինը պահպանելով)։ Դենատուրացիայի օրինակ է ձվի սպիտակուցի կոագուլյացիան, երբ ձվերը եփում են:
2. Սպիտակուցի հիդրոլիզ- առաջնային կառուցվածքի անդառնալի ոչնչացում թթվային կամ ալկալային լուծույթամինաթթուների առաջացմամբ։ Ահա թե ինչպես կարող եք տեղադրել քանակական կազմըսպիտակուցներ.
3. Որակական ռեակցիաներ.
Բիուրետի ռեակցիա- փոխազդեցություն պեպտիդային կապև պղնձի (II) աղերը ալկալային լուծույթում: Ռեակցիայի վերջում լուծումը դառնում է մանուշակագույն։
Xantoprotein ռեակցիա- ազոտաթթվի հետ արձագանքելիս նկատվում է դեղին գույն:
Սպիտակուցի կենսաբանական նշանակությունը.
1. Սպիտակուցները շինանյութ են դրանից կառուցված մկանները, ոսկորները, հյուսվածքները։
2. Սպիտակուցներ՝ ընկալիչներ. Նրանք փոխանցում և ընկալում են շրջակա բջիջներից ստացվող ազդանշանները:
3. Սպիտակուցները կարեւոր դեր են խաղում օրգանիզմի իմունային համակարգում:
4. Սպիտակուցները կատարում են տրանսպորտային գործառույթներ և տեղափոխում են մոլեկուլներ կամ իոններ սինթեզի կամ կուտակման վայր: (Հեմոգլոբինը թթվածինը տեղափոխում է հյուսվածքներ):
5. Սպիտակուցներ - կատալիզատորներ - ֆերմենտներ. Սրանք շատ հզոր ընտրողական կատալիզատորներ են, որոնք միլիոնավոր անգամներ արագացնում են ռեակցիաները:
Կան մի շարք ամինաթթուներ, որոնք չեն կարող սինթեզվել մարմնում. անփոխարինելի, ստացվում են միայն սննդից՝ տիզին, ֆենիլալանին, մետինին, վալին, լեյցին, տրիպտոֆան, իզոլեյցին, թրեոնին։
ՍՊԻՏԱԿՈՒՆՆԵՐ (սպիտակուցներ), ազոտ պարունակող բարդ միացությունների դաս, կենդանի նյութի ամենաբնորոշ և կարևոր (նուկլեինաթթուների հետ մեկտեղ) բաղադրիչները։ Սպիտակուցները կատարում են բազմաթիվ և բազմազան գործառույթներ։ Սպիտակուցների մեծ մասը կատալիզացնող ֆերմենտներ են քիմիական ռեակցիաներ. Ֆիզիոլոգիական պրոցեսները կարգավորող շատ հորմոններ նույնպես սպիտակուցներ են։ Կառուցվածքային սպիտակուցները, ինչպիսիք են կոլագենը և կերատինը, ոսկրային հյուսվածքի, մազերի և եղունգների հիմնական բաղադրիչներն են: Մկանների կծկվող սպիտակուցները կարող են փոխել իրենց երկարությունը՝ օգտագործելով քիմիական էներգիակատարել մեխանիկական աշխատանք. Սպիտակուցները ներառում են հակամարմիններ, որոնք կապում և չեզոքացնում են թունավոր նյութերը: Որոշ սպիտակուցներ, որոնք կարող են արձագանքել արտաքին ազդեցություններին (լույս, հոտ), ծառայում են որպես ընկալիչներ զգայական օրգաններում, որոնք ընկալում են գրգռվածությունը: Շատ սպիտակուցներ, որոնք տեղակայված են բջջի ներսում և դրանց վրա բջջային թաղանթ, կատարել կարգավորող գործառույթներ.19-րդ դարի առաջին կեսին։ Շատ քիմիկոսներ, և նրանց թվում հիմնականում Ջ. ֆոն Լիբիգը, աստիճանաբար եկան այն եզրակացության, որ սպիտակուցները ներկայացնում են ազոտային միացությունների հատուկ դաս: «Սպիտակուցներ» անվանումը (հունարենից.
պրոտոներ առաջին) առաջարկվել է 1840 թվականին հոլանդացի քիմիկոս Գ.Մուլդերի կողմից։ ՖԻԶԻԿԱԿԱՆ ՀԱՏԿՈՒԹՅՈՒՆՆԵՐ Սպիտակուցներ պինդ վիճակում սպիտակ, և լուծույթում անգույն են, բացառությամբ այն դեպքերի, երբ դրանք կրում են որոշ քրոմոֆոր (գունավոր) խումբ, ինչպիսին է հեմոգլոբինը: Տարբեր սպիտակուցների մեջ ջրի լուծելիությունը մեծապես տարբերվում է: Այն նաև փոխվում է` կախված pH-ից և լուծույթում աղերի կոնցենտրացիայից, ուստի հնարավոր է ընտրել այնպիսի պայմաններ, որոնց դեպքում մեկ սպիտակուցը ընտրողաբար կտեղավորվի այլ սպիտակուցների առկայության դեպքում: Այս «աղը հանելու» մեթոդը լայնորեն կիրառվում է սպիտակուցների մեկուսացման և մաքրման համար: Մաքրված սպիտակուցը հաճախ նստում է լուծույթից բյուրեղների տեսքով:Այլ միացությունների համեմատ՝ սպիտակուցների մոլեկուլային զանգվածը շատ մեծ է՝ տատանվում է մի քանի հազարից մինչև միլիոնավոր դալտոններ։ Հետևաբար, ուլտրակենտրոնացման ժամանակ սպիտակուցները նստում են, այն էլ՝ տարբեր արագությամբ։ Սպիտակուցի մոլեկուլներում դրական և բացասական լիցքավորված խմբերի առկայության պատճառով դրանք շարժվում են տարբեր արագություններով և էլեկտրական դաշտում։ Սա էլեկտրաֆորեզի հիմքն է՝ մեթոդ, որն օգտագործվում է առանձին սպիտակուցները բարդ խառնուրդներից մեկուսացնելու համար։ Սպիտակուցները նույնպես մաքրվում են քրոմատագրման միջոցով։
ՔԻՄԻԱԿԱՆ ՀԱՏԿՈՒԹՅՈՒՆՆԵՐ Կառուցվածք. Սպիտակուցները պոլիմերներ են, այսինքն. մոլեկուլներ, որոնք շղթաների պես կառուցված են կրկնվող մոնոմերային միավորներից կամ ենթամիավորներից, որոնց դերը նրանք խաղում են ա -ամինաթթուներ. Ամինաթթուների ընդհանուր բանաձևըորտեղ Ռ ջրածնի ատոմ կամ որոշ օրգանական խումբ։Սպիտակուցի մոլեկուլը (պոլիպեպտիդային շղթա) կարող է բաղկացած լինել միայն համեմատաբար փոքր թվով ամինաթթուներից կամ մի քանի հազար մոնոմերային միավորներից։ Ամինաթթուների համակցությունը շղթայում հնարավոր է, քանի որ դրանցից յուրաքանչյուրն ունի երկու տարբեր քիմիական խմբեր՝ հիմնական հատկություններով ամինախումբ,
NH 2 և թթվային կարբոքսիլ խումբ՝ COOH։ Այս երկու խմբերն էլ կապված են ա - ածխածնի ատոմ. Մեկ ամինաթթվի կարբոքսիլ խումբը կարող է ձևավորել ամիդային (պեպտիդ) կապ մեկ այլ ամինաթթվի ամինո խմբի հետ. Երկու ամինաթթուների այս ձևով կապվելուց հետո շղթան կարող է երկարացվել՝ երկրորդ ամինաթթուն ավելացնելով երրորդը և այլն: Ինչպես երևում է վերը նշված հավասարումից, երբ ձևավորվում է պեպտիդային կապ, ազատվում է ջրի մոլեկուլ։ Թթուների, ալկալիների կամ պրոտեոլիտիկ ֆերմենտների առկայության դեպքում ռեակցիան ընթանում է հակառակ ուղղությամբ՝ պոլիպեպտիդային շղթան ջրի ավելացումով բաժանվում է ամինաթթուների։ Այս ռեակցիան կոչվում է հիդրոլիզ։ Հիդրոլիզը տեղի է ունենում ինքնաբերաբար, և էներգիա է պահանջվում ամինաթթուները պոլիպեպտիդային շղթայի մեջ միացնելու համար:
Երկու ամինաթթուների այս ձևով կապվելուց հետո շղթան կարող է երկարացվել՝ երկրորդ ամինաթթուն ավելացնելով երրորդը և այլն: Ինչպես երևում է վերը նշված հավասարումից, երբ ձևավորվում է պեպտիդային կապ, ազատվում է ջրի մոլեկուլ։ Թթուների, ալկալիների կամ պրոտեոլիտիկ ֆերմենտների առկայության դեպքում ռեակցիան ընթանում է հակառակ ուղղությամբ՝ պոլիպեպտիդային շղթան ջրի ավելացումով բաժանվում է ամինաթթուների։ Այս ռեակցիան կոչվում է հիդրոլիզ։ Հիդրոլիզը տեղի է ունենում ինքնաբերաբար, և էներգիա է պահանջվում ամինաթթուները պոլիպեպտիդային շղթայի մեջ միացնելու համար: Կարբոքսիլ խումբը և ամիդային խումբը (կամ նմանատիպ իմիդ խումբը ամինաթթվի պրոլինի դեպքում) առկա են բոլոր ամինաթթուներում, սակայն ամինաթթուների միջև տարբերությունները որոշվում են խմբի բնույթով կամ «կողային շղթայով»: որը նշված է վերևում տառով
Ռ . Կողային շղթայի դերը կարող է խաղալ ջրածնի մեկ ատոմը, ինչպես ամինաթթուների գլիցինը, կամ ինչ-որ ծավալուն խումբ, ինչպես հիստիդինը և տրիպտոֆանը: Որոշ կողմնակի շղթաներ քիմիապես իներտ են, իսկ մյուսները նկատելի են ռեակտիվություն.Շատ հազարավոր տարբեր ամինաթթուներ կարող են սինթեզվել, և շատ տարբեր ամինաթթուներ են հանդիպում բնության մեջ, սակայն սպիտակուցի սինթեզի համար օգտագործվում են միայն 20 տեսակի ամինաթթուներ՝ ալանին, արգինին, ասպարագին, ասպարթաթթու, վալին, հիստիդին, գլիցին, գլուտամին, գլուտամին: թթու, իզոլեյցին, լեյցին, լիզին, մեթիոնին, պրոլին, սերին, թիրոզին, թրեոնին, տրիպտոֆան, ֆենիլալանին և ցիստեին (սպիտակուցներում ցիստեինը կարող է առկա լինել որպես դիմեր
ցիստին): Ճիշտ է, որոշ սպիտակուցներ պարունակում են նաև այլ ամինաթթուներ, բացի կանոնավոր հանդիպող քսանից, բայց դրանք ձևավորվում են թվարկված քսանից մեկի փոփոխության արդյունքում այն սպիտակուցի մեջ ներառվելուց հետո:Օպտիկական ակտիվություն. Բոլոր ամինաթթուները, բացառությամբ գլիցինի, ունեն ա Ածխածնի ատոմը կցված է չորս տարբեր խմբերի: Երկրաչափության տեսանկյունից չորս տարբեր խմբեր կարող են կցվել երկու եղանակով, և, համապատասխանաբար, կան երկու հնարավոր կոնֆիգուրացիաներ կամ երկու իզոմերներ, որոնք կապված են միմյանց հետ, քանի որ առարկան իր հայելային պատկերին է, այսինքն. Ինչպես ձախ ձեռքըդեպի աջ։ Մեկ կոնֆիգուրացիան կոչվում է ձախ կամ ձախլիկ (Լ ), իսկ մյուսը աջ, կամ դեքստրոտորատոր (Դ ), քանի որ երկու նման իզոմերներ տարբերվում են բևեռացված լույսի հարթության պտտման ուղղությամբ։ Հանդիպում է միայն սպիտակուցներումԼ -ամինաթթուներ (բացառություն է գլիցինը, այն կարող է ներկայացվել միայն մեկ ձևով, քանի որ նրա չորս խմբերից երկուսը նույնն են), և բոլորն ունեն. օպտիկական ակտիվություն(քանի որ կա միայն մեկ իզոմեր):Դ -ամինաթթուները բնության մեջ հազվադեպ են. դրանք հայտնաբերված են որոշ հակաբիոտիկների և բակտերիաների բջջային պատի մեջ:Ամինաթթուների հաջորդականությունը. Պոլիպեպտիդային շղթայում ամինաթթուները դասավորված են ոչ թե պատահական, այլ որոշակի ֆիքսված հերթականությամբ, և հենց այս կարգն է որոշում սպիտակուցի գործառույթներն ու հատկությունները։ Փոփոխելով ամինաթթուների 20 տեսակների հերթականությունը՝ դուք կարող եք ստեղծել հսկայական քանակությամբ տարբեր սպիտակուցներ, ինչպես այբուբենի տառերից կարող եք ստեղծել բազմաթիվ տարբեր տեքստեր:Նախկինում սպիտակուցի ամինաթթուների հաջորդականությունը որոշելը հաճախ տևում էր մի քանի տարի: Ուղղակի սահմանումիսկ այժմ դա բավականին աշխատատար խնդիր է, չնայած ստեղծվել են սարքեր, որոնք թույլ են տալիս այն իրականացնել ավտոմատ կերպով։ Սովորաբար ավելի հեշտ է որոշել համապատասխան գենի նուկլեոտիդային հաջորդականությունը և դրանից դուրս բերել սպիտակուցի ամինաթթուների հաջորդականությունը։ Մինչ օրս արդեն որոշված են հարյուրավոր սպիտակուցների ամինաթթուների հաջորդականությունը։ Վերծանված սպիտակուցների գործառույթները սովորաբար հայտնի են, և դա օգնում է պատկերացնել նմանատիպ սպիտակուցների հնարավոր գործառույթները, որոնք ձևավորվում են, օրինակ, չարորակ նորագոյացություններում:
Բարդ սպիտակուցներ. Միայն ամինաթթուներից բաղկացած սպիտակուցները կոչվում են պարզ: Հաճախ, սակայն, մետաղի ատոմ կամ որևէ այլ քիմիական միացություն, որը ամինաթթու չէ։ Նման սպիտակուցները կոչվում են բարդ: Օրինակ՝ հեմոգլոբինը. այն պարունակում է երկաթի պորֆիրին, որը որոշում է նրա կարմիր գույնը և թույլ է տալիս նրան հանդես գալ որպես թթվածնի կրիչ։Բարդ սպիտակուցների անունները ցույց են տալիս կցված խմբերի բնույթը՝ գլիկոպրոտեինները պարունակում են շաքարներ, լիպոպրոտեինները՝ ճարպեր։ Եթե ֆերմենտի կատալիտիկ ակտիվությունը կախված է կցված խմբից, ապա այն կոչվում է պրոթեզային խումբ։ Հաճախ վիտամինը պրոթեզային խմբի դեր է կատարում կամ դրա մի մասն է: Վիտամին A-ն, օրինակ, կցված է ցանցաթաղանթի սպիտակուցներից մեկին, որոշում է նրա զգայունությունը լույսի նկատմամբ։
Երրորդական կառուցվածք. Կարևորը ոչ այնքան բուն սպիտակուցի ամինաթթուների հաջորդականությունն է (առաջնային կառուցվածքը), այլ այն, թե ինչպես է այն դրված տիեզերքում: Պոլիպեպտիդային շղթայի ողջ երկարությամբ ջրածնի իոնները ձևավորվում են կանոնավոր ջրածնային կապեր, որոնք նրան տալիս են պարույրի կամ շերտի (երկրորդական կառուցվածք) տեսք։ Նման խխունջների և շերտերի համակցությունից առաջանում է հաջորդ կարգի կոմպակտ ձև՝ սպիտակուցի երրորդական կառուցվածքը։ Շղթայի մոնոմերային միավորները պահող կապերի շուրջ հնարավոր են փոքր անկյուններով պտույտներ։ Հետևաբար, մաքուրի հետ երկրաչափական կետՀաշվի առնելով, որ ցանկացած պոլիպեպտիդ շղթայի համար հնարավոր կոնֆիգուրացիաների թիվը անսահման մեծ է: Իրականում յուրաքանչյուր սպիտակուց սովորաբար գոյություն ունի միայն մեկ կոնֆիգուրացիայի մեջ, որը որոշվում է իր ամինաթթուների հաջորդականությամբ: Այս կառույցը կոշտ չէ, կարծես « շնչում է» տատանվում է որոշակի միջին կոնֆիգուրացիայի շուրջ: Շղթան ծալվում է այնպիսի կոնֆիգուրացիայի մեջ, որում ազատ էներգիան (աշխատանք արտադրելու ունակությունը) նվազագույն է, ճիշտ այնպես, ինչպես արձակված զսպանակը սեղմվում է միայն նվազագույն ազատ էներգիային համապատասխան վիճակի: Հաճախ շղթայի մի մասը կոշտորեն կապված է մյուսի հետ դիսուլֆիդով (ՍՍ) կապեր երկու ցիստեինի մնացորդների միջև: Մասամբ սա է պատճառը, որ ցիստեինը հատկապես կարևոր դեր է խաղում ամինաթթուների մեջ:Սպիտակուցների կառուցվածքի բարդությունն այնքան մեծ է, որ դեռևս հնարավոր չէ հաշվարկել սպիտակուցի երրորդական կառուցվածքը, նույնիսկ եթե հայտնի է նրա ամինաթթուների հաջորդականությունը։ Բայց եթե հնարավոր է ստանալ սպիտակուցային բյուրեղներ, ապա դրա երրորդական կառուցվածքը կարելի է որոշել ռենտգենյան դիֆրակցիայով։
Կառուցվածքային, կծկվող և որոշ այլ սպիտակուցներում շղթաները երկարաձգվում են, և մոտակայքում ընկած մի քանի թեթև ծալված շղթաներ ձևավորում են մանրաթելեր. մանրաթելերն իրենց հերթին ծալվում են մանրաթելերի ավելի մեծ գոյացությունների: Այնուամենայնիվ, լուծույթում գտնվող սպիտակուցների մեծ մասը ունեն գնդաձև ձև. շղթաները ոլորված են գնդիկի մեջ, ինչպես մանվածքը գնդակի մեջ: Այս կոնֆիգուրացիայով ազատ էներգիան նվազագույն է, քանի որ հիդրոֆոբ («ջուր վանող») ամինաթթուները թաքնված են գլոբուլի ներսում, իսկ հիդրոֆիլ («ջուր ձգող») ամինաթթուները՝ դրա մակերեսին։
Շատ սպիտակուցներ մի քանի պոլիպեպտիդ շղթաների համալիրներ են: Այս կառուցվածքը կոչվում է սպիտակուցի չորրորդական կառուցվածք։ Հեմոգլոբինի մոլեկուլը, օրինակ, բաղկացած է չորս ենթամիավորներից, որոնցից յուրաքանչյուրը գնդաձեւ սպիտակուց է։
Կառուցվածքային սպիտակուցները, իրենց գծային կոնֆիգուրացիայի շնորհիվ, ձևավորում են մանրաթելեր, որոնք ունեն շատ բարձր առաձգական ուժ, մինչդեռ գնդաձև կոնֆիգուրացիան թույլ է տալիս սպիտակուցներին հատուկ փոխազդեցության մեջ մտնել այլ միացությունների հետ: Գնդիկի մակերեսին, երբ շղթաները ճիշտ դրված են, հայտնվում են որոշակի ձևի խոռոչներ, որոնցում տեղակայված են ռեակտիվ քիմիական խմբեր: Եթե տվյալ սպիտակուցը ֆերմենտ է, ապա ինչ-որ նյութի մեկ այլ, սովորաբար ավելի փոքր, մոլեկուլ մտնում է այդպիսի խոռոչ, ինչպես որ բանալին մտնում է կողպեք; սա փոխում է կոնֆիգուրացիան էլեկտրոնային ամպմոլեկուլների վրա ազդում են խոռոչի քիմիական խմբերը, և դա ստիպում է նրան արձագանքել որոշակի ձևով: Այս կերպ ֆերմենտը կատալիզացնում է ռեակցիան։ Հակամարմինների մոլեկուլներն ունեն նաև խոռոչներ, որոնցում կապվում են տարբեր օտար նյութեր և դրանով իսկ անվնաս են դառնում։ «Կողպեք և բանալին» մոդելը, որը բացատրում է սպիտակուցների փոխազդեցությունը այլ միացությունների հետ, թույլ է տալիս հասկանալ ֆերմենտների և հակամարմինների առանձնահատկությունները, այսինքն. միայն որոշակի միացությունների հետ արձագանքելու նրանց ունակությունը:
Սպիտակուցներ տարբեր տեսակի օրգանիզմներում. Սպիտակուցներ, որոնք կատարում են նույն գործառույթը տարբեր տեսակներբույսերը և կենդանիները և, հետևաբար, կրում են նույն անունը, նույնպես ունեն նմանատիպ կոնֆիգուրացիա: Նրանք, սակայն, որոշ չափով տարբերվում են իրենց ամինաթթուների հաջորդականությամբ: Քանի որ տեսակները տարբերվում են ընդհանուր նախնուց, որոշ ամինաթթուներ որոշակի դիրքերում փոխարինվում են մյուսների կողմից մուտացիաներով: Ժառանգական հիվանդություններ առաջացնող վնասակար մուտացիաները մերժվում են բնական ընտրություն, բայց օգտակար կամ գոնե չեզոքները կարող են մնալ։ Որքան ավելի մոտ են միմյանց երկուսը կենսաբանական տեսակներ, այնքան քիչ տարբերություններ են հայտնաբերվում դրանց սպիտակուցներում։Որոշ սպիտակուցներ փոխվում են համեմատաբար արագ, մյուսները շատ պահպանված են: Վերջինս ներառում է, օրինակ, ցիտոքրոմը Հետշնչառական ֆերմենտ, որը հայտնաբերված է կենդանի օրգանիզմների մեծ մասում: Մարդկանց և շիմպանզեների մոտ նրա ամինաթթուների հաջորդականությունները նույնական են, իսկ ցիտոքրոմում ՀետՑորենի մեջ ամինաթթուների միայն 38%-ն էր տարբեր: Նույնիսկ մարդկանց ու բակտերիաների համեմատությունը՝ ցիտոքրոմների նմանությունը Հետ(տարբերությունները ազդում են այստեղ ամինաթթուների 65%-ի վրա) դեռ կարելի է տեսնել, թեև բակտերիաների և մարդկանց ընդհանուր նախնին ապրել է Երկրի վրա մոտ երկու միլիարդ տարի առաջ: Մեր օրերում ամինաթթուների հաջորդականությունների համեմատությունը հաճախ օգտագործվում է ֆիլոգենետիկ (ընտանեկան) ծառ կառուցելու համար՝ արտացոլելով տարբեր օրգանիզմների միջև էվոլյուցիոն հարաբերությունները։
Դենատուրացիա. Սինթեզված սպիտակուցի մոլեկուլը՝ ծալովի, ձեռք է բերում իր բնորոշ կոնֆիգուրացիան։ Այնուամենայնիվ, այս կոնֆիգուրացիան կարող է ոչնչացվել տաքացման, pH-ի փոփոխման, օրգանական լուծիչների ազդեցության միջոցով և նույնիսկ լուծույթը պարզապես թափահարելով, մինչև դրա մակերեսին փուչիկները հայտնվեն: Այս ձևով ձևափոխված սպիտակուցը կոչվում է դենատուրացված; այն կորցնում է իր կենսաբանական ակտիվությունը և սովորաբար դառնում է անլուծելի։ Դենատուրացված սպիտակուցի հայտնի օրինակներ են խաշած ձվերը կամ հարած սերուցքը: Փոքր սպիտակուցները, որոնք պարունակում են ընդամենը մոտ հարյուր ամինաթթուներ, ունակ են վերածնվել, այսինքն. նորից ձեռք բերել սկզբնական կազմաձևը: Բայց սպիտակուցների մեծ մասը պարզապես վերածվում է խճճված պոլիպեպտիդային շղթաների զանգվածի և չի վերականգնում իրենց նախկին կոնֆիգուրացիան։Ակտիվ սպիտակուցների մեկուսացման հիմնական դժվարություններից մեկը նրանց ծայրահեղ զգայունությունն է դենատուրացիայի նկատմամբ: Սպիտակուցների այս հատկությունը օգտակար կիրառություն է գտնում պահածոյացման մեջ։ սննդամթերք: բարձր ջերմաստիճանանդառնալիորեն այլասերում է միկրոօրգանիզմների ֆերմենտները, և միկրոօրգանիզմները մահանում են:
ՍՊՏՈՒՏԻՆՆԵՐԻ ՍԻՆԹԵԶ Սպիտակուցը սինթեզելու համար կենդանի օրգանիզմը պետք է ունենա ֆերմենտների համակարգ, որը կարող է միացնել մի ամինաթթուն մյուսին։ Անհրաժեշտ է նաև տեղեկատվության աղբյուր՝ որոշելու համար, թե որ ամինաթթուները պետք է համակցվեն: Քանի որ մարմնում կան հազարավոր տեսակի սպիտակուցներ, և դրանցից յուրաքանչյուրը բաղկացած է միջինում մի քանի հարյուր ամինաթթուներից, անհրաժեշտ տեղեկատվությունպետք է իսկապես հսկայական լինի: Այն պահվում է մոլեկուլներում (նման է, թե ինչպես է պահվում ձայնագրությունը մագնիսական ժապավենի վրա) նուկլեինաթթուներ, որոնցից ստեղծվում են գեներ։ սմ . նաև Ժառանգական; ՆՈՒԿԼԵԻԿ ԹԹՈՒՆԵՐ.Ֆերմենտների ակտիվացում. Ամինաթթուներից սինթեզված պոլիպեպտիդային շղթան միշտ չէ, որ սպիտակուց է իր վերջնական ձևով: Շատ ֆերմենտներ սկզբում սինթեզվում են որպես ոչ ակտիվ պրեկուրսորներ և ակտիվանում են միայն այն բանից հետո, երբ մեկ այլ ֆերմենտ հեռացնում է մի քանի ամինաթթուներ շղթայի մի ծայրից: Նման կերպ ակտիվ ձևորոշ մարսողական ֆերմենտներ, ինչպիսիք են տրիպսինը, սինթեզվում են. այս ֆերմենտները ակտիվանում են մարսողական տրակտում շղթայի տերմինալ հատվածի հեռացման արդյունքում։ Ինսուլին հորմոնը, որի մոլեկուլն իր ակտիվ ձևով բաղկացած է երկու կարճ շղթայից, սինթեզվում է մեկ շղթայի տեսքով, այսպես կոչված. պրոինսուլին. Հետո միջին մասըայս շղթան հեռացվում է, իսկ մնացած բեկորները կապվում են միմյանց հետ՝ ձևավորելով ակտիվ հորմոնի մոլեկուլ։ Կոմպլեքս սպիտակուցները ձևավորվում են միայն այն բանից հետո, երբ որոշակի քիմիական խումբ կցվում է սպիտակուցին, և այդ կցումը հաճախ պահանջում է նաև ֆերմենտ:Նյութափոխանակության շրջանառություն. Կենդանիներին պիտակավորված ամինաթթուներով կերակրելուց հետո ռադիոակտիվ իզոտոպներածխածինը, ազոտը կամ ջրածինը, պիտակը արագորեն մտնում է իր սպիտակուցների մեջ: Եթե պիտակավորված ամինաթթուները դադարում են մտնել օրգանիզմ, ապա սպիտակուցներում պիտակի քանակը սկսում է նվազել: Այս փորձերը ցույց են տալիս, որ ստացված սպիտակուցները օրգանիզմում չեն պահվում մինչև կյանքի վերջ։ Նրանք բոլորը, չնչին բացառություններով, գտնվում են դինամիկ վիճակում, անընդհատ տրոհվում են ամինաթթուների, իսկ հետո նորից սինթեզվում։Որոշ սպիտակուցներ քայքայվում են, երբ բջիջները մահանում են և ոչնչացվում: Դա տեղի է ունենում անընդհատ, օրինակ, կարմիր արյան բջիջների և էպիթելային բջիջների դեպքում, որոնք ծածկում են աղիքի ներքին մակերեսը: Բացի այդ, սպիտակուցների քայքայումն ու վերասինթեզը տեղի է ունենում նաև կենդանի բջիջներում։ Տարօրինակ կերպով, սպիտակուցների քայքայման մասին ավելի քիչ է հայտնի, քան դրանց սինթեզի մասին: Ակնհայտ է, սակայն, որ տրոհումը ներառում է պրոտեոլիտիկ ֆերմենտներ, որոնք նման են նրանց, որոնք սպիտակուցները տրոհում են մարսողական տրակտում ամինաթթուների:
Տարբեր սպիտակուցների կես կյանքը տատանվում է մի քանի ժամից մինչև մի քանի ամիս: Միակ բացառությունը կոլագենի մոլեկուլն է։ Ձևավորվելուց հետո դրանք մնում են կայուն և չեն թարմացվում կամ փոխարինվում: Այնուամենայնիվ, ժամանակի ընթացքում դրանց որոշ հատկություններ փոխվում են, մասնավորապես առաձգականությունը, և քանի որ դրանք չեն թարմացվում, դա հանգեցնում է որոշակի տարիքային փոփոխությունների, ինչպիսիք են մաշկի վրա կնճիռների տեսքը:
Սինթետիկ սպիտակուցներ. Քիմիկոսները վաղուց սովորել են պոլիմերացնել ամինաթթուները, սակայն ամինաթթուները միաձուլվում են անկանոն կերպով, այնպես որ նման պոլիմերացման արտադրանքը քիչ նմանություն ունի բնականին։ Ճիշտ է, հնարավոր է միավորել ամինաթթուները տվյալ հերթականությամբ, ինչը հնարավորություն է տալիս ստանալ որոշ կենսաբանական ակտիվ սպիտակուցներ, մասնավորապես՝ ինսուլին։ Գործընթացը բավականին բարդ է, և այս կերպ հնարավոր է ստանալ միայն այն սպիտակուցները, որոնց մոլեկուլները պարունակում են մոտ հարյուր ամինաթթուներ։ Փոխարենը նախընտրելի է սինթեզել կամ մեկուսացնել գենի նուկլեոտիդային հաջորդականությունը, որը համապատասխանում է ցանկալի ամինաթթուների հաջորդականությանը, այնուհետև այդ գենը ներմուծել մանրէի մեջ, որը կարտադրվի բազմապատկման միջոցով: մեծ թվովցանկալի արտադրանքը. Այս մեթոդը, սակայն, ունի նաև իր թերությունները. սմ . նաև ԳԵՆԱՏԵԽՆԻԿԱ. ՍՊԵՏՈՒՆԻԿ ԵՎ ՍՆՆԴԻՐ Երբ մարմնում սպիտակուցները տրոհվում են ամինաթթուների, այդ ամինաթթուները կարող են կրկին օգտագործվել սպիտակուցներ սինթեզելու համար: Միևնույն ժամանակ, ամինաթթուներն իրենք ենթակա են քայքայման, ուստի դրանք ամբողջությամբ չեն վերաօգտագործվում: Պարզ է նաև, որ աճի, հղիության և վերքերի բուժման ընթացքում սպիտակուցի սինթեզը պետք է գերազանցի քայքայմանը: Մարմինը անընդհատ կորցնում է որոշ սպիտակուցներ. Սրանք մազերի, եղունգների և մաշկի մակերեսային շերտի սպիտակուցներն են։ Ուստի սպիտակուցներ սինթեզելու համար յուրաքանչյուր օրգանիզմ պետք է ամինաթթուներ ստանա սննդից։ Կանաչ բույսերը սինթեզվում են CO-ից 2 , ջուրը և ամոնիակը կամ նիտրատները բոլոր 20 ամինաթթուներն են, որոնք առկա են սպիտակուցներում: Շատ բակտերիաներ կարող են նաև սինթեզել ամինաթթուներ շաքարի (կամ որոշ համարժեքի) և ֆիքսված ազոտի առկայության դեպքում, սակայն շաքարը, ի վերջո, մատակարարվում է կանաչ բույսերի կողմից: Կենդանիներն ունեն ամինաթթուներ սինթեզելու սահմանափակ կարողություն. նրանք ամինաթթուներ են ստանում՝ ուտելով կանաչ բույսեր կամ այլ կենդանիներ։ Մարսողական համակարգում ներծծվող սպիտակուցները տրոհվում են ամինաթթուների, վերջիններս ներծծվում են, և դրանցից կառուցվում են տվյալ օրգանիզմին բնորոշ սպիտակուցներ։ Կլանված սպիտակուցներից ոչ մեկը, որպես այդպիսին, չի մտնում մարմնի կառուցվածքների մեջ: Միակ բացառությունն այն է, որ շատ կաթնասունների մոտ որոշ մայրական հակամարմիններ կարող են անձեռնմխելիորեն պլասենցայի միջով անցնել պտղի արյան հոսք, իսկ մոր կաթի միջոցով (հատկապես որոճողների մոտ) կարող են փոխանցվել նորածինին ծնվելուց անմիջապես հետո:Սպիտակուցի պահանջ. Հասկանալի է, որ կյանքը պահպանելու համար օրգանիզմը պետք է որոշակի քանակությամբ սպիտակուց ստանա սննդից։ Այնուամենայնիվ, այս անհրաժեշտության չափը կախված է մի շարք գործոններից: Մարմինը սննդի կարիք ունի և՛ որպես էներգիայի աղբյուր (կալորիականություն), և՛ որպես նյութ՝ իր կառուցվածքները կառուցելու համար։ Էներգիայի կարիքն առաջին տեղում է: Սա նշանակում է, որ երբ սննդակարգում քիչ ածխաջրեր և ճարպեր կան, դիետիկ սպիտակուցներն օգտագործվում են ոչ թե սեփական սպիտակուցների սինթեզի համար, այլ որպես կալորիաների աղբյուր։ Երկարատև ծոմապահության ժամանակ նույնիսկ ձեր սեփական սպիտակուցներն են օգտագործվում էներգիայի կարիքները բավարարելու համար։ Եթե սննդակարգում բավարար քանակությամբ ածխաջրեր կան, ապա սպիտակուցի սպառումը կարող է կրճատվել:Ազոտի հավասարակշռությունը. Միջին հաշվով մոտ. Սպիտակուցի ընդհանուր զանգվածի 16%-ը ազոտ է։ Երբ սպիտակուցներում պարունակվող ամինաթթուները քայքայվում են, նրանց մեջ պարունակվող ազոտը օրգանիզմից դուրս է գալիս մեզով և (ավելի քիչ չափով) կղանքով՝ տարբեր ազոտային միացությունների տեսքով։ Ուստի հարմար է օգտագործել այնպիսի ցուցանիշ, ինչպիսին է ազոտի հավասարակշռությունը՝ սպիտակուցային սնուցման որակը գնահատելու համար, այսինքն. տարբերությունը (գրամներով) օրգանիզմ մտնող ազոտի քանակի և օրական արտազատվող ազոտի քանակի միջև։ Մեծահասակների նորմալ սնուցման դեպքում այդ քանակները հավասար են: Աճող օրգանիզմում արտազատվող ազոտի քանակը պակաս է ստացվածից, այսինքն. հաշվեկշիռը դրական է. Եթե սննդակարգում սպիտակուցի պակաս կա, հավասարակշռությունը բացասական է։ Եթե սննդակարգում կա բավարար կալորիա, բայց դրա մեջ չկան սպիտակուցներ, օրգանիզմը խնայում է սպիտակուցները։ Սպիտակուցային նյութափոխանակությունՄիևնույն ժամանակ, այն դանդաղում է, և սպիտակուցի սինթեզում ամինաթթուների վերամշակումը տեղի է ունենում հնարավորինս առավելագույն արդյունավետությամբ: Այնուամենայնիվ, կորուստներն անխուսափելի են, և ազոտային միացությունները դեռևս արտազատվում են մեզով և մասամբ՝ կղանքով։ Սպիտակուցների ծոմապահության ժամանակ օրգանիզմից օրական արտազատվող ազոտի քանակը կարող է ծառայել որպես օրական սպիտակուցի պակասի չափիչ։ Բնական է ենթադրել, որ սննդակարգ մտցնելով այս պակասին համարժեք սպիտակուցի քանակություն, կարելի է վերականգնել ազոտի հավասարակշռությունը։ Սակայն դա ճիշտ չէ։ Այս քանակությամբ սպիտակուց ստանալուց հետո մարմինը սկսում է ավելի քիչ արդյունավետ օգտագործել ամինաթթուները, ուստի որոշ լրացուցիչ սպիտակուցներ են պահանջվում ազոտի հավասարակշռությունը վերականգնելու համար:Եթե սննդակարգում սպիտակուցի քանակությունը գերազանցում է այն, ինչ անհրաժեշտ է ազոտի հավասարակշռությունը պահպանելու համար, ապա թվում է, որ վնաս չկա: Ավելորդ ամինաթթուները պարզապես օգտագործվում են որպես էներգիայի աղբյուր: Որպես հատկապես վառ օրինակ, էսկիմոսները օգտագործում են քիչ ածխաջրեր և մոտ տասն անգամ ավելի շատ սպիտակուցներ, որոնք անհրաժեշտ են ազոտի հավասարակշռությունը պահպանելու համար: Այնուամենայնիվ, շատ դեպքերում սպիտակուցը որպես էներգիայի աղբյուր օգտագործելը ձեռնտու չէ, քանի որ ածխաջրերի որոշակի քանակությունը կարող է շատ ավելի շատ կալորիա արտադրել, քան նույն քանակությամբ սպիտակուցը: Աղքատ երկրներում մարդիկ իրենց կալորիաները ստանում են ածխաջրերից և սպառում նվազագույն քանակսկյուռիկ.
Եթե օրգանիզմը ստանում է անհրաժեշտ քանակությամբ կալորիաներ ոչ սպիտակուցային մթերքների տեսքով, ապա ազոտի հավասարակշռության պահպանումն ապահովելու համար սպիտակուցի նվազագույն քանակությունը կազմում է մոտ. 30 գ օրական. Այսքան սպիտակուց է պարունակվում չորս կտոր հացում կամ 0,5 լիտր կաթում։ Մի փոքր ավելի մեծ թիվը սովորաբար համարվում է օպտիմալ; Խորհուրդ է տրվում 50-ից 70 գ:
Հիմնական ամինաթթուներ. Մինչ այժմ սպիտակուցը համարվում էր որպես ամբողջություն։ Մինչդեռ, որպեսզի սպիտակուցի սինթեզ տեղի ունենա, բոլորը էական ամինաթթուներ. Կենդանու մարմինն ինքնին ունակ է սինթեզել որոշ ամինաթթուներ: Դրանք կոչվում են փոխարինելի, քանի որ պարտադիր չէ, որ դրանք առկա լինեն սննդակարգում, միայն կարևոր է, որ սպիտակուցի ընդհանուր մատակարարումը որպես ազոտի աղբյուր բավարար լինի. ապա, եթե կա ոչ էական ամինաթթուների պակաս, ապա մարմինը կարող է սինթեզել դրանք ավելցուկային առկաների հաշվին։ Մնացած, «էական» ամինաթթուները չեն կարող սինթեզվել և պետք է մարմնին մատակարարվեն սննդի միջոցով: Մարդկանց համար անհրաժեշտ են վալինը, լեյցինը, իզոլեյցինը, թրեոնինը, մեթիոնինը, ֆենիլալանինը, տրիպտոֆանը, հիստիդինը, լիզինը և արգինինը: (Չնայած արգինինը կարող է սինթեզվել մարմնում, այն դասակարգվում է որպես էական ամինաթթու, քանի որ այն բավարար քանակությամբ չի արտադրվում նորածինների և աճող երեխաների մոտ: Մյուս կողմից, սննդի այս ամինաթթուների մի մասը կարող է անհարկի դառնալ մեծահասակների համար: մարդ.)Էական ամինաթթուների այս ցանկը մոտավորապես նույնն է այլ ողնաշարավորների և նույնիսկ միջատների մոտ: Սպիտակուցների սննդային արժեքը սովորաբար որոշվում է՝ նրանց կերակրելով աճող առնետներին և վերահսկելով կենդանիների քաշի ավելացումը:
Սպիտակուցների սննդային արժեքը. Սպիտակուցի սննդային արժեքը որոշվում է էական ամինաթթուով, որն առավել պակաս է: Սա բացատրենք օրինակով։ Մեր օրգանիզմի սպիտակուցները պարունակում են միջինը մոտ. 2% տրիպտոֆան (ըստ քաշի): Ենթադրենք, որ սննդակարգը ներառում է 1% տրիպտոֆան պարունակող 10 գ սպիտակուց, և որ դրա մեջ կան բավականաչափ այլ էական ամինաթթուներ։ Մեր դեպքում այս թերի սպիտակուցի 10 գ-ը էապես համարժեք է 5 գ ամբողջական սպիտակուցի; մնացած 5 գ-ը կարող է ծառայել միայն որպես էներգիայի աղբյուր։ Նկատի ունեցեք, որ քանի որ ամինաթթուները գործնականում չեն պահվում մարմնում, և որպեսզի սպիտակուցի սինթեզ տեղի ունենա, բոլոր ամինաթթուները պետք է միաժամանակ ներկա լինեն, էական ամինաթթուների ընդունման ազդեցությունը հնարավոր է հայտնաբերել միայն այն դեպքում, եթե դրանք բոլորը: միևնույն ժամանակ մտնել օրգանիզմ. Կենդանական սպիտակուցների մեծ մասի միջին կազմը մոտ է սպիտակուցների միջին կազմին մարդու մարմին, ուստի մենք դժվար թե բախվենք ամինաթթուների պակասի հետ, եթե մեր սննդակարգը հարուստ է մթերքներով, ինչպիսիք են միսը, ձուն, կաթը և պանիրը: Այնուամենայնիվ, կան սպիտակուցներ, ինչպիսիք են ժելատինը (կոլագենի դենատուրացիայի արտադրանք), որոնք շատ քիչ էական ամինաթթուներ են պարունակում։ Բուսական սպիտակուցները, թեև այս առումով ավելի լավն են, քան ժելատինը, բայց նաև աղքատ են էական ամինաթթուներով. Նրանք հատկապես քիչ են լիզինի և տրիպտոֆանի պարունակությամբ: Այնուամենայնիվ, զուտ բուսակերական դիետան ընդհանրապես չի կարող վնասակար համարվել, եթե այն չի սպառում մի փոքր ավելի մեծ քանակությամբ բուսական սպիտակուցներ, որոնք բավարար են օրգանիզմին էական ամինաթթուներով ապահովելու համար։ Բույսերն իրենց սերմերում պարունակում են ամենաշատ սպիտակուցը, հատկապես՝ ցորենի և տարբեր հատիկաընդեղենի սերմերում։ Երիտասարդ ընձյուղները, օրինակ՝ ծնեբեկը, նույնպես հարուստ են սպիտակուցներով։Սինթետիկ սպիտակուցներ սննդակարգում. Փոքր քանակությամբ սինթետիկ էական ամինաթթուներ կամ ամինաթթուներով հարուստ սպիտակուցներ ավելացնելով ոչ ամբողջական սպիտակուցներին, ինչպիսիք են եգիպտացորենի սպիտակուցները, վերջիններիս սննդային արժեքը կարող է զգալիորեն մեծանալ, այսինքն. դրանով իսկ մեծացնելով սպառված սպիտակուցի քանակը: Մեկ այլ հնարավորություն է բակտերիաների կամ խմորիչի աճեցումը նավթի ածխաջրածինների վրա՝ որպես ազոտի աղբյուր նիտրատների կամ ամոնիակի ավելացմամբ: Այս կերպ ստացված մանրէաբանական սպիտակուցը կարող է ծառայել որպես թռչնաբուծության կամ անասունների կեր, կամ կարող է ուղղակիորեն սպառվել մարդկանց կողմից: Երրորդ, լայնորեն կիրառվող մեթոդը օգտագործում է որոճողների ֆիզիոլոգիան: Որոճողների մոտ՝ ստամոքսի սկզբնական հատվածում, այսպես կոչված. Որովայնում բնակվում են բակտերիաների և նախակենդանիների հատուկ ձևեր, որոնք թերի բուսական սպիտակուցները վերածում են ավելի ամբողջական մանրէաբանական սպիտակուցների, իսկ դրանք, իրենց հերթին, մարսումից և կլանումից հետո վերածվում են կենդանական սպիտակուցների։ Միզանյութը՝ էժանագին սինթետիկ ազոտ պարունակող միացություն, կարող է ավելացվել անասունների կերերին։ Որովայնում ապրող միկրոօրգանիզմները օգտագործում են միզանյութի ազոտը՝ ածխաջրերը (որոնցից շատ ավելի շատ է կերերի մեջ) սպիտակուցի փոխակերպելու համար։ Անասնաբուծական կերերի ամբողջ ազոտի մոտ մեկ երրորդը կարող է հայտնվել միզանյութի տեսքով, ինչը, ըստ էության, որոշակի չափով նշանակում է սպիտակուցի քիմիական սինթեզ: ԱՄՆ-ում այս մեթոդը կարևոր դեր է խաղում որպես սպիտակուց ստանալու ուղիներից մեկը։ԳՐԱԿԱՆՈՒԹՅՈՒՆ Մյուրեյ Ռ., Գրեններ Դ., Մեյես Պ., Ռոդվել Վ. Մարդու կենսաքիմիա, հատ. 12. Մ., 1993Alberts B, Bray D, Lewis J, et al. Մոլեկուլային կենսաբանությունբջիջները, հատ. 13. Մ., 1994
Նախքան սպիտակուցի ամենակարևոր ֆիզիկական և քիմիական հատկությունների մասին խոսելը, դուք պետք է իմանաք, թե ինչից է այն բաղկացած և ինչ կառուցվածք ունի: Սպիտակուցները կարևոր բնական բիոպոլիմեր են.
Ինչ են ամինաթթուները
Սրանք օրգանական միացություններ են, որոնք պարունակում են կարբոքսիլ և ամին խմբեր: Առաջին խմբի շնորհիվ նրանք ունեն ածխածին, թթվածին և ջրածին, իսկ մյուսը՝ ազոտ և ջրածին։ Ալֆա ամինաթթուները համարվում են ամենակարևորը, քանի որ դրանք անհրաժեշտ են սպիտակուցների ձևավորման համար:
Կան էական ամինաթթուներ, որոնք կոչվում են պրոտեինոգեն ամինաթթուներ: Այսպիսով, նրանք պատասխանատու են սպիտակուցների տեսքի համար: Դրանցից ընդամենը 20-ն է, բայց դրանք կարող են առաջացնել անթիվ սպիտակուցային միացություններ: Սակայն դրանցից ոչ մեկը մյուսի հետ լիովին նույնական չի լինի։ Դա հնարավոր է դարձել այս ամինաթթուներում հայտնաբերված տարրերի համակցության շնորհիվ:
Նրանց սինթեզն օրգանիզմում չի լինում։ Հետեւաբար, նրանք այնտեղ հասնում են սննդի հետ միասին: Եթե մարդը դրանք ստանում է անբավարար քանակությամբ, ապա բնականոն գործունեությունը կարող է խաթարվել տարբեր համակարգեր. Սպիտակուցները ձևավորվում են պոլիկոնդենսացիայի ռեակցիայի միջոցով:

Սպիտակուցներ և դրանց կառուցվածքը
Նախքան սպիտակուցների ֆիզիկական հատկություններին անցնելը, արժե դրա ավելի ճշգրիտ սահմանումը տալ օրգանական միացություն. Սպիտակուցները ամենակարևոր կենսաօրգանական միացություններից են, որոնք ձևավորվում են ամինաթթուների շնորհիվ և մասնակցում են մարմնում տեղի ունեցող բազմաթիվ գործընթացներին:
Այս միացությունների կառուցվածքը կախված է ամինաթթուների մնացորդների հերթափոխի հաջորդականությունից։ Արդյունքում, այն ունի հետևյալ տեսքը.
- առաջնային (գծային);
- երկրորդական (պարույր);
- երրորդական (գլոբուլային):

Նրանց դասակարգումը
Շնորհիվ սպիտակուցային միացությունների հսկայական բազմազանության և դրանց կազմի և տարբեր կառուցվածքների բարդության տարբեր աստիճանի, հարմարության համար կան դասակարգումներ, որոնք հիմնված են այս բնութագրերի վրա:
Նրանց կազմը հետևյալն է.
- պարզ;
- համալիր, որոնք իրենց հերթին բաժանվում են.
- սպիտակուցների և ածխաջրերի համադրություն;
- սպիտակուցների և ճարպերի համադրություն;
- սպիտակուցի մոլեկուլների և նուկլեինաթթուների միացում.
Ըստ լուծելիության.
- ջրի լուծվող;
- ճարպ լուծվող.
Սպիտակուցային միացությունների կարճ նկարագրություն
Նախքան սպիտակուցների ֆիզիկական և քիմիական հատկություններին անցնելը, օգտակար կլինի դրանց մի փոքր բնութագրում տալ: Իհարկե, նրանց հատկությունները ունեն կարևորկենդանի օրգանիզմի բնականոն գործունեության համար։ Իր սկզբնական վիճակում է պինդ նյութեր, որոնք կամ լուծվում են տարբեր հեղուկների մեջ, կամ ոչ։
Հակիրճ խոսելով ֆիզիկական սպիտակուցների հատկությունները, այնուհետև նրանք որոշում են օրգանիզմի ամենակարևոր կենսաբանական գործընթացները: Օրինակ՝ նյութերի տեղափոխումը, շինարարական ֆունկցիան և այլն: Սպիտակուցների ֆիզիկական հատկությունները կախված են դրանց լուծելի լինելուց, թե ոչ: Հենց այս հատկանիշների մասին կգրվի հետագա։

Սպիտակուցների ֆիզիկական հատկությունները
Նրանց մասին վերևում արդեն գրվել է ագրեգացման վիճակև լուծելիություն։ Հետևաբար, մենք անցնում ենք հետևյալ հատկություններին.
- Նրանք ունեն մեծ մոլեկուլային քաշ, որը կախված է որոշակի պայմաններմիջավայրը։
- Դրանց լուծելիությունը լայն տիրույթ ունի, ինչի արդյունքում հնարավոր է դառնում էլեկտրոֆորեզը՝ մեթոդ, որով սպիտակուցները մեկուսացնում են խառնուրդներից։
Սպիտակուցային միացությունների քիմիական հատկությունները
Ընթերցողներն այժմ գիտեն, թե ինչ ֆիզիկական հատկություններ ունեն սպիտակուցները: Այժմ մենք պետք է խոսենք ոչ պակաս կարևոր քիմիականների մասին։ Դրանք թվարկված են ստորև.
- Դենատուրացիա. Սպիտակուցների կոագուլյացիա բարձր ջերմաստիճանի պայմաններում ուժեղ թթուներկամ ալկալիներ. Դենատուրացիայի ժամանակ պահպանվում է միայն առաջնային կառուցվածքը, այն էլ՝ բոլոր կենսաբանական հատկություններսպիտակուցները կորչում են.
- Հիդրոլիզ. Արդյունքում առաջանում են պարզ սպիտակուցներ և ամինաթթուներ, քանի որ առաջնային կառուցվածքը քայքայվում է։ Այն մարսողության գործընթացի հիմքն է։
- Սպիտակուցի որոշման որակական ռեակցիաներ. Դրանցից միայն երկուսն են, իսկ երրորդն անհրաժեշտ է այս միացություններում ծծմբի հայտնաբերման համար։
- Բիուրետի ռեակցիա.Սպիտակուցները ենթարկվում են պղնձի հիդրօքսիդի նստվածքին: Արդյունքը մանուշակագույն գույն է:
- Xantoprotein ռեակցիա. Ազդեցությունն իրականացվում է խտացված օգտագործմամբ ազոտական թթու. Այս ռեակցիայի արդյունքում ստացվում է սպիտակ նստվածք, որը տաքացնելիս դառնում է դեղին: Իսկ եթե ջուր ավելացնեք ամոնիակի լուծույթ, ապա հայտնվում է նարնջագույն գույնը:
- Սպիտակուցներում ծծմբի որոշում. Երբ սպիտակուցներն այրվում են, սկսում է զգալ «այրված եղջյուրի» հոտը։ Այս երեւույթը բացատրվում է նրանով, որ դրանք պարունակում են ծծումբ։

Այսպիսով, սրանք բոլորը սպիտակուցների ֆիզիկական և քիմիական հատկություններն էին: Բայց, իհարկե, միայն դրանց պատճառով չէ, որ դրանք համարվում են կենդանի օրգանիզմի ամենակարեւոր բաղադրիչները։ Նրանք որոշում են ամենակարևոր կենսաբանական գործառույթները:
Սպիտակուցների կենսաբանական հատկությունները
Մենք վերանայել ենք ֆիզիկական հատկություններսպիտակուցները քիմիայում. Բայց արժե նաև խոսել այն մասին, թե ինչ ազդեցություն ունեն դրանք օրգանիզմի վրա, և ինչու առանց դրանց այն ամբողջությամբ չի գործի: Սպիտակուցների հետևյալ գործառույթներն են.
- ֆերմենտային. Մարմնի ռեակցիաների մեծ մասը տեղի է ունենում սպիտակուցային ծագում ունեցող ֆերմենտների մասնակցությամբ.
- տրանսպորտ. Այս տարրերը այլ կարևոր մոլեկուլներ են փոխանցում հյուսվածքներին և օրգաններին: Ամենակարևոր տրանսպորտային սպիտակուցներից մեկը հեմոգլոբինն է.
- կառուցվածքային. Սպիտակուցները հիմնականն են շինանյութշատ հյուսվածքների համար (մկաններ, ծածկույթներ, կրող);
- պաշտպանիչ. Հակամարմինները և հակատոքսինները սպիտակուցային միացությունների հատուկ տեսակ են, որոնք կազմում են անձեռնմխելիության հիմքը.
- ազդանշան Զգայական օրգանների աշխատանքի համար պատասխանատու ընկալիչները իրենց կառուցվածքում ունեն նաև սպիտակուցներ.
- պահեստավորում. Այս գործառույթըկատարել հատուկ սպիտակուցներ, որոնք կարող են լինել շինանյութեր և լրացուցիչ էներգիայի աղբյուրներ նոր օրգանիզմների զարգացման ընթացքում:
Սպիտակուցները կարող են վերածվել ճարպերի և ածխաջրերի: Բայց նրանք չեն կարողանա սկյուռ դառնալ։ Ուստի այս կոնկրետ միացությունների բացակայությունը հատկապես վտանգավոր է կենդանի օրգանիզմի համար։ Ազատված էներգիան փոքր է և այս առումով զիջում է ճարպերին և ածխաջրերին։ Այնուամենայնիվ, դրանք օրգանիզմում էական ամինաթթուների աղբյուրն են:

Ինչպե՞ս հասկանալ, որ օրգանիզմում սպիտակուցը բավարար չէ: Մարդու առողջությունը վատթարանում է, արագ հյուծվածություն և հոգնածություն է առաջանում: Սպիտակուցի հիանալի աղբյուրներ են ցորենի, մսի և ձկնամթերքի, կաթնամթերքի, ձվի և լոբազգիների որոշ տեսակներ:
Կարևոր է իմանալ ոչ միայն սպիտակուցների ֆիզիկական, այլև քիմիական հատկությունները, ինչպես նաև իմանալ, թե դրանք ինչ նշանակություն ունեն օրգանիզմի համար կենսաբանական տեսանկյունից։ Սպիտակուցային միացությունները եզակի են նրանով, որ դրանք էական ամինաթթուների աղբյուրներ են, որոնք անհրաժեշտ են մարդու օրգանիզմի բնականոն գործունեության համար:
Ի թիվս օրգանական նյութեր սկյուռիկներ, կամ սպիտակուցներ, ամենաբազմաթիվ, ամենատարբեր և առաջնային նշանակություն ունեցող կենսապոլիմերներն են։ Նրանց բաժինն է 50 - 80% չոր բջջային զանգված:
Սպիտակուցի մոլեկուլները մեծ չափերով են, այդ պատճառով էլ կոչվում են մակրոմոլեկուլներ. Բացի ածխածնից, թթվածնից, ջրածնից և ազոտից, սպիտակուցները կարող են պարունակել ծծումբ, ֆոսֆոր և երկաթ: Սպիտակուցները միմյանցից տարբերվում են մոնոմերների քանակով (հարյուրից մինչև մի քանի հազար), կազմով և հաջորդականությամբ։ Սպիտակուցի մոնոմերները ամինաթթուներ են (նկ. 1)
Սպիտակուցների անսահման բազմազանություն է ստեղծվում ամեն ինչի տարբեր համակցություններով 20 ամինաթթուներ. Յուրաքանչյուր ամինաթթու ունի իր անունը, հատուկ կառուցվածքը և հատկությունները: Նրանց ընդհանուր բանաձևը կարելի է ներկայացնել հետևյալ կերպ.
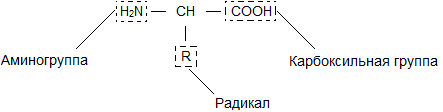
Ամինաթթվի մոլեկուլը բաղկացած է երկու մասից, որոնք նույնական են բոլոր ամինաթթուներին, որոնցից մեկը ամինո խումբն է ( -NH 2) հիմնական հատկություններով, մյուսը՝ կարբոքսիլ խմբի ( -ՔՈՀ) Հետ թթվային հատկություններ. Մոլեկուլի մի մասը, որը կոչվում է ռադիկալ ( Ռ), տարբեր ամինաթթուներ ունեն տարբեր կառուցվածք։ Հիմնական և թթվային խմբերի առկայությունը մեկ ամինաթթվի մոլեկուլում որոշում է դրանց բարձր ռեակտիվությունը։ Ամինաթթուները միավորվում են այս խմբերի միջոցով՝ ձևավորելով սպիտակուցներ: Այս դեպքում հայտնվում է ջրի մոլեկուլ, իսկ ազատված էլեկտրոնները կազմում են պեպտիդային կապ։ Ահա թե ինչու են սպիտակուցները կոչվում պոլիպեպտիդներ.
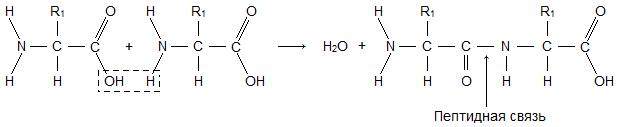
Սպիտակուցի մոլեկուլները կարող են ունենալ տարբեր տարածական կոնֆիգուրացիաներ, և դրանց կառուցվածքում կան կառուցվածքային կազմակերպման չորս մակարդակ։
Պոլիպեպտիդային շղթայում ամինաթթուների հաջորդականությունն է առաջնային կառուցվածքըսկյուռիկ. Այն յուրահատուկ է ցանկացած սպիտակուցի համար և որոշում է դրա ձևը, հատկությունները և գործառույթները:
Սպիտակուցների մեծամասնությունը պարուրաձև ձև ունի՝ դրանց միջև ջրածնային կապերի ձևավորման արդյունքում -CO-Եվ -NH-պոլիպեպտիդային շղթայի տարբեր ամինաթթուների մնացորդների խմբեր: Ջրածնային կապերը թույլ են, բայց միասին վերցրած դրանք բավականին ամուր կառուցվածք են տալիս: Այս պարույրն է երկրորդական կառուցվածքըսկյուռիկ.
Երրորդական կառուցվածք- պոլիպեպտիդային շղթայի եռաչափ տարածական «փաթեթավորում»: Արդյունքը տարօրինակ, բայց հատուկ կոնֆիգուրացիա է յուրաքանչյուր սպիտակուցի համար. գնդիկ. Երրորդական կառուցվածքի ամրությունը ապահովվում է տարբեր կապերով, որոնք առաջանում են ամինաթթուների ռադիկալների միջև։
Չորրորդական կառուցվածքբնորոշ չէ բոլոր սպիտակուցներին: Այն առաջանում է երրորդական կառուցվածքով մի քանի մակրոմոլեկուլների միացման արդյունքում բարդ համալիրի մեջ։ Օրինակ, մարդու արյան մեջ հեմոգլոբինը չորս սպիտակուցային մակրոմոլեկուլների համալիր է:
Սպիտակուցի մոլեկուլների կառուցվածքի այս բարդությունը կապված է այս կենսապոլիմերներին բնորոշ գործառույթների բազմազանության հետ:
Սպիտակուցի բնական կառուցվածքի խախտումը կոչվում է denaturation. Այն կարող է առաջանալ ջերմաստիճանի ազդեցության տակ, քիմիական նյութեր, ճառագայթային էներգիա և այլ գործոններ։ Թույլ ազդեցությամբ քայքայվում է միայն չորրորդական կառուցվածքը, ավելի ուժեղի հետ՝ երրորդականը, իսկ հետո երկրորդականը, իսկ սպիտակուցը մնում է պոլիպեպտիդային շղթայի տեսքով։
Այս գործընթացը մասամբ շրջելի է. եթե առաջնային կառուցվածքը չի վնասվել, ապա դենատուրացված սպիտակուցը կարողանում է վերականգնել իր կառուցվածքը։ Դրանից բխում է, որ սպիտակուցի մակրոմոլեկուլի բոլոր կառուցվածքային առանձնահատկությունները որոշվում են նրա առաջնային կառուցվածքով։
Բացառությամբ պարզ սպիտակուցներ, բաղկացած միայն ամինաթթուներից, կան նաև բարդ սպիտակուցներ
ՍՊԻՏԱԿՈՒՆՆԵՐ
(սպիտակուցներ), ազոտ պարունակող բարդ միացությունների դաս, կենդանի նյութի ամենաբնորոշ և կարևոր (նուկլեինաթթուների հետ մեկտեղ) բաղադրիչները։ Սպիտակուցները կատարում են բազմաթիվ և բազմազան գործառույթներ։ Սպիտակուցների մեծ մասը ֆերմենտներ են, որոնք կատալիզացնում են քիմիական ռեակցիաները: Ֆիզիոլոգիական պրոցեսները կարգավորող շատ հորմոններ նույնպես սպիտակուցներ են։ Կառուցվածքային սպիտակուցները, ինչպիսիք են կոլագենը և կերատինը, ոսկրային հյուսվածքի, մազերի և եղունգների հիմնական բաղադրիչներն են: Մկանային կծկվող սպիտակուցներն ունեն իրենց երկարությունը փոխելու հատկություն՝ օգտագործելով քիմիական էներգիան մեխանիկական աշխատանք կատարելու համար։ Սպիտակուցները ներառում են հակամարմիններ, որոնք կապում և չեզոքացնում են թունավոր նյութերը: Որոշ սպիտակուցներ, որոնք կարող են արձագանքել արտաքին ազդեցություններին (լույս, հոտ), ծառայում են որպես ընկալիչներ զգայական օրգաններում, որոնք ընկալում են գրգռվածությունը: Բջջի ներսում և բջջաթաղանթի վրա տեղակայված բազմաթիվ սպիտակուցներ կատարում են կարգավորիչ գործառույթներ։ 19-րդ դարի առաջին կեսին։ Շատ քիմիկոսներ, և նրանց թվում հիմնականում Ջ. ֆոն Լիբիգը, աստիճանաբար եկան այն եզրակացության, որ սպիտակուցները ներկայացնում են ազոտային միացությունների հատուկ դաս: «Սպիտակուցներ» անվանումը (հունարեն պրոտոսից - առաջինը) առաջարկվել է 1840 թվականին հոլանդացի քիմիկոս Գ. Մուլդերի կողմից:
ՖԻԶԻԿԱԿԱՆ ՀԱՏԿՈՒԹՅՈՒՆՆԵՐ
Սպիտակուցները պինդ վիճակում սպիտակ են, բայց լուծույթով անգույն, եթե դրանք չեն կրում քրոմոֆոր (գունավոր) խումբ, ինչպիսին է հեմոգլոբինը: Տարբեր սպիտակուցների մեջ ջրի լուծելիությունը մեծապես տարբերվում է: Այն նաև փոխվում է` կախված pH-ից և լուծույթում աղերի կոնցենտրացիայից, ուստի հնարավոր է ընտրել այնպիսի պայմաններ, որոնց դեպքում մեկ սպիտակուցը ընտրողաբար կտեղավորվի այլ սպիտակուցների առկայության դեպքում: Այս «աղով հանելու» մեթոդը լայնորեն կիրառվում է սպիտակուցների մեկուսացման և մաքրման համար։ Մաքրված սպիտակուցը հաճախ նստում է լուծույթից բյուրեղների տեսքով: Այլ միացությունների համեմատ, սպիտակուցների մոլեկուլային քաշը շատ մեծ է՝ մի քանի հազարից մինչև միլիոնավոր դալտոններ: Հետևաբար, ուլտրակենտրոնացման ժամանակ սպիտակուցները նստում են, այն էլ՝ տարբեր արագությամբ։ Սպիտակուցի մոլեկուլներում դրական և բացասական լիցքավորված խմբերի առկայության պատճառով դրանք շարժվում են տարբեր արագություններով և էլեկտրական դաշտում։
ՔԻՄԻԱԿԱՆ ՀԱՏԿՈՒԹՅՈՒՆՆԵՐ
Սա էլեկտրաֆորեզի հիմքն է՝ մեթոդ, որն օգտագործվում է առանձին սպիտակուցները բարդ խառնուրդներից մեկուսացնելու համար։ Սպիտակուցները նույնպես մաքրվում են քրոմատագրման միջոցով։
Որտեղ R-ը ջրածնի ատոմ է կամ որոշ օրգանական խումբ: Սպիտակուցի մոլեկուլը (պոլիպեպտիդային շղթա) կարող է բաղկացած լինել միայն համեմատաբար փոքր թվով ամինաթթուներից կամ մի քանի հազար մոնոմերային միավորներից։ Ամինաթթուների համակցությունը շղթայում հնարավոր է, քանի որ դրանցից յուրաքանչյուրն ունի երկու տարբեր քիմիական խմբեր՝ հիմնական ամինախումբ՝ NH2 և թթվային կարբոքսիլ խումբ՝ COOH։ Այս երկու խմբերն էլ կապված են a-ածխածնի ատոմին։ Մեկ ամինաթթվի կարբոքսիլ խումբը կարող է ձևավորել ամիդային (պեպտիդ) կապ մեկ այլ ամինաթթվի ամինո խմբի հետ.

Երկու ամինաթթուների այս ձևով կապվելուց հետո շղթան կարող է երկարացվել՝ երկրորդ ամինաթթուն ավելացնելով երրորդը և այլն: Ինչպես երևում է վերը նշված հավասարումից, երբ ձևավորվում է պեպտիդային կապ, ազատվում է ջրի մոլեկուլ։ Թթուների, ալկալիների կամ պրոտեոլիտիկ ֆերմենտների առկայության դեպքում ռեակցիան ընթանում է հակառակ ուղղությամբ՝ պոլիպեպտիդային շղթան ջրի ավելացումով բաժանվում է ամինաթթուների։ Այս ռեակցիան կոչվում է հիդրոլիզ։ Հիդրոլիզը տեղի է ունենում ինքնաբերաբար, և էներգիա է պահանջվում ամինաթթուները պոլիպեպտիդային շղթայի մեջ միացնելու համար: Կարբոքսիլ խումբը և ամիդային խումբը (կամ նմանատիպ իմիդ խումբը ամինաթթվի պրոլինի դեպքում) առկա են բոլոր ամինաթթուներում, սակայն ամինաթթուների միջև տարբերությունները որոշվում են խմբի բնույթով կամ «կողային շղթայով»: որը վերը նշված է R տառով: Կողային շղթայի դերը կարող է խաղալ ջրածնի ատոմը, ինչպես ամինաթթու գլիկինը, և որոշ մեծ խումբ, ինչպես հիստիդինը և տրիպտոֆանը: Որոշ կողային շղթաներ քիմիապես իներտ են, իսկ մյուսները նկատելիորեն ռեակտիվ են: Շատ հազարավոր տարբեր ամինաթթուներ կարող են սինթեզվել, և շատ տարբեր ամինաթթուներ են հանդիպում բնության մեջ, սակայն սպիտակուցի սինթեզի համար օգտագործվում են միայն 20 տեսակի ամինաթթուներ՝ ալանին, արգինին, ասպարագին, ասպարթաթթու, վալին, հիստիդին, գլիցին, գլուտամին, գլուտամին: թթու, իզոլեյցին, լեյցին, լիզին, մեթիոնին, պրոլին, սերին, թիրոզին, թրեոնին, տրիպտոֆան, ֆենիլալանին և ցիստեին (սպիտակուցներում ցիստեինը կարող է առկա լինել որպես դիմեր - ցիստին): Ճիշտ է, որոշ սպիտակուցներ պարունակում են նաև այլ ամինաթթուներ, բացի կանոնավոր հանդիպող քսանից, բայց դրանք ձևավորվում են թվարկված քսանից մեկի փոփոխության արդյունքում այն սպիտակուցի մեջ ներառվելուց հետո:
Օպտիկական ակտիվություն.Բոլոր ամինաթթուները, բացառությամբ գլիցինի, ունեն չորս տարբեր խմբեր, որոնք կցված են a-ածխածնի ատոմին: Երկրաչափության տեսանկյունից չորս տարբեր խմբեր կարող են կցվել երկու եղանակով, և, համապատասխանաբար, կան երկու հնարավոր կոնֆիգուրացիաներ կամ երկու իզոմերներ, որոնք կապված են միմյանց հետ, քանի որ առարկան իր հայելային պատկերին է, այսինքն. ինչպես ձախ ձեռքը դեպի աջ: Մի կոնֆիգուրացիան կոչվում է ձախակողմյան կամ ձախլիկ (L), իսկ մյուսը աջակողմյան կամ աջակողմյան (D), քանի որ երկու իզոմերները տարբերվում են բևեռացված լույսի հարթության պտտման ուղղությամբ: Սպիտակուցներում հայտնաբերված են միայն L-ամինաթթուներ (բացառություն է գլիցինը, այն կարելի է գտնել միայն մեկ ձևով, քանի որ նրա չորս խմբերից երկուսը նույնն են), և բոլորն էլ օպտիկական ակտիվ են (քանի որ կա միայն մեկ իզոմեր): D-ամինաթթուները բնության մեջ հազվադեպ են. դրանք հայտնաբերված են որոշ հակաբիոտիկների և բակտերիաների բջջային պատի մեջ:
Ամինաթթուների հաջորդականությունը.Պոլիպեպտիդային շղթայում ամինաթթուները դասավորված են ոչ թե պատահական, այլ որոշակի ֆիքսված հերթականությամբ, և հենց այս կարգն է որոշում սպիտակուցի գործառույթներն ու հատկությունները։ Փոփոխելով ամինաթթուների 20 տեսակների հերթականությունը՝ դուք կարող եք ստեղծել հսկայական քանակությամբ տարբեր սպիտակուցներ, ինչպես այբուբենի տառերից կարող եք ստեղծել բազմաթիվ տարբեր տեքստեր: Նախկինում սպիտակուցի ամինաթթուների հաջորդականությունը որոշելը հաճախ տևում էր մի քանի տարի: Ուղղակի որոշումը դեռևս բավականին աշխատատար խնդիր է, թեև ստեղծվել են սարքեր, որոնք թույլ են տալիս այն իրականացնել ավտոմատ կերպով։ Սովորաբար ավելի հեշտ է որոշել համապատասխան գենի նուկլեոտիդային հաջորդականությունը և դրանից դուրս բերել սպիտակուցի ամինաթթուների հաջորդականությունը։ Մինչ օրս արդեն որոշված են հարյուրավոր սպիտակուցների ամինաթթուների հաջորդականությունը։ Վերծանված սպիտակուցների գործառույթները սովորաբար հայտնի են, և դա օգնում է պատկերացնել նմանատիպ սպիտակուցների հնարավոր գործառույթները, որոնք ձևավորվում են, օրինակ, չարորակ նորագոյացություններում:
Բարդ սպիտակուցներ.Միայն ամինաթթուներից բաղկացած սպիտակուցները կոչվում են պարզ: Հաճախ, սակայն, մետաղի ատոմը կամ որոշ քիմիական միացություն, որը ամինաթթու չէ, կցվում է պոլիպեպտիդային շղթային։ Նման սպիտակուցները կոչվում են բարդ: Օրինակ՝ հեմոգլոբինը. այն պարունակում է երկաթի պորֆիրին, որը որոշում է նրա կարմիր գույնը և թույլ է տալիս նրան հանդես գալ որպես թթվածնի կրիչ։ Բարդ սպիտակուցների անունները ցույց են տալիս կցված խմբերի բնույթը՝ գլիկոպրոտեինները պարունակում են շաքարներ, լիպոպրոտեինները՝ ճարպեր։ Եթե ֆերմենտի կատալիտիկ ակտիվությունը կախված է կցված խմբից, ապա այն կոչվում է պրոթեզային խումբ։ Հաճախ վիտամինը պրոթեզային խմբի դեր է կատարում կամ դրա մի մասն է: Վիտամին A-ն, օրինակ, կցված է ցանցաթաղանթի սպիտակուցներից մեկին, որոշում է նրա զգայունությունը լույսի նկատմամբ։
Երրորդական կառուցվածք. Կարևորը ոչ այնքան բուն սպիտակուցի ամինաթթուների հաջորդականությունն է (առաջնային կառուցվածքը), այլ այն, թե ինչպես է այն դրված տիեզերքում: Պոլիպեպտիդային շղթայի ողջ երկարությամբ ջրածնի իոնները կազմում են կանոնավոր ջրածնային կապեր, որոնք տալիս են նրան պարույրի կամ շերտի (երկրորդական կառուցվածք) տեսք։ Նման խխունջների և շերտերի համադրությունից առաջանում է հաջորդ կարգի կոմպակտ ձև՝ սպիտակուցի երրորդական կառուցվածք։ Շղթայի մոնոմերային միավորները պահող կապերի շուրջ հնարավոր են փոքր անկյուններով պտույտներ։ Հետևաբար, զուտ երկրաչափական տեսանկյունից, ցանկացած պոլիպեպտիդային շղթայի համար հնարավոր կոնֆիգուրացիաների թիվը անսահման մեծ է: Իրականում յուրաքանչյուր սպիտակուց սովորաբար գոյություն ունի միայն մեկ կոնֆիգուրացիայի մեջ, որը որոշվում է իր ամինաթթուների հաջորդականությամբ: Այս կառուցվածքը կոշտ չէ, այն կարծես «շնչում է»՝ այն տատանվում է որոշակի միջին կոնֆիգուրացիայի շուրջ: Շղթան ծալվում է այնպիսի կոնֆիգուրացիայի մեջ, որում ազատ էներգիան (աշխատանք արտադրելու ունակությունը) նվազագույն է, ճիշտ այնպես, ինչպես արձակված զսպանակը սեղմվում է միայն նվազագույն ազատ էներգիային համապատասխան վիճակի: Հաճախ շղթայի մի մասը սերտորեն կապված է մյուսի հետ երկու ցիստեին մնացորդների միջև դիսուլֆիդային (-S-S-) կապերով: Մասամբ սա է պատճառը, որ ցիստեինը հատկապես կարևոր դեր է խաղում ամինաթթուների մեջ: Սպիտակուցների կառուցվածքի բարդությունն այնքան մեծ է, որ դեռևս հնարավոր չէ հաշվարկել սպիտակուցի երրորդական կառուցվածքը, նույնիսկ եթե հայտնի է նրա ամինաթթուների հաջորդականությունը։ Բայց եթե հնարավոր է ստանալ սպիտակուցային բյուրեղներ, ապա դրա երրորդական կառուցվածքը կարելի է որոշել ռենտգենյան դիֆրակցիայով։ Կառուցվածքային, կծկվող և որոշ այլ սպիտակուցներում շղթաները երկարաձգվում են, և մոտակայքում ընկած մի քանի թեթև ծալված շղթաներ ձևավորում են մանրաթելեր. մանրաթելերն իրենց հերթին ծալվում են ավելի մեծ գոյացությունների՝ մանրաթելերի։ Այնուամենայնիվ, լուծույթում գտնվող սպիտակուցների մեծ մասը ունեն գնդաձև ձև. շղթաները ոլորված են գնդիկի մեջ, ինչպես մանվածքը գնդակի մեջ: Այս կոնֆիգուրացիայով ազատ էներգիան նվազագույն է, քանի որ հիդրոֆոբ («ջուր վանող») ամինաթթուները թաքնված են գլոբուլի ներսում, իսկ հիդրոֆիլ («ջուր ձգող») ամինաթթուները՝ դրա մակերեսին։ Շատ սպիտակուցներ մի քանի պոլիպեպտիդ շղթաների համալիրներ են: Այս կառուցվածքը կոչվում է սպիտակուցի չորրորդական կառուցվածք։ Հեմոգլոբինի մոլեկուլը, օրինակ, բաղկացած է չորս ենթամիավորներից, որոնցից յուրաքանչյուրը գնդաձեւ սպիտակուց է։ Կառուցվածքային սպիտակուցները, իրենց գծային կոնֆիգուրացիայի շնորհիվ, ձևավորում են մանրաթելեր, որոնք ունեն շատ բարձր առաձգական ուժ, մինչդեռ գնդաձև կոնֆիգուրացիան թույլ է տալիս սպիտակուցներին հատուկ փոխազդեցության մեջ մտնել այլ միացությունների հետ: Գնդիկի մակերեսին, երբ շղթաները ճիշտ դրված են, հայտնվում են որոշակի ձևի խոռոչներ, որոնցում տեղակայված են ռեակտիվ քիմիական խմբեր: Եթե սպիտակուցը ֆերմենտ է, ապա ինչ-որ նյութի մեկ այլ, սովորաբար ավելի փոքր, մոլեկուլ մտնում է այդպիսի խոռոչ, ինչպես որ բանալին մտնում է կողպեք; այս դեպքում մոլեկուլի էլեկտրոնային ամպի կոնֆիգուրացիան փոխվում է խոռոչում տեղակայված քիմիական խմբերի ազդեցության տակ, և դա ստիպում է նրան արձագանքել որոշակի ձևով: Այս կերպ ֆերմենտը կատալիզացնում է ռեակցիան։ Հակամարմինների մոլեկուլներն ունեն նաև խոռոչներ, որոնցում կապվում են տարբեր օտար նյութեր և դրանով իսկ անվնաս են դառնում։ «Կողպեք և բանալին» մոդելը, որը բացատրում է սպիտակուցների փոխազդեցությունը այլ միացությունների հետ, թույլ է տալիս հասկանալ ֆերմենտների և հակամարմինների առանձնահատկությունները, այսինքն. միայն որոշակի միացությունների հետ արձագանքելու նրանց ունակությունը: Սպիտակուցներ տարբեր տեսակի օրգանիզմներում. Սպիտակուցները, որոնք կատարում են նույն գործառույթը բույսերի և կենդանիների տարբեր տեսակների մեջ և, հետևաբար, կրում են նույն անվանումը, նույնպես ունեն նմանատիպ կոնֆիգուրացիա: Նրանք, սակայն, որոշ չափով տարբերվում են իրենց ամինաթթուների հաջորդականությամբ: Քանի որ տեսակները տարբերվում են ընդհանուր նախնուց, որոշ ամինաթթուներ որոշակի դիրքերում փոխարինվում են մյուսների կողմից մուտացիաներով: Վնասակար մուտացիաները, որոնք առաջացնում են ժառանգական հիվանդություններ, վերացվում են բնական ընտրության միջոցով, սակայն օգտակար կամ առնվազն չեզոքները կարող են պահպանվել: Որքան ավելի մոտ են երկու տեսակները միմյանց, այնքան քիչ տարբերություններ են հայտնաբերվում նրանց սպիտակուցներում: Որոշ սպիտակուցներ փոխվում են համեմատաբար արագ, մյուսները շատ պահպանված են: Վերջինս ներառում է, օրինակ, ցիտոքրոմ c, շնչառական ֆերմենտ, որը հայտնաբերված է կենդանի օրգանիզմների մեծ մասում: Մարդկանց և շիմպանզեների մոտ նրա ամինաթթուների հաջորդականությունը նույնական է, սակայն ցորենի ցիտոքրոմ c-ում ամինաթթուների միայն 38%-ն է տարբերվում: Նույնիսկ մարդկանց և բակտերիաների համեմատության ժամանակ կարելի է նկատել ցիտոքրոմ c-ի նմանությունը (տարբերությունները ազդում են ամինաթթուների 65%-ի վրա), թեև բակտերիաների և մարդկանց ընդհանուր նախահայրն ապրել է Երկրի վրա մոտ երկու միլիարդ տարի առաջ: Մեր օրերում ամինաթթուների հաջորդականությունների համեմատությունը հաճախ օգտագործվում է ֆիլոգենետիկ (ընտանեկան) ծառ կառուցելու համար՝ արտացոլելով տարբեր օրգանիզմների միջև էվոլյուցիոն հարաբերությունները։
Դենատուրացիա.Սինթեզված սպիտակուցի մոլեկուլը՝ ծալովի, ձեռք է բերում իր բնորոշ կոնֆիգուրացիան։ Այնուամենայնիվ, այս կոնֆիգուրացիան կարող է ոչնչացվել տաքացման, pH-ի փոփոխման, օրգանական լուծիչների ազդեցության միջոցով և նույնիսկ լուծույթը պարզապես թափահարելով, մինչև դրա մակերեսին փուչիկները հայտնվեն: Այս ձևով ձևափոխված սպիտակուցը կոչվում է դենատուրացված; այն կորցնում է իր կենսաբանական ակտիվությունը և սովորաբար դառնում է անլուծելի։ Դենատուրացված սպիտակուցի հայտնի օրինակներ են խաշած ձվերը կամ հարած սերուցքը: Փոքր սպիտակուցները, որոնք պարունակում են ընդամենը մոտ հարյուր ամինաթթուներ, ունակ են վերածնվել, այսինքն. նորից ձեռք բերել սկզբնական կազմաձևը: Բայց սպիտակուցների մեծ մասը պարզապես վերածվում է խճճված պոլիպեպտիդային շղթաների զանգվածի և չի վերականգնում իրենց նախկին կոնֆիգուրացիան։ Ակտիվ սպիտակուցների մեկուսացման հիմնական դժվարություններից մեկը նրանց ծայրահեղ զգայունությունն է դենատուրացիայի նկատմամբ: Սպիտակուցների այս հատկությունը օգտակար կիրառություն է գտնում սննդամթերքի պահպանման գործում. բարձր ջերմաստիճանն անդառնալիորեն դենատուրացիա է անում միկրոօրգանիզմների ֆերմենտները, և միկրոօրգանիզմները մահանում են:
ՍՊՏՈՒՏԻՆՆԵՐԻ ՍԻՆԹԵԶ
Սպիտակուցը սինթեզելու համար կենդանի օրգանիզմը պետք է ունենա ֆերմենտների համակարգ, որը կարող է միացնել մի ամինաթթուն մյուսին։ Անհրաժեշտ է նաև տեղեկատվության աղբյուր՝ որոշելու համար, թե որ ամինաթթուները պետք է համակցվեն: Քանի որ մարմնում կան հազարավոր տեսակի սպիտակուցներ, և դրանցից յուրաքանչյուրը բաղկացած է միջինում մի քանի հարյուր ամինաթթուներից, պահանջվող տեղեկատվությունը պետք է իսկապես հսկայական լինի: Այն պահվում է (նման է, թե ինչպես է ձայնագրությունը պահվում մագնիսական ժապավենի վրա) գեները կազմող նուկլեինաթթվի մոլեկուլներում։
Տես նաև
ԺԱՌԱՆԳՈՒԹՅՈՒՆ;
ՆՈՒԿԼԵԻԿ ԹԹՈՒՆԵՐ.
Ֆերմենտների ակտիվացում.Ամինաթթուներից սինթեզված պոլիպեպտիդային շղթան միշտ չէ, որ սպիտակուց է իր վերջնական ձևով: Շատ ֆերմենտներ սկզբում սինթեզվում են որպես ոչ ակտիվ պրեկուրսորներ և ակտիվանում են միայն այն բանից հետո, երբ մեկ այլ ֆերմենտ հեռացնում է մի քանի ամինաթթուներ շղթայի մի ծայրից: Որոշ մարսողական ֆերմենտներ, ինչպիսիք են տրիպսինը, սինթեզվում են այս ոչ ակտիվ ձևով. այս ֆերմենտները ակտիվանում են մարսողական տրակտում շղթայի տերմինալ հատվածի հեռացման արդյունքում։ Ինսուլին հորմոնը, որի մոլեկուլն իր ակտիվ ձևով բաղկացած է երկու կարճ շղթայից, սինթեզվում է մեկ շղթայի տեսքով, այսպես կոչված. պրոինսուլին. Այնուհետև այս շղթայի միջին մասը հանվում է, իսկ մնացած բեկորները միանում են՝ ձևավորելով ակտիվ հորմոնի մոլեկուլը: Կոմպլեքս սպիտակուցները ձևավորվում են միայն այն բանից հետո, երբ որոշակի քիմիական խումբ կցվում է սպիտակուցին, և այդ կցումը հաճախ պահանջում է նաև ֆերմենտ:
Նյութափոխանակության շրջանառություն.Կենդանիներին ածխածնի, ազոտի կամ ջրածնի ռադիոակտիվ իզոտոպներով պիտակավորված ամինաթթուներով կերակրելուց հետո պիտակը արագորեն ներառվում է նրա սպիտակուցների մեջ: Եթե պիտակավորված ամինաթթուները դադարում են մտնել օրգանիզմ, ապա սպիտակուցներում պիտակի քանակը սկսում է նվազել: Այս փորձերը ցույց են տալիս, որ ստացված սպիտակուցները օրգանիզմում չեն պահվում մինչև կյանքի վերջ։ Նրանք բոլորը, չնչին բացառություններով, գտնվում են դինամիկ վիճակում, անընդհատ տրոհվում են ամինաթթուների, իսկ հետո նորից սինթեզվում։ Որոշ սպիտակուցներ քայքայվում են, երբ բջիջները մահանում են և ոչնչացվում: Դա տեղի է ունենում անընդհատ, օրինակ, կարմիր արյան բջիջների և էպիթելային բջիջների դեպքում, որոնք ծածկում են աղիքի ներքին մակերեսը: Բացի այդ, սպիտակուցների քայքայումն ու վերասինթեզը տեղի է ունենում նաև կենդանի բջիջներում։ Տարօրինակ կերպով, սպիտակուցների քայքայման մասին ավելի քիչ է հայտնի, քան դրանց սինթեզի մասին: Ակնհայտ է, սակայն, որ տրոհումը ներառում է պրոտեոլիտիկ ֆերմենտներ, որոնք նման են նրանց, որոնք սպիտակուցները տրոհում են մարսողական տրակտում ամինաթթուների: Տարբեր սպիտակուցների կիսամյակը տատանվում է՝ մի քանի ժամից մինչև մի քանի ամիս: Միակ բացառությունը կոլագենի մոլեկուլներն են: Ձևավորվելուց հետո դրանք մնում են կայուն և չեն թարմացվում կամ փոխարինվում: Այնուամենայնիվ, ժամանակի ընթացքում դրանց որոշ հատկություններ փոխվում են, մասնավորապես առաձգականությունը, և քանի որ դրանք չեն թարմացվում, դա հանգեցնում է որոշակի տարիքային փոփոխությունների, ինչպիսիք են մաշկի վրա կնճիռների տեսքը:
Սինթետիկ սպիտակուցներ.Քիմիկոսները վաղուց սովորել են պոլիմերացնել ամինաթթուները, սակայն ամինաթթուները միաձուլվում են անկանոն կերպով, այնպես որ նման պոլիմերացման արտադրանքը քիչ նմանություն ունի բնականին։ Ճիշտ է, հնարավոր է միավորել ամինաթթուները տվյալ հերթականությամբ, ինչը հնարավորություն է տալիս ստանալ որոշ կենսաբանական ակտիվ սպիտակուցներ, մասնավորապես՝ ինսուլին։ Գործընթացը բավականին բարդ է, և այս կերպ հնարավոր է ստանալ միայն այն սպիտակուցները, որոնց մոլեկուլները պարունակում են մոտ հարյուր ամինաթթուներ։ Փոխարենը նախընտրելի է սինթեզել կամ մեկուսացնել գենի նուկլեոտիդային հաջորդականությունը, որը համապատասխանում է ցանկալի ամինաթթուների հաջորդականությանը, այնուհետև այդ գենը ներմուծել բակտերիա, որը կարտադրի մեծ քանակությամբ ցանկալի արտադրանքը բազմապատկման միջոցով: Այս մեթոդը, սակայն, ունի նաև իր թերությունները.
Տես նաևԳԵՆԵՏԻԿԱԿԱՆ ԻՆԺԵՆԻՏԻԱ.
ՍՊԵՏՈՒՆԻԿ ԵՎ ՍՆՆԴԻՐ
Երբ մարմնում սպիտակուցները տրոհվում են ամինաթթուների, այդ ամինաթթուները կարող են կրկին օգտագործվել սպիտակուցներ սինթեզելու համար: Միևնույն ժամանակ, ամինաթթուներն իրենք ենթակա են քայքայման, ուստի դրանք ամբողջությամբ չեն վերաօգտագործվում: Պարզ է նաև, որ աճի, հղիության և վերքերի բուժման ընթացքում սպիտակուցի սինթեզը պետք է գերազանցի քայքայմանը: Մարմինը անընդհատ կորցնում է որոշ սպիտակուցներ. Սրանք մազերի, եղունգների և մաշկի մակերեսային շերտի սպիտակուցներն են։ Ուստի սպիտակուցներ սինթեզելու համար յուրաքանչյուր օրգանիզմ պետք է ամինաթթուներ ստանա սննդից։
Ամինաթթուների աղբյուրները.Կանաչ բույսերը սինթեզում են բոլոր 20 ամինաթթուները, որոնք առկա են սպիտակուցներում CO2-ից, ջրից և ամոնիակից կամ նիտրատներից: Շատ բակտերիաներ կարող են նաև սինթեզել ամինաթթուներ շաքարի (կամ որոշ համարժեքի) և ֆիքսված ազոտի առկայության դեպքում, սակայն շաքարը, ի վերջո, մատակարարվում է կանաչ բույսերի կողմից: Կենդանիներն ունեն ամինաթթուներ սինթեզելու սահմանափակ կարողություն. նրանք ամինաթթուներ են ստանում՝ ուտելով կանաչ բույսեր կամ այլ կենդանիներ։ Մարսողական համակարգում ներծծվող սպիտակուցները տրոհվում են ամինաթթուների, վերջիններս ներծծվում են, և դրանցից կառուցվում են տվյալ օրգանիզմին բնորոշ սպիտակուցներ։ Կլանված սպիտակուցներից ոչ մեկը, որպես այդպիսին, չի մտնում մարմնի կառուցվածքների մեջ: Միակ բացառությունն այն է, որ շատ կաթնասունների մոտ որոշ մայրական հակամարմիններ կարող են անձեռնմխելիորեն պլասենցայի միջով անցնել պտղի արյան հոսք, իսկ մոր կաթի միջոցով (հատկապես որոճողների մոտ) կարող են փոխանցվել նորածինին ծնվելուց անմիջապես հետո:
Սպիտակուցի պահանջ.Հասկանալի է, որ կյանքը պահպանելու համար օրգանիզմը պետք է որոշակի քանակությամբ սպիտակուց ստանա սննդից։ Այնուամենայնիվ, այս անհրաժեշտության չափը կախված է մի շարք գործոններից: Մարմինը սննդի կարիք ունի և՛ որպես էներգիայի աղբյուր (կալորիականություն), և՛ որպես նյութ՝ իր կառուցվածքները կառուցելու համար։ Էներգիայի կարիքն առաջին տեղում է: Սա նշանակում է, որ երբ սննդակարգում քիչ ածխաջրեր և ճարպեր կան, դիետիկ սպիտակուցներն օգտագործվում են ոչ թե սեփական սպիտակուցների սինթեզի համար, այլ որպես կալորիաների աղբյուր։ Երկարատև ծոմապահության ժամանակ նույնիսկ ձեր սեփական սպիտակուցներն են օգտագործվում էներգիայի կարիքները բավարարելու համար։ Եթե սննդակարգում բավարար քանակությամբ ածխաջրեր կան, ապա սպիտակուցի սպառումը կարող է կրճատվել:
Ազոտի հավասարակշռությունը. Միջին հաշվով մոտ. Սպիտակուցի ընդհանուր զանգվածի 16%-ը ազոտ է։ Երբ սպիտակուցներում պարունակվող ամինաթթուները քայքայվում են, նրանց մեջ պարունակվող ազոտը օրգանիզմից դուրս է գալիս մեզով և (ավելի քիչ չափով) կղանքով՝ տարբեր ազոտային միացությունների տեսքով։ Ուստի հարմար է օգտագործել այնպիսի ցուցանիշ, ինչպիսին է ազոտի հավասարակշռությունը՝ սպիտակուցային սնուցման որակը գնահատելու համար, այսինքն. տարբերությունը (գրամներով) օրգանիզմ մտնող ազոտի քանակի և օրական արտազատվող ազոտի քանակի միջև։ Մեծահասակների նորմալ սնուցման դեպքում այդ քանակները հավասար են: Աճող օրգանիզմում արտազատվող ազոտի քանակը պակաս է ստացվածից, այսինքն. հաշվեկշիռը դրական է. Եթե սննդակարգում սպիտակուցի պակաս կա, հավասարակշռությունը բացասական է։ Եթե սննդակարգում կա բավարար կալորիա, բայց դրա մեջ չկան սպիտակուցներ, օրգանիզմը խնայում է սպիտակուցները։ Միևնույն ժամանակ, սպիտակուցային նյութափոխանակությունը դանդաղում է, և ամինաթթուների կրկնակի օգտագործումը սպիտակուցների սինթեզում տեղի է ունենում առավելագույն արդյունավետությամբ: Այնուամենայնիվ, կորուստներն անխուսափելի են, և ազոտային միացությունները դեռևս արտազատվում են մեզով և մասամբ՝ կղանքով։ Սպիտակուցների ծոմապահության ժամանակ օրգանիզմից օրական արտազատվող ազոտի քանակը կարող է ծառայել որպես օրական սպիտակուցի պակասի չափիչ։ Բնական է ենթադրել, որ սննդակարգ մտցնելով այս պակասին համարժեք սպիտակուցի քանակություն, կարելի է վերականգնել ազոտի հավասարակշռությունը։ Սակայն դա ճիշտ չէ։ Այս քանակությամբ սպիտակուց ստանալուց հետո մարմինը սկսում է ավելի քիչ արդյունավետ օգտագործել ամինաթթուները, ուստի որոշ լրացուցիչ սպիտակուցներ են պահանջվում ազոտի հավասարակշռությունը վերականգնելու համար: Եթե սննդակարգում սպիտակուցի քանակությունը գերազանցում է այն, ինչ անհրաժեշտ է ազոտի հավասարակշռությունը պահպանելու համար, ապա թվում է, որ վնաս չկա: Ավելորդ ամինաթթուները պարզապես օգտագործվում են որպես էներգիայի աղբյուր: Որպես հատկապես վառ օրինակ, էսկիմոսները օգտագործում են քիչ ածխաջրեր և մոտ տասն անգամ ավելի շատ սպիտակուցներ, որոնք անհրաժեշտ են ազոտի հավասարակշռությունը պահպանելու համար: Այնուամենայնիվ, շատ դեպքերում սպիտակուցը որպես էներգիայի աղբյուր օգտագործելը ձեռնտու չէ, քանի որ ածխաջրերի որոշակի քանակությունը կարող է շատ ավելի շատ կալորիա արտադրել, քան նույն քանակությամբ սպիտակուցը: Աղքատ երկրներում մարդիկ իրենց կալորիաները ստանում են ածխաջրերից և սպառում են նվազագույն քանակությամբ սպիտակուցներ: Եթե օրգանիզմը ստանում է անհրաժեշտ քանակությամբ կալորիաներ ոչ սպիտակուցային մթերքների տեսքով, ապա ազոտի հավասարակշռության պահպանումն ապահովելու համար սպիտակուցի նվազագույն քանակությունը կազմում է մոտ. 30 գ օրական. Այսքան սպիտակուց է պարունակվում չորս կտոր հացում կամ 0,5 լիտր կաթում։ Մի փոքր ավելի մեծ թիվը սովորաբար համարվում է օպտիմալ; Խորհուրդ է տրվում 50-ից 70 գ:
Հիմնական ամինաթթուներ.Մինչ այժմ սպիտակուցը համարվում էր որպես ամբողջություն։ Մինչդեռ, որպեսզի սպիտակուցի սինթեզ տեղի ունենա, օրգանիզմում պետք է առկա լինեն բոլոր անհրաժեշտ ամինաթթուները։ Կենդանու մարմինն ինքնին ունակ է սինթեզել որոշ ամինաթթուներ: Դրանք կոչվում են փոխարինելի, քանի որ պարտադիր չէ, որ դրանք առկա լինեն սննդակարգում. կարևոր է միայն, որ սպիտակուցի ընդհանուր մատակարարումը որպես ազոտի աղբյուր բավարար լինի. ապա, եթե կա ոչ էական ամինաթթուների պակաս, ապա մարմինը կարող է սինթեզել դրանք ավելցուկային առկաների հաշվին։ Մնացած, «էական» ամինաթթուները չեն կարող սինթեզվել և պետք է մարմնին մատակարարվեն սննդի միջոցով: Մարդկանց համար անհրաժեշտ են վալինը, լեյցինը, իզոլեյցինը, թրեոնինը, մեթիոնինը, ֆենիլալանինը, տրիպտոֆանը, հիստիդինը, լիզինը և արգինինը: (Չնայած արգինինը կարող է սինթեզվել մարմնում, այն դասակարգվում է որպես էական ամինաթթու, քանի որ այն բավարար քանակությամբ չի արտադրվում նորածինների և աճող երեխաների մոտ: Մյուս կողմից, սննդի այս ամինաթթուների մի մասը կարող է անհարկի դառնալ մեծահասակների համար: անձ:) Էական ամինաթթուների այս ցանկը ամինաթթուները նույնպես մոտավորապես նույնն են այլ ողնաշարավորների և նույնիսկ միջատների մոտ: Սպիտակուցների սննդային արժեքը սովորաբար որոշվում է՝ նրանց կերակրելով աճող առնետներին և վերահսկելով կենդանիների քաշի ավելացումը:
Սպիտակուցների սննդային արժեքը.Սպիտակուցի սննդային արժեքը որոշվում է էական ամինաթթուով, որն առավել պակաս է: Սա բացատրենք օրինակով։ Մեր օրգանիզմի սպիտակուցները պարունակում են միջինը մոտ. 2% տրիպտոֆան (ըստ քաշի): Ենթադրենք, որ սննդակարգը ներառում է 1% տրիպտոֆան պարունակող 10 գ սպիտակուց, և որ դրա մեջ կան բավականաչափ այլ էական ամինաթթուներ։ Մեր դեպքում այս թերի սպիտակուցի 10 գ-ը էապես համարժեք է 5 գ ամբողջական սպիտակուցի; մնացած 5 գ-ը կարող է ծառայել միայն որպես էներգիայի աղբյուր։ Նկատի ունեցեք, որ քանի որ ամինաթթուները գործնականում չեն պահվում մարմնում, և որպեսզի սպիտակուցի սինթեզ տեղի ունենա, բոլոր ամինաթթուները պետք է միաժամանակ ներկա լինեն, էական ամինաթթուների ընդունման ազդեցությունը հնարավոր է հայտնաբերել միայն այն դեպքում, եթե դրանք բոլորը: միևնույն ժամանակ մտնել օրգանիզմ: Կենդանական սպիտակուցների մեծ մասի միջին բաղադրությունը մոտ է մարդու օրգանիզմի սպիտակուցների միջին բաղադրությանը, ուստի մենք դժվար թե հանդիպենք ամինաթթուների պակասի, եթե մեր սննդակարգը հարուստ է մթերքներով, ինչպիսիք են միսը, ձուն, կաթը և պանիրը: Այնուամենայնիվ, կան սպիտակուցներ, ինչպիսիք են ժելատինը (կոլագենի դենատուրացիայի արտադրանք), որոնք շատ քիչ էական ամինաթթուներ են պարունակում։ Բուսական սպիտակուցները, թեև այս առումով ավելի լավն են, քան ժելատինը, բայց նաև աղքատ են էական ամինաթթուներով. Նրանք հատկապես քիչ են լիզինի և տրիպտոֆանի պարունակությամբ: Այնուամենայնիվ, զուտ բուսակերական դիետան ընդհանրապես չի կարող վնասակար համարվել, եթե այն չի սպառում մի փոքր ավելի մեծ քանակությամբ բուսական սպիտակուցներ, որոնք բավարար են օրգանիզմին էական ամինաթթուներով ապահովելու համար։ Բույսերն իրենց սերմերում պարունակում են ամենաշատ սպիտակուցը, հատկապես՝ ցորենի և տարբեր հատիկաընդեղենի սերմերում։ Երիտասարդ ընձյուղները, օրինակ՝ ծնեբեկը, նույնպես հարուստ են սպիտակուցներով։
Սինթետիկ սպիտակուցներ սննդակարգում.Փոքր քանակությամբ սինթետիկ էական ամինաթթուներ կամ ամինաթթուներով հարուստ սպիտակուցներ ավելացնելով ոչ ամբողջական սպիտակուցներին, ինչպիսիք են եգիպտացորենի սպիտակուցները, վերջիններիս սննդային արժեքը կարող է զգալիորեն մեծանալ, այսինքն. դրանով իսկ մեծացնելով սպառված սպիտակուցի քանակը: Մեկ այլ հնարավորություն է բակտերիաների կամ խմորիչի աճեցումը նավթի ածխաջրածինների վրա՝ որպես ազոտի աղբյուր նիտրատների կամ ամոնիակի ավելացմամբ: Այս կերպ ստացված մանրէաբանական սպիտակուցը կարող է ծառայել որպես թռչնաբուծության կամ անասունների կեր, կամ կարող է ուղղակիորեն սպառվել մարդկանց կողմից: Երրորդ, լայնորեն կիրառվող մեթոդը օգտագործում է որոճողների ֆիզիոլոգիան: Որոճողների մոտ՝ ստամոքսի սկզբնական հատվածում, այսպես կոչված. Որովայնում բնակվում են բակտերիաների և նախակենդանիների հատուկ ձևեր, որոնք թերի բուսական սպիտակուցները վերածում են ավելի ամբողջական մանրէաբանական սպիտակուցների, իսկ դրանք, իրենց հերթին, մարսվելուց և կլանվելուց հետո վերածվում են կենդանական սպիտակուցների։ Միզանյութը՝ էժանագին սինթետիկ ազոտ պարունակող միացություն, կարող է ավելացվել անասունների կերերին։ Որովայնում ապրող միկրոօրգանիզմները օգտագործում են միզանյութի ազոտը՝ ածխաջրերը (որոնցից շատ ավելի շատ է կերերի մեջ) սպիտակուցի փոխակերպելու համար։ Անասնաբուծական կերերի ամբողջ ազոտի մոտ մեկ երրորդը կարող է հայտնվել միզանյութի տեսքով, ինչը, ըստ էության, որոշակի չափով նշանակում է սպիտակուցի քիմիական սինթեզ: ԱՄՆ-ում այս մեթոդը կարևոր դեր է խաղում որպես սպիտակուց ստանալու ուղիներից մեկը։
ԳՐԱԿԱՆՈՒԹՅՈՒՆ
Murray R., Grenner D., Mayes P., Rodwell W. Human Biochemistry, vols. 1-2. Մ., 1993 Alberts B., Bray D., Luce J. et al., vol. 1-3. Մ., 1994
Collier's Encyclopedia. - Բաց հասարակություն. 2000 .
Առնչվող հոդվածներ
-
Ասմարա Էրիթրեա.
Սուրբ Մարիամ եկեղեցի
-
12-րդ դարում հիմնադրված Ասմարան երկրի մայրաքաղաք է հռչակվել 1884 թվականին։ 1800-ականների վերջ Իտալիան սկսեց Էրիթրեայի գաղութացումը, և շուտով Ասմարան ափի հետ կապող նեղ երկաթուղի կառուցվեց, որը բարձրացրեց կարգավիճակը...
Ովքե՞ր են «խաչակիրները».
-
Թագավորին հավատարիմ ասպետների, գեղեցիկ տիկնոջ և զինվորական պարտականությունների մասին շատ դարեր շարունակ ոգեշնչել են տղամարդկանց, իսկ արվեստի մարդկանց՝ ստեղծագործելու համար (1200-1278 թթ.) Ուլրիխ ֆոն Լիխտենշտեյնը չի գրոհել Երուսաղեմը: ..
Աստվածաշնչի մեկնաբանության սկզբունքները (կարդալու 4 ոսկե կանոն)
-
Բարև, եղբայր Իվան: Ես նույն բանն ունեի սկզբում։ Բայց որքան շատ ժամանակ էի նվիրում Աստծուն՝ ծառայությանը և Նրա Խոսքին, այնքան ավելի հասկանալի էր դառնում ինձ համար: Այս մասին ես գրել եմ «Աստվածաշունչը պետք է ուսումնասիրել» գլխում իմ «Վերադառնալով...
Գործողությունը տեղի է ունենում Սուրբ Ծննդի նախօրեին։ Խորհրդական Ստալբաումի տանը բոլորը պատրաստվում են տոնին, իսկ երեխաներ Մարին ու Ֆրիցը անհամբեր սպասում են նվերների։ Նրանք զարմանում են, թե այս անգամ ինչ կտա իրենց կնքահայրը՝ ժամագործ ու կախարդ Դրոսսելմայերը։ Ի թիվս...
-
Ռուսական ուղղագրության և կետադրության կանոններ (1956)
Նոր դպրոցի կետադրական դասընթացը հիմնված է ինտոնացիոն-քերականական սկզբունքի վրա՝ ի տարբերություն դասական դպրոցի, որտեղ ինտոնացիան գործնականում չի ուսումնասիրվում։ Թեև նոր տեխնիկան օգտագործում է կանոնների դասական ձևակերպումներ, նրանք ստանում են...
-
Կոժեմյակիններ՝ հայր և որդի Կոժեմյակինս՝ հայր և որդի
| Կադետների ստեղծագործականությունը Նրանք մահվան երեսին նայեցին | Ռուսաստանի Դաշնության հերոս Սուվորովի կուրսանտ Դմիտրի Սերգեևիչ Կոժեմյակինը (1977-2000) Ահա թե ինչպես նա մնաց դեսանտայինների սրտերում: ես...
