O toplotni energiji v preprostem jeziku! Koliko toplote je potrebno za m gramov. Koliko toplote je potrebno za m gramov
730. Zakaj se voda uporablja za hlajenje nekaterih mehanizmov?
Voda ima odlično specifično toplotno kapaciteto, ki spodbuja dobro odvajanje toplote iz mehanizma.
731. V katerem primeru je treba porabiti več energije: segreti en liter vode za 1 °C ali segreti sto gramov vode za 1 °C?
Za segrevanje litra vode, večja kot je masa, več energije je treba porabiti.
732. Bakronikljevo srebro in srebrne vilice enake mase smo spustili v vročo vodo. Ali bodo od vode prejeli enako količino toplote?
Vilice iz bakroniklja bodo prejele več toplote, ker je specifična toplota bakroniklja večja kot pri srebru.
733. Kos svinca in kos litega železa enake mase smo trikrat udarili s kladivom. Kateri kos je postal bolj vroč?
Svinec se bolj segreje, ker je njegova specifična toplotna kapaciteta nižja od litega železa in za segrevanje svinca potrebuje manj energije.
734. V eni bučki je voda, v drugi pa kerozin enake mase in temperature. V vsako bučko smo spustili enako segreto železovo kocko. Kaj se bo bolj segrelo visoka temperatura– voda ali kerozin?
kerozin.
735. Zakaj so temperaturna nihanja pozimi in poleti v mestih na morski obali manjša kot v mestih v notranjosti?
Voda se segreva in ohlaja počasneje kot zrak. Pozimi ohlaja in premika tople zračne mase na kopno, zaradi česar je podnebje na obali toplejše.
736. Specifična toplotna kapaciteta aluminija je 920 J/kg °C. Kaj to pomeni?
To pomeni, da je za segrevanje 1 kg aluminija za 1 °C potrebno porabiti 920 J.
737. Aluminijeve in bakrene palice enake mase 1 kg ohladimo za 1 °C. Koliko se bo spremenila notranja energija vsakega bloka? Za katero vrstico se bo spremenila več in za koliko?
738. Koliko toplote je potrebno za segrevanje kilograma železne gredice za 45 °C?

739. Koliko toplote je potrebno za segrevanje 0,25 kg vode s 30 °C na 50 °C?

740. Kako se bo spremenila notranja energija dveh litrov vode, če se segrejeta za 5 °C?

741. Koliko toplote potrebujemo, da segrejemo 5 g vode z 20 °C na 30 °C?

742. Koliko toplote je potrebno za segrevanje aluminijaste krogle z maso 0,03 kg za 72 °C?
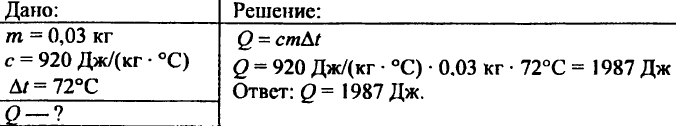
743. Izračunaj količino toplote, ki je potrebna za segrevanje 15 kg bakra na 80 °C.

744. Izračunaj količino toplote, ki je potrebna za segrevanje 5 kg bakra od 10 °C do 200 °C.

745. Koliko toplote je potrebno za segrevanje 0,2 kg vode s 15 °C na 20 °C?

746. Voda z maso 0,3 kg se je ohladila za 20 °C. Za koliko se je zmanjšala notranja energija vode?

747. Koliko toplote potrebujemo, da segrejemo 0,4 kg vode s temperaturo 20 °C na temperaturo 30 °C?

748. Koliko toplote se porabi za segrevanje 2,5 kg vode za 20 °C?
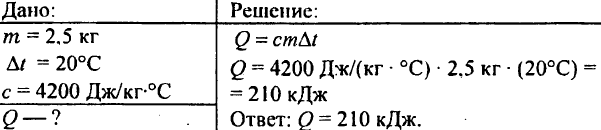
749. Kolikšna količina toplote se je sprostila, ko se je 250 g vode ohladilo z 90 °C na 40 °C?
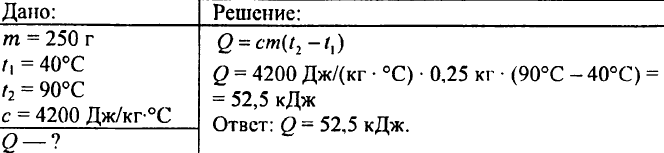
750. Koliko toplote je potrebno za segrevanje 0,015 litra vode za 1 °C?

751. Izračunajte količino toplote, potrebno za ogrevanje ribnika s prostornino 300 m3 za 10 °C?
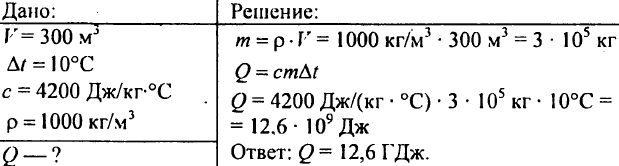
752. Koliko toplote je treba dodati 1 kg vode, da se njena temperatura zviša s 30 °C na 40 °C?
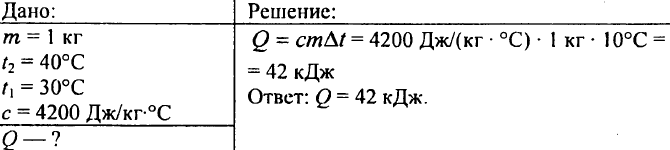
753. Voda s prostornino 10 litrov se je s temperature 100 °C ohladila na temperaturo 40 °C. Koliko toplote se je pri tem sprostilo?

754. Izračunaj količino toplote, potrebno za segrevanje 1 m3 peska za 60 °C.

755. Prostornina zraka 60 m3, specifična toplotna kapaciteta 1000 J/kg °C, gostota zraka 1,29 kg/m3. Koliko toplote je potrebno, da se temperatura dvigne na 22 °C?

756. Vodo smo segreli za 10 °C, pri čemer smo porabili 4,20 103 J toplote. Določite količino vode.

757. Vodi z maso 0,5 kg smo predali 20,95 kJ toplote. Kakšna je bila temperatura vode, če je bila začetna temperatura vode 20 °C?

758. Bakreno posodo, ki tehta 2,5 kg, napolnimo z 8 kg vode pri 10 °C. Koliko toplote je potrebno, da se voda v kozici segreje do vrenja?

759. V bakren lonec z maso 300 g nalijemo liter vode s temperaturo 15 °C.

760. Kos segretega granita, ki tehta 3 kg, damo v vodo. Granit preda 12,6 kJ toplote vodi, ki se ohladi za 10 °C. Kakšna je specifična toplotna kapaciteta kamna?
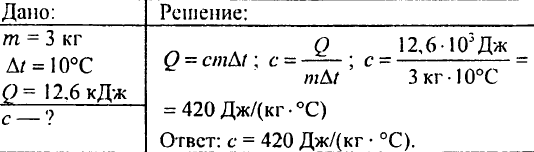
761. 5 kg vode pri 12 °C smo dodali vročo vodo pri 50 °C in dobili zmes s temperaturo 30 °C. Koliko vode ste dodali?

762. Vodo pri 20 °C smo dodali 3 litrom vode pri 60 °C in dobili vodo pri 40 °C. Koliko vode ste dodali?

763. Kakšna bo temperatura zmesi, če zmešaš 600 g vode pri 80 °C z 200 g vode pri 20 °C?

764. Liter vode pri 90 °C smo vlili v vodo pri 10 °C in temperatura vode je postala 60 °C. Koliko hladne vode je bilo tam?

765. Določite, koliko vlijete v posodo topla voda, segreto na 60 °C, če je v posodi že 20 litrov hladne vode s temperaturo 15 °C; temperatura mešanice naj bo 40 °C.

766. Ugotovi, koliko toplote je potrebno za segrevanje 425 g vode za 20 °C.

767. Za koliko stopinj se segreje 5 kg vode, če voda prejme 167,2 kJ?

768. Koliko toplote je potrebno za segrevanje m gramov vode pri temperaturi t1 na temperaturo t2?
769. V kalorimeter vlijemo 2 kg vode s temperaturo 15 °C. Na kakšno temperaturo se segreje voda v kalorimetru, če vanjo spustimo 500 g medeninasto utež, segreto na 100 °C? Specifična toplotna kapaciteta medenine je 0,37 kJ/(kg °C).
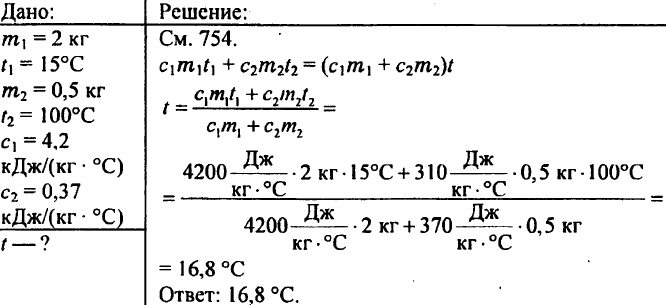
770. Obstajajo kosi bakra, kositra in aluminija enake prostornine. Kateri od teh kosov ima največjo in kateri najmanjšo toplotno kapaciteto?

771. V kalorimeter smo vlili 450 g vode, katere temperatura je bila 20 °C. Ko smo v to vodo potopili 200 g železnih opilkov, segretih na 100 °C, je temperatura vode postala 24 °C. Določite specifično toplotno kapaciteto žagovine.

772. V bakrenem kalorimetru, ki tehta 100 g, je 738 g vode, katere temperatura je 15 °C. V ta kalorimeter smo spustili 200 g bakra pri temperaturi 100 °C, nato pa se je temperatura kalorimetra dvignila na 17 °C. Kakšna je specifična toplotna kapaciteta bakra?

773. Jekleno kroglico z maso 10 g vzamemo iz peči in jo damo v vodo s temperaturo 10 °C. Temperatura vode se je dvignila na 25 °C. Kolikšna je bila temperatura krogle v peči, če je bila masa vode 50 g? Specifična toplotna kapaciteta jekla je 0,5 kJ/(kg °C).
776. Vodi z maso 0,95 g pri temperaturi 80 °C smo zmešali vodo z maso 0,15 g pri temperaturi 15 °C. Določite temperaturo mešanice. 779. Jekleno rezilo, ki tehta 2 kg, smo segreli na temperaturo 800 °C in ga nato spustili v posodo s 15 litri vode s temperaturo 10 °C. Do katere temperature se bo segrela voda v posodi?

(Navedba: Za rešitev tega problema je potrebno sestaviti enačbo, v kateri je neznana temperatura vode v posodi po spuščanju rezalnika vzeta kot neznanka.)
780. Kakšno temperaturo bo voda dobila, če zmešaš 0,02 kg vode pri 15 °C, 0,03 kg vode pri 25 °C in 0,01 kg vode pri 60 °C?
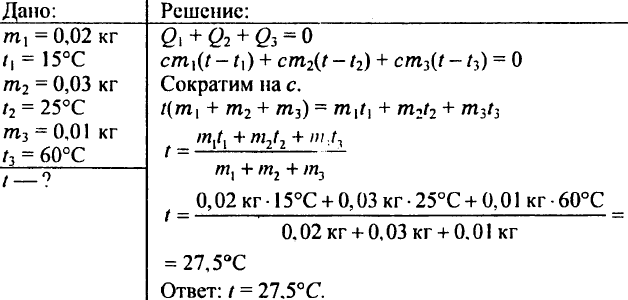
781. Za ogrevanje dobro prezračenega razreda je potrebna količina toplote 4,19 MJ na uro. Voda v radiatorje vstopa pri 80 °C, iz njih pa pri 72 °C. Koliko vode je treba vsako uro dovajati v radiatorje?

782. Svinec z maso 0,1 kg pri temperaturi 100 °C smo potopili v aluminijast kalorimeter z maso 0,04 kg, v katerem je bilo 0,24 kg vode pri temperaturi 15 °C. Nato je temperatura v kalorimetru dosegla 16 °C. Kakšna je specifična toplota svinca?

“...- Kolikor papig lahko spraviš vate, takšna je tvoja višina.
- Zelo je potrebno! Ne bom pogoltnil toliko papagajev!...«
Iz filma "38 papagajev"
Po mednarodnih pravilih SI (International System of Units) se količina toplotne energije ali količina toplote meri v Joulih [J], obstajajo pa tudi več enot kiloJoule [kJ] = 1000 J., MegaJoule [MJ] = 1.000.000 J, GigaJoule [ GJ] = 1.000.000.000 J itd. Ta merska enota toplotne energije je glavna mednarodna enota in se največkrat uporablja v znanstvenih in znanstveno-tehničnih izračunih.
Vsi pa vemo ali smo že vsaj enkrat slišali še eno mersko enoto za količino toplote (ali preprosto toploto) kalorija, pa tudi kilokalorija, megakalorija in gigakalorija, kar pomenijo predpone kilo, giga in mega. pomeni, glejte zgornji primer z Jouli. V naši državi je zgodovinsko gledano pri izračunu tarif za ogrevanje, pa naj gre za ogrevanje na elektriko, plin ali kotle na pelete, običajno upoštevati strošek točno ene gigakalorije toplotne energije.
Kaj je torej gigakalorija, kilovat, kilovatna*ura ali kilovatna uro in jouli in kako so med seboj povezani?, boste izvedeli v tem članku.
Torej, osnovna enota toplotne energije je, kot že omenjeno, Joule. Toda preden govorimo o merskih enotah, je načeloma treba na vsakdanji ravni razložiti, kaj je toplotna energija ter kako in zakaj jo meriti.
Vsi vemo že od otroštva, da bi se ogreli (dobili toplotna energija) morate nekaj zažgati, zato smo vsi kurili ogenj, tradicionalno gorivo za ogenj je les. Tako se očitno pri zgorevanju goriva (katerega koli: les, premog, peleti, zemeljski plin, dizelsko gorivo) sprošča toplotna energija (toplota). Toda za ogrevanje na primer različnih količin vode potrebujemo različne količine drv (ali drugega goriva). Jasno je, da je za segrevanje dveh litrov vode dovolj nekaj požarov, za pripravo pol vedra juhe za celoten tabor pa se morate založiti z več svežnji drv. Da tako strogih tehničnih veličin, kot sta količina toplote in zgorevalna toplota goriva, ne bi merili s snopi drv in vedri juhe, so se ogrevalci odločili za jasnost in red ter se dogovorili, da bodo izumili enoto za količino toplote. Da bi bila ta enota povsod enaka, je bilo definirano takole: en kilogram vode pri normalnih pogojih segreti za eno stopinjo ( atmosferski tlak) zahteva 4.190 kalorij ali 4,19 kilokalorij, zato bo za segrevanje enega grama vode dovolj tisočkrat manj toplote - 4,19 kalorij.
Kalorija je povezana z mednarodno enoto toplotne energije, joulom, z naslednjim razmerjem:
1 kalorija = 4,19 joulov.
Tako bo segrevanje 1 grama vode za eno stopinjo zahtevalo 4,19 joulov toplotne energije, segrevanje enega kilograma vode pa 4190 joulov toplote.
V tehnologiji poleg merske enote toplotne (in katere koli druge) energije obstaja enota moči in v skladu z mednarodni sistem(SI) je Watt. Pojem moči velja tudi za grelne naprave. Če je grelna naprava sposobna oddati 1 Joule toplotne energije v 1 sekundi, potem je njena moč 1 Watt. Moč je sposobnost naprave, da proizvede (ustvari) določeno količino energije (v našem primeru toplotne energije) na časovno enoto. Vrnimo se k našemu primeru z vodo, da segrejemo en kilogram (ali en liter, v primeru vode je kilogram enak litru) vode za eno stopinjo Celzija (ali Kelvina, ni razlike), potrebujemo moč 1 kilokalorije ali 4.190 J toplotne energije. Da segrejemo en kilogram vode v 1 sekundi časa za 1 stopinjo, potrebujemo napravo z naslednjo močjo:
4190 J./1 s. = 4.190 W. ali 4,19 kW.
Če želimo naš kilogram vode v isti sekundi segreti za 25 stopinj, potem bomo potrebovali petindvajsetkrat večjo moč, tj.
4,19*25 =104,75 kW.
Tako lahko sklepamo, da ima kotel na pelete moč 104,75 kW. v eni sekundi segreje 1 liter vode za 25 stopinj.
Ko smo prišli do vatov in kilovatov, bi morali reči nekaj besed o njih. Kot že omenjeno, je Watt enota za moč, kamor sodi tudi toplotna moč kotla, a poleg kotlov na pelete in plinskih kotlov človeštvo pozna tudi električne kotle, katerih moč se meri seveda v isti kilovatov in ne porabljajo niti peletov niti plina ter elektrike, katere količina se meri v kilovatnih urah. Pravilno črkovanje energijske enote kilovat*ura (in sicer kilovat pomnožen z uro, ne deljeno), pisanje kW/uro je napaka!
V električnih kotlih električna energija se pretvori v toploto (t. i. Joulova toplota) in če je kotel porabil 1 kW*uro električne energije, koliko toplote je potem proizvedel? Če želite odgovoriti na to preprosto vprašanje, morate narediti preprost izračun.
Pretvorimo kilovate v kilodžule/sekundo (kilodžul na sekundo) in ure v sekunde: v eni uri je 3600 sekund, dobimo:
1 kW*ura = [1 kJ/s]*3600 s.=1.000 J *3600 s = 3.600.000 Joulov ali 3,6 MJ.
Torej,
1 kW*ura = 3,6 MJ.
Po drugi strani pa je 3,6 MJ/4,19 = 0,859 Mcal = 859 kcal = 859.000 cal. Energija (toplotna).
Zdaj pa preidimo na Gigakalorije, katerih cena je različne vrste Ogrevalci radi preštevajo goriva.
1 Gcal = 1.000.000.000 kal.
1.000.000.000 kal. = 4,19*1.000.000.000 = 4.190.000.000 J. = 4.190 MJ. = 4,19 GJ.
Ali če vemo, da je 1 kW*ura = 3,6 MJ, preračunajmo 1 Gigakalorije na kilovatno uro:
1 Gcal = 4190 MJ/3,6 MJ = 1.163 kW*ure!
Če se po branju tega članka odločite, da se posvetujete s strokovnjakom našega podjetja o katerem koli vprašanju v zvezi z oskrbo s toploto, potem Tukaj!
Vir: teplo-en.ru
(ali prenos toplote).
Specifična toplotna kapaciteta snovi.
Toplotna zmogljivost- to je količina toplote, ki jo telo absorbira pri segrevanju za 1 stopinjo.
Toplotno kapaciteto telesa označuje velika črka latinska črka Z.
Od česa je odvisna toplotna kapaciteta telesa? Najprej od njegove mase. Jasno je, da bo segrevanje na primer 1 kilograma vode zahtevalo več toplote kot segrevanje 200 gramov.
Kaj pa vrsta snovi? Naredimo poskus. Vzemimo dve enaki posodi in tako, da v eno od njih nalijemo vodo, ki tehta 400 g, v drugo pa rastlinsko olje, ki tehta 400 g, ju začnemo segrevati z enakimi gorilniki. Z opazovanjem odčitkov termometra bomo videli, da se olje hitro segreje. Da se voda in olje segrejeta na enako temperaturo, je treba vodo segrevati dlje. A dlje ko segrevamo vodo, več toplote prejme od gorilnika.
Tako segrevanje iste mase različnih snovi na isto temperaturo zahteva različne količine toplote. Količina toplote, ki je potrebna za ogrevanje telesa, in s tem njegova toplotna kapaciteta sta odvisni od vrste snovi, iz katere je telo sestavljeno.
Tako je na primer za povečanje temperature vode, ki tehta 1 kg, za 1 °C potrebna količina toplote, ki je enaka 4200 J, in za segrevanje enake mase sončničnega olja za 1 °C, količina toplote, ki je enaka Zahteva se 1700 J.
Fizikalna količina, ki kaže, koliko toplote je potrebno za segrevanje 1 kg snovi za 1 ºС, se imenuje specifično toplotno kapaciteto te snovi.
Vsaka snov ima svojo specifično toplotno kapaciteto, ki jo označujemo z latinsko črko c in merimo v joulih na kilogram stopinje (J/(kg °C)).
Specifična toplotna kapaciteta iste snovi v različnih agregatnih stanjih (trdno, tekoče in plinasto) je različna. Na primer, specifična toplotna kapaciteta vode je 4200 J/(kg °C), specifična toplotna kapaciteta ledu pa 2100 J/(kg °C); aluminij v trdnem stanju ima specifično toplotno kapaciteto 920 J/(kg - °C), v tekočem stanju pa 1080 J/(kg - °C).
Upoštevajte, da ima voda zelo visoko specifično toplotno kapaciteto. Zato voda v morjih in oceanih, ki se poleti segreje, absorbira iz zraka veliko število toplota. Zahvaljujoč temu v tistih krajih, ki se nahajajo v bližini velikih vodnih teles, poletje ni tako vroče kot v krajih, ki so daleč od vode.
Izračun količine toplote, ki je potrebna za ogrevanje telesa ali ki jo telo sprosti pri ohlajanju.
Iz navedenega je razvidno, da je količina toplote, ki je potrebna za segrevanje telesa, odvisna od vrste snovi, iz katere je telo sestavljeno (to je njena specifična toplotna kapaciteta) in od mase telesa. Jasno je tudi, da je količina toplote odvisna od tega, za koliko stopinj bomo povišali telesno temperaturo.
Če želite torej določiti količino toplote, ki je potrebna za ogrevanje telesa ali ki jo telo sprosti med ohlajanjem, morate specifično toplotno kapaciteto telesa pomnožiti z njegovo maso in z razliko med njegovo končno in začetno temperaturo:
Q = cm (t 2 - t 1 ) ,
kje Q- količino toplote, c— specifično toplotno kapaciteto, m- telesna teža, t 1 — začetna temperatura, t 2 — končna temperatura.
Ko se telo segreje t 2 > t 1 in zato Q > 0 . Ko se telo ohladi t 2i< t 1 in zato Q< 0 .
Če je znana toplotna kapaciteta celotnega telesa Z, Q določeno s formulo:
Q = C (t 2 - t 1 ) .
Človeštvo pozna nekaj vrst energije - mehanska energija(kinetična in potencialna), notranja energija (toplotna), energija polja (gravitacijska, elektromagnetna in jedrska), kemična. Izpostaviti velja energijo poka...
Energija vakuuma in temna energija, ki še vedno obstaja le v teoriji. V tem članku, prvem v razdelku o toplotni tehniki, bom poskusil v preprostem in dostopnem jeziku z uporabo praktični primer, govori o najpomembnejši vrsti energije v življenju ljudi - o toplotna energija in o tem, da bi jo pravočasno rodila toplotna moč.
Nekaj besed za razumevanje mesta toplotne tehnike kot veje znanosti o pridobivanju, prenosu in uporabi toplotne energije. Sodobna toplotna tehnika je nastala iz splošne termodinamike, ki je ena od vej fizike. Termodinamika je dobesedno "toplo" plus "moč". Tako je termodinamika veda o "spremembi temperature" sistema.
Zunanji vpliv na sistem, ki spremeni njegovo notranjo energijo, je lahko posledica izmenjave toplote. Toplotna energija, ki ga sistem pridobi ali izgubi kot rezultat takšne interakcije z okoljem, imenujemo količino toplote in se meri v enotah SI v Joulih.
Če niste ogrevalni inženir in se s toplotnotehničnimi vprašanji ne ukvarjate vsakodnevno, potem ko se z njimi srečate, jih je včasih brez izkušenj zelo težko hitro razumeti. Brez izkušenj si je težko celo predstavljati dimenzije zahtevanih vrednosti količine toplote in toplotne moči. Koliko joulov energije je potrebnih za segrevanje 1000 kubičnih metrov zraka s temperature -37˚С na +18˚С?.. Kakšno moč toplotnega vira potrebujemo, da to storimo v 1 uri?.. Danes lahko na ta ne najtežja vprašanja odgovorite »takoj« »Ni vsakdo inženir. Včasih se strokovnjaki celo spomnijo formul, a le redki jih znajo uporabiti v praksi!
Ko boste ta članek prebrali do konca, boste zlahka rešili resnične industrijske in vsakdanje probleme, povezane z ogrevanjem in hlajenjem različnih materialov. Razumevanje fizikalnega bistva procesov prenosa toplote in poznavanje preprostih osnovnih formul so glavni bloki v temelju znanja v toplotni tehniki!
Količina toplote med različnimi fizikalnimi procesi.
Večina znanih snovi je lahko v trdnem, tekočem, plinastem ali plazemskem stanju pri različnih temperaturah in tlakih. Prehod iz enega agregatnega stanja v drugo poteka pri konstantni temperaturi(pod pogojem, da se tlak in drugi parametri ne spremenijo okolju) in ga spremlja absorpcija ali sproščanje toplotne energije. Kljub dejstvu, da je 99 % snovi v vesolju v stanju plazme, tega agregatnega stanja v tem članku ne bomo obravnavali.
Razmislite o grafu, predstavljenem na sliki. Prikazuje temperaturno odvisnost snovi T na količino toplote Q, pripeljal do določenega zaprt sistem ki vsebuje določeno maso določene snovi.

1. Trdna snov, ki ima temperaturo T1, segrejte na temperaturo Tmelt, ki za ta proces porabi količino toplote, ki je enaka Q1 .
2. Nato se začne proces taljenja, ki poteka pri konstantni temperaturi Tpl(temperatura taljenja). Za taljenje celotne mase trdne snovi je potrebno porabiti toplotno energijo v količini Q2 - Q1 .
3. Nato se tekočina, ki nastane pri taljenju trdne snovi, segreje do vrelišča (tvorba plina) Tkp, poraba za to količino toplote enaka Q3-Q2 .
4. Sedaj na stalnem vrelišču Tkp tekočina zavre in izhlapi ter se spremeni v plin. Za pretvorbo celotne mase tekočine v plin je potrebno porabiti toplotno energijo v količini Q4-Q3.
5. Na zadnji stopnji se plin segreje s temperature Tkp do določene temperature T2. V tem primeru bo količina porabljene toplote V5-Q4. (Če plin segrejemo na temperaturo ionizacije, se bo plin spremenil v plazmo.)
Tako ogrevanje originala trdna na temperaturo T1 do temperature T2 smo porabili toplotno energijo v višini V5, prenos snovi skozi tri agregatna stanja.
Če se premikamo v nasprotni smeri, bomo snovi odvzeli enako količino toplote V5, ki je šel skozi stopnje kondenzacije, kristalizacije in ohlajanja od temperature T2 do temperature T1. Seveda razmišljamo o zaprtem sistemu brez izgub energije v zunanje okolje.
Upoštevajte, da je možen prehod iz trdnega stanja v plinasto stanje, mimo tekoče faze. Ta proces se imenuje sublimacija, obratni proces pa desublimacija.
Tako smo ugotovili, da je za procese prehodov med agregatnimi stanji snovi značilna poraba energije pri stalni temperaturi. Pri segrevanju snovi, ki se nahaja v eni konstanti agregatno stanje, se temperatura dvigne in porablja se tudi toplotna energija.
Glavne formule za prenos toplote.
Formule so zelo preproste.
Količina toplote Q v J se izračuna po formulah:
1. S strani porabe toplote, to je s strani obremenitve:
1.1. Pri ogrevanju (hlajenju):
Q = m * c *(T2 -T1)
m – masa snovi v kg
z - specifična toplotna kapaciteta snovi v J/(kg*K)
1.2. Pri taljenju (zamrzovanju):
Q = m * λ
λ – specifična toplota taljenja in kristalizacije snovi v J/kg
1.3. Med vrenjem izhlapevanje (kondenzacija):
Q = m * r
r – specifična toplota nastajanja plinov in kondenzacije snovi v J/kg
2. S strani proizvodnje toplote, torej s strani vira:
2.1. Ko gorivo gori:
Q = m * q
q – specifična toplota zgorevanja goriva v J/kg
2.2. Pri pretvorbi električne energije v toplotno energijo (Joule-Lenzov zakon):
Q =t *I *U =t *R *I ^2=(t /R)*U^2
t – čas v s
jaz – efektivna trenutna vrednost v A
U – efektivna vrednost napetosti v V
R – Upornost obremenitve v ohmih
Sklepamo, da je količina toplote pri vseh faznih pretvorbah in med segrevanjem premo sorazmerna z maso snovi, poleg tega pa premo sorazmerna tudi temperaturni razliki. Koeficienti sorazmernosti ( c , λ , r , q ) za vsako snov imajo svoje pomene in so določeni empirično (povzeto iz referenčnih knjig).
Toplotna moč n v W je količina toplote, prenesena v sistem v določenem času:
N=Q/t
Čim hitreje želimo telo segreti na določeno temperaturo, tem večja moč naj bo vir toplotne energije – vse je logično.
Izračun aplikativnega problema v Excelu.
V življenju je pogosto treba narediti hiter ocenjevalni izračun, da bi razumeli, ali je smiselno nadaljevati študij teme, narediti projekt in podrobne, natančne, zamudne izračune. Če v nekaj minutah naredite izračun tudi z natančnostjo ±30%, lahko sprejmete pomembno upravljavsko odločitev, ki bo 100-krat cenejša in 1000-krat učinkovitejša ter navsezadnje 100.000-krat učinkovitejša od izvedbe natančnega izračuna v enem tednu, sicer in mesece, s strani skupine dragih specialistov...
Problemski pogoji:
Iz skladišča na ulici pripeljemo 3 tone valjane kovine v prostore delavnice za pripravo valjane kovine dimenzij 24m x 15m x 7m. Na kovinskih voznih parkih je poledica skupna masa 20 kg. Zunaj je -37˚С. Koliko toplote je potrebno za segrevanje kovine na +18˚С; segrejte led, ga stopite in segrejte vodo na +18˚С; ogreti celotno količino zraka v prostoru, ob predpostavki, da je bilo ogrevanje pred tem popolnoma izklopljeno? Kakšno moč naj ima ogrevalni sistem, če mora biti vse našteto opravljeno v 1 uri? (Zelo težki in skoraj nerealni pogoji - predvsem glede zraka!)
Izračun bomo opravili v programuMS Excel ali v programuOOo Izračun.
Preverite barvno oblikovanje celic in pisave na strani »«.
Začetni podatki:
1. Zapišemo imena snovi:
v celico D3: Jeklo
v celico E3: Led
v celico F3: Led/voda
v celico G3: voda
v celico G3: zrak
2. Vnesemo imena procesov:
v celice D4, E4, G4, G4: toplota
v celico F4: taljenje
3. Specifična toplotna kapaciteta snovi c v J/(kg*K) pišemo za jeklo, led, vodo in zrak
v celico D5: 460
v celico E5: 2110
v celico G5: 4190
v celico H5: 1005
4. Specifična toplota taljenje ledu λ vnesite v J/kg
v celico F6: 330000
5. Veliko snovi m Vnesemo v kg za jeklo in led
v celico D7: 3000
v celico E7: 20
Ker se masa ne spremeni, ko se led spremeni v vodo, potem
v celicah F7 in G7: =E7 =20
Maso zraka dobimo tako, da prostornino prostora pomnožimo s specifično težo
v celici H7: =24*15*7*1,23 =3100
6. Čas postopka t na minuto pišemo le enkrat za jeklo
v celico D8: 60
Časovne vrednosti za segrevanje ledu, njegovo taljenje in segrevanje nastale vode se izračunajo iz pogoja, da morajo biti vsi ti trije procesi končani v enakem času, kot je predvideno za segrevanje kovine. Preberite ustrezno
v celici E8: =E12/(($E$12+$F$12+$G$12)/D8) =9,7
v celici F8: =F12/(($E$12+$F$12+$G$12)/D8) =41,0
v celici G8: =G12/(($E$12+$F$12+$G$12)/D8) =9,4
V istem predvidenem času naj se ogreje tudi zrak, beremo
v celici H8: =D8 =60,0
7. Začetna temperatura vseh snovi T1 Postavimo ga na ˚C
v celico D9: -37
v celico E9: -37
v celico F9: 0
v celico G9: 0
v celico H9: -37
8. Končna temperatura vseh snovi T2 Postavimo ga na ˚C
v celico D10: 18
v celico E10: 0
v celico F10: 0
v celico G10: 18
v celico H10: 18
Mislim, da glede členov 7 in 8 ne bi smelo biti vprašanj.

Rezultati izračuna:
9. Količina toplote Q v KJ, potrebnih za vsakega od procesov, izračunamo
za ogrevanje jekla v celici D12: =D7*D5*(D10-D9)/1000 =75900
za segrevanje ledu v celici E12: =E7*E5*(E10-E9)/1000 = 1561
za taljenje ledu v celici F12: =F7*F6/1000 = 6600
za ogrevanje vode v celici G12: =G7*G5*(G10-G9)/1000 = 1508
za ogrevanje zraka v celici H12: =H7*H5*(H10-H9)/1000 = 171330
Odčitamo skupno količino toplotne energije, ki je potrebna za vse procese
v združeni celici D13E13F13G13H13: =SUM(D12:H12) = 256900
V celicah D14, E14, F14, G14, H14 in združeni celici D15E15F15G15H15 je količina toplote podana v merski enoti lok - v Gcal (v gigakalorijah).
10. Toplotna moč n v kW, potrebnih za vsak proces
za ogrevanje jekla v celici D16: =D12/(D8*60) =21,083
za segrevanje ledu v celici E16: =E12/(E8*60) = 2,686
za taljenje ledu v celici F16: =F12/(F8*60) = 2,686
za ogrevanje vode v celici G16: =G12/(G8*60) = 2,686
za ogrevanje zraka v celici H16: =H12/(H8*60) = 47,592
Skupna toplotna moč, potrebna za pravočasno dokončanje vseh procesov t izračunano
v združeni celici D17E17F17G17H17: =D13/(D8*60) = 71,361
V celicah D18, E18, F18, G18, H18 in združeni celici D19E19F19G19H19 je toplotna moč podana v merski enoti lok - v Gcal/uro.
S tem je izračun v Excelu zaključen.
Sklepi:
Upoštevajte, da segrevanje zraka zahteva več kot dvakrat več energije kot segrevanje enake mase jekla.
Ogrevanje vode stane dvakrat več energije kot ogrevanje ledu. Postopek taljenja porabi velikokrat več energije kot postopek segrevanja (pri majhni temperaturni razliki).
Ogrevanje vode zahteva desetkrat več toplotne energije kot ogrevanje jekla in štirikrat več kot ogrevanje zraka.
Za prejemanje informacije o izdaji novih člankov in za prenos delovnih programskih datotek Prosim vas, da se naročite na obvestila v oknu na koncu članka ali v oknu na vrhu strani.
Po vnosu vašega naslova e-pošta in kliknite na gumb "Prejemanje obvestil o člankih". NE POZABITEPOTRDI NAROČNIŠTVO s klikom na povezavo v pismu, ki vam bo takoj prispelo na navedeni e-poštni naslov (včasih v mapi « Neželena pošta » )!
Spomnili smo se pojmov »količina toplote« in »toplotna moč«, preučili temeljne formule za prenos toplote in analizirali praktični primer. Upam, da je bil moj jezik preprost, jasen in zanimiv.
Čakam na vprašanja in komentarje na članek!
prosim SPOŠTOVANJE datoteka za prenos avtorskega dela PO NAROČNICI za objave člankov.
Po definiciji je kalorija količina toplote, ki je potrebna za ogrevanje kubični centimeter vode za 1 stopinjo Celzija. Gigakalorija, ki se uporablja za merjenje toplotne energije v termoenergetiki in komunali, je milijarda kalorij. V 1 metru je 100 centimetrov, torej v enem kubični meter– 100 x 100 x 100 = 1000000 centimetrov. Tako za segrevanje kocke vode z
1 stopinja bo potrebnih milijon kalorij ali 0,001 Gcal.
V mojem mestu je cena ogrevanja 1132,22 rubljev / Gcal, cena tople vode pa 71,65 rubljev / kubični meter, cena hladne vode pa 16,77 rubljev / kubični meter.
Koliko Gcal se porabi za ogrevanje 1 kubičnega metra vode?
Mislim, da
s x 1132,22 = 71,65 - 16,77 in tako rešite enačbe, da ugotovite, čemu je enako s (Gcal), to je enako 0,0484711452 Gcal
Nekaj dvomim, po mojem mnenju se narobe odločam
ODGOVOR:
V vašem izračunu ne najdem nobenih napak.
Seveda zgornje tarife ne bi smele vključevati stroškov odpadne vode (odplake).
Približen izračun za mesto Iževsk po starih standardih izgleda takole:
0,19 Gcal na osebo na mesec (ta norma je zdaj odpravljena, vendar ni druge, primerna je na primer) / 3,6 kubičnih metrov. na osebo na mesec (poraba tople vode) = 0,05278 Gcal na 1 kubični meter. (toliko toplote je potrebno za segrevanje 1 kubičnega metra hladne vode na standardno temperaturo tople vode, ki je, naj vas spomnim, 60 stopinj C).
Za natančnejši izračun količine toplotne energije za ogrevanje vode z uporabo neposredne metode na podlagi fizikalne količine(in ne drugače na podlagi odobrenih tarif za oskrbo s toplo vodo) - priporočam uporabo predloga za izračun tarife za toplo vodo (REK UR). Formula za izračun med drugim uporablja temperaturo hladne vode v poletnem in zimskem (ogrevalnem) obdobju ter trajanje teh obdobij.
Oznake: gigakalorija, vroča voda
- Storitve tople vode plačujemo, temperatura je bistveno nižja od standardne. Kaj narediti?
- Trajanje odklopa oskrbe s toplo vodo, določeno s pravilnikom, ni nezakonito - odločba Vrhovnega sodišča Ruske federacije (2017)
- Pobuda za vzpostavitev pravičnejše tarife in načina merjenja porabe tople vode
- O postopku za ponovni izračun zneska plačila za ogrevanje in toplo vodo med izpadi - pojasnilo Rospotrebnadzorja za SD
- O obračunavanju hladilne tekočine v zaprtem sistemu oskrbe s toploto - pismo Ministrstva za gradbeništvo Ruske federacije z dne 31. marca 2015 št. 9116-OD/04
- UR - O znižanju nadomestil za ogrevanje in toplo vodo - dopis Ministrstva za energijo UR z dne 17.08.2015 št. 11-10/5661
- Kakšen je standardni rok za overitev skupnega hišnega števca za ogrevanje in sanitarno vodo?
- Umazana vroča voda iz pipe. Kam se obrniti?
- Ali se lahko vodomer v stanovanju poveča za celoten vhod? Kako plačati? Mesečni odčitki - 42 kubičnih metrov
- Postopek vodenja ločenega računovodstva stroškov na področju oskrbe z vodo in sanitarij - ukaz Ministrstva za gradbeništvo Ruske federacije z dne 25. januarja 2014 št. 22/pr.
- plačilo vode in elektrike v stanovanju brez nastanitve
- toplotni obračun po ODPU do 1/12
- Oskrba z električno energijo
- Ogromna plačila za sobo v študentskem domu (17,3 m2)
| Komentarji: (11) | |
| Namig: delite povezavo na družbenih omrežjih, če želite dobiti več odgovorov/komentarjev! | |
Sorodni članki
-
Vojaška naselja Puškin okoli Arakcheeva
Aleksej Andrejevič Arakčejev (1769-1834) - ruski državnik in vojskovodja, grof (1799), artilerijski general (1807). Izhajal je iz plemiške družine Arakčejevih. Uveljavil se je pod Pavlom I. in prispeval k njegovi vojaški ...
-
Preprosti fizikalni poskusi doma
Lahko se uporablja pri pouku fizike na stopnjah postavljanja ciljev in ciljev lekcije, ustvarjanja problemskih situacij pri preučevanju nove teme, uporabe novega znanja pri utrjevanju. Predstavitev Zabavni poskusi lahko učenci uporabljajo za...
-
Dinamična sinteza odmičnih mehanizmov Primer sinusnega zakona gibanja odmičnih mehanizmov
Odmični mehanizem je mehanizem z višjim kinematičnim parom, ki ima možnost zagotoviti obstojnost izhodnega člena, struktura pa vsebuje vsaj en člen z delovno površino spremenljive ukrivljenosti. Cam mehanizmi ...
-
Vojna se še ni začela Vse Podkast oddaje Glagolev FM
Predstava Semjona Aleksandrovskega po drami Mihaila Durnenkova "Vojna se še ni začela" je bila uprizorjena v gledališču Praktika. Poroča Alla Shenderova. V zadnjih dveh tednih je to že druga moskovska premiera po besedilu Mihaila Durnenkova....
-
Predstavitev na temo "metodološka soba v dhowu"
| Dekoracija pisarn v predšolski vzgojni ustanovi Zagovor projekta "Novoletna dekoracija pisarne" za mednarodno leto gledališča Bilo je januarja A. Barto Gledališče senc Rekviziti: 1. Velik zaslon (list na kovinski palici) 2. Svetilka za vizažisti...
-
Datumi Olgine vladavine v Rusiji
Po umoru kneza Igorja so se Drevljani odločili, da je odslej njihovo pleme svobodno in da jim ni treba plačevati davka Kijevski Rusiji. Še več, njihov princ Mal se je poskušal poročiti z Olgo. Tako se je želel polastiti kijevskega prestola in sam...

