คุณสมบัติทางกายภาพและเคมีของเบนซีน คุณสมบัติทางเคมี
ปฏิกิริยากลุ่มแรกคือปฏิกิริยาทดแทน เราบอกว่าเอรีนไม่มีพันธะหลายพันธะในโครงสร้างของโมเลกุล แต่มีระบบคอนจูเกตที่ประกอบด้วยอิเล็กตรอน 6 ตัว ซึ่งมีความเสถียรมากและให้ความแข็งแรงเพิ่มเติมแก่วงแหวนเบนซีน ดังนั้นใน ปฏิกิริยาเคมีประการแรก การแทนที่อะตอมไฮโดรเจนเกิดขึ้นมากกว่าการทำลายวงแหวนเบนซีน
เราได้พบกับปฏิกิริยาการทดแทนเมื่อพูดถึงอัลเคนแล้ว แต่สำหรับพวกเขาแล้วปฏิกิริยาเหล่านี้ก็เป็นไปตามนั้น กลไกที่รุนแรงและเอรีนมีลักษณะเฉพาะด้วยกลไกไอออนิกของปฏิกิริยาทดแทน
อันดับแรกฮาโลเจนคุณสมบัติทางเคมี การแทนที่อะตอมไฮโดรเจนด้วยอะตอมฮาโลเจน คลอรีน หรือโบรมีน
ปฏิกิริยาเกิดขึ้นเมื่อถูกความร้อนและมีส่วนร่วมของตัวเร่งปฏิกิริยาเสมอ ในกรณีของคลอรีน อาจเป็นอะลูมิเนียมคลอไรด์ หรือเฟอร์ริกคลอไรด์สาม ตัวเร่งปฏิกิริยาโพลาไรซ์โมเลกุลฮาโลเจน ทำให้เกิดความแตกแยกของพันธะเฮเทอโรไลติกและผลิตไอออน
คลอรีนเป็นไอออนที่มีประจุบวกและทำปฏิกิริยากับเบนซีน
หากเกิดปฏิกิริยากับโบรมีน ตัวเร่งปฏิกิริยาคือไอรอนโบรไมด์หรืออะลูมิเนียมโบรไมด์

สิ่งสำคัญคือต้องสังเกตว่าปฏิกิริยานี้เกิดขึ้นกับโมเลกุลโบรมีน ไม่ใช่กับน้ำโบรมีน เบนซินไม่ทำปฏิกิริยากับน้ำโบรมีน
ฮาโลเจนของเบนซีนคล้ายคลึงกันมีลักษณะเป็นของตัวเอง ในโมเลกุลโทลูอีน หมู่เมทิลเอื้อต่อการแทนที่ในวงแหวน ปฏิกิริยาเพิ่มขึ้น และปฏิกิริยาเกิดขึ้นภายใต้สภาวะที่เบากว่า นั่นคือที่อุณหภูมิห้อง
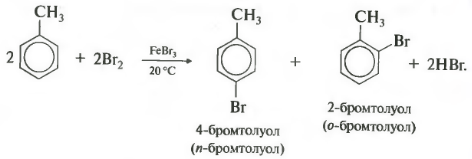
สิ่งสำคัญคือต้องสังเกตว่าการแทนที่จะเกิดขึ้นในตำแหน่งออร์โธและพาราเสมอ ดังนั้นจึงได้ส่วนผสมของไอโซเมอร์
ที่สองคุณสมบัติของไนเตรตของเบนซีน การแนะนำหมู่ไนโตรในวงแหวนเบนซีน

ของเหลวสีเหลืองหนักที่มีกลิ่นอัลมอนด์ขมจะก่อตัวเป็นไนโตรเบนซีน ดังนั้นปฏิกิริยาจึงมีคุณภาพต่อเบนซีน สำหรับไนเตรตจะใช้ส่วนผสมไนเตรตของกรดไนตริกและกรดซัลฟิวริกเข้มข้น ปฏิกิริยาเกิดขึ้นโดยการให้ความร้อน
ฉันขอเตือนคุณว่าสำหรับไนเตรตของอัลเคนในปฏิกิริยา Konovalov นั้นจะใช้กรดไนตริกเจือจางโดยไม่ต้องเติมกรดซัลฟิวริก
ในระหว่างการไนเตรตของโทลูอีนตลอดจนระหว่างฮาโลเจนจะเกิดส่วนผสมของออร์โธ - และพารา - ไอโซเมอร์

ที่สามสมบัติอัลคิเลชันของเบนซีนกับฮาโลอัลเคน

ปฏิกิริยานี้ทำให้เกิดการนำอนุมูลไฮโดรคาร์บอนเข้าไปในวงแหวนเบนซีน และถือได้ว่าเป็นวิธีการผลิตสารคล้ายคลึงกันของเบนซีน อะลูมิเนียมคลอไรด์ใช้เป็นตัวเร่งปฏิกิริยาซึ่งส่งเสริมการสลายตัวของโมเลกุลฮาโลอัลเคนให้เป็นไอออน จำเป็นต้องมีเครื่องทำความร้อนด้วย
ที่สี่สมบัติอัลคิเลชันของเบนซีนกับอัลคีน

ด้วยวิธีนี้ คุณสามารถได้รับ เช่น คิวมีนหรือเอทิลเบนซีน ตัวเร่งปฏิกิริยาอลูมิเนียมคลอไรด์
2. ปฏิกิริยาเติมเบนซีน
ปฏิกิริยากลุ่มที่สองคือปฏิกิริยาการบวก เราบอกว่าปฏิกิริยาเหล่านี้ไม่ปกติ แต่เกิดขึ้นได้ภายใต้สภาวะที่ค่อนข้างรุนแรงโดยมีการทำลายอาหาร คลาวด์อิเล็กทรอนิกส์และการเกิดพันธะหกซิกมา
ประการที่ห้าทรัพย์สินใน รายการทั่วไปการเติมไฮโดรเจน การเติมไฮโดรเจน
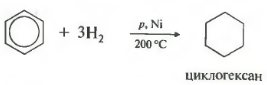
อุณหภูมิ ความดัน ตัวเร่งปฏิกิริยา นิกเกิล หรือแพลทินัม โทลูอีนสามารถทำปฏิกิริยาในลักษณะเดียวกันได้
ที่หกคุณสมบัติคลอรีน โปรดทราบว่าเรากำลังพูดถึงปฏิกิริยากับคลอรีนโดยเฉพาะ เนื่องจากโบรมีนไม่เข้าสู่ปฏิกิริยานี้

ปฏิกิริยานี้เกิดขึ้นภายใต้การฉายรังสีอัลตราไวโอเลตที่รุนแรง Hexachlorocyclohexane หรือชื่ออื่นของ hexachlorane ซึ่งเป็นของแข็งได้ถูกสร้างขึ้น
สิ่งสำคัญคือต้องจำไว้ว่าสำหรับน้ำมันเบนซิน เป็นไปไม่ได้ปฏิกิริยาการเติมของไฮโดรเจนเฮไลด์ (ไฮโดรฮาโลเจน) และการเติมน้ำ (ไฮเดรชั่น)
3. การทดแทนในห่วงโซ่ด้านข้างของสารเบนซีนที่คล้ายคลึงกัน
ปฏิกิริยากลุ่มที่สามเกี่ยวข้องกับความคล้ายคลึงกันของเบนซีนเท่านั้น - นี่คือการทดแทนในห่วงโซ่ด้านข้าง
ที่เจ็ดคุณสมบัติในรายการฮาโลเจนทั่วไปที่อะตอมคาร์บอนอัลฟ่าในสายโซ่ด้านข้าง

ปฏิกิริยานี้เกิดขึ้นเมื่อถูกความร้อนหรือฉายรังสี และจะเกิดเฉพาะที่อัลฟ่าคาร์บอนเท่านั้น ในขณะที่ฮาโลเจนยังคงดำเนินต่อไป อะตอมฮาโลเจนที่สองจะกลับสู่ตำแหน่งอัลฟา
4. ออกซิเดชันของสารเบนซีนที่คล้ายคลึงกัน
ปฏิกิริยากลุ่มที่สี่คือปฏิกิริยาออกซิเดชัน
วงแหวนเบนซีนแรงเกินไป เบนซีนก็เลย ไม่ออกซิไดซ์โพแทสเซียมเปอร์แมงกาเนตไม่เปลี่ยนสีสารละลาย นี่เป็นสิ่งสำคัญมากที่ต้องจำ
แต่ความคล้ายคลึงกันของเบนซีนจะถูกออกซิไดซ์โดยสารละลายที่เป็นกรดของโพแทสเซียมเปอร์แมงกาเนตเมื่อถูกความร้อน และนี่คือคุณสมบัติทางเคมีประการที่แปด

สิ่งนี้จะผลิตกรดเบนโซอิก สังเกตการเปลี่ยนสีของสารละลาย ในกรณีนี้ ไม่ว่าสายโซ่คาร์บอนขององค์ประกอบแทนที่จะยาวแค่ไหน มันก็จะแตกหลังจากอะตอมของคาร์บอนตัวแรกเสมอ และอะตอมอัลฟ่าจะถูกออกซิไดซ์เป็นหมู่คาร์บอกซิลที่มีการก่อตัวของกรดเบนโซอิก ส่วนที่เหลือของโมเลกุลจะถูกออกซิไดซ์เป็นกรดที่สอดคล้องกัน หรือหากเป็นคาร์บอนเพียงอะตอมเดียวก็จะถูกออกซิไดซ์ คาร์บอนไดออกไซด์.
หากความคล้ายคลึงกันของเบนซีนมีองค์ประกอบไฮโดรคาร์บอนมากกว่าหนึ่งองค์ประกอบบนวงแหวนอะโรมาติก การเกิดออกซิเดชันจะเกิดขึ้นตามกฎเดียวกัน - คาร์บอนที่อยู่ในตำแหน่งอัลฟาจะถูกออกซิไดซ์

ตัวอย่างนี้สร้างกรดอะโรมาติก dibasic ที่เรียกว่ากรดทาทาลิก
ฉันอยากจะสังเกตการเกิดออกซิเดชันของคิวมีน ไอโซโพรพิลเบนซีน โดยออกซิเจนในบรรยากาศโดยมีกรดซัลฟิวริกอยู่เป็นพิเศษ

นี่เป็นวิธีที่เรียกว่าคิวมีนในการผลิตฟีนอล ตามกฎแล้ว เราพบปฏิกิริยานี้ในเรื่องที่เกี่ยวข้องกับการผลิตฟีนอล นี่เป็นวิธีการทางอุตสาหกรรม
เก้าคุณสมบัติการเผาไหม้, ออกซิเดชันโดยสมบูรณ์กับออกซิเจน เบนซีนและความคล้ายคลึงกันของมันจะเผาไหม้เป็นคาร์บอนไดออกไซด์และน้ำ
ให้เราเขียนสมการการเผาไหม้ของเบนซีนในรูปแบบทั่วไป
ตามกฎการอนุรักษ์มวล ควรมีอะตอมทางด้านซ้ายเท่ากับจำนวนอะตอมทางด้านขวา เพราะในปฏิกิริยาเคมี อะตอมจะไม่หายไป แต่ลำดับของพันธะระหว่างอะตอมนั้นเปลี่ยนแปลงไป ดังนั้นจะมีโมเลกุลคาร์บอนไดออกไซด์มากเท่ากับอะตอมของคาร์บอนในโมเลกุลอารีน เนื่องจากโมเลกุลประกอบด้วยอะตอมของคาร์บอนหนึ่งอะตอม นั่นคือ n CO 2 โมเลกุล จะมีโมเลกุลของน้ำน้อยกว่าอะตอมไฮโดรเจนถึงสองเท่า นั่นคือ (2n-6)/2 ซึ่งหมายถึง n-3
มีจำนวนอะตอมออกซิเจนทางซ้ายและขวาเท่ากัน ทางด้านขวามี 2n จากคาร์บอนไดออกไซด์ เนื่องจากแต่ละโมเลกุลมีอะตอมออกซิเจน 2 อะตอม บวก n-3 จากน้ำ รวมเป็น 3n-3 ทางด้านซ้ายมีจำนวนอะตอมออกซิเจน 3n-3 เท่ากัน ซึ่งหมายความว่ามีโมเลกุลน้อยกว่าสองเท่า เนื่องจากโมเลกุลประกอบด้วยอะตอม 2 อะตอม นั่นคือ (3n-3)/2 โมเลกุลออกซิเจน
ดังนั้นเราจึงได้รวบรวมสมการสำหรับการเผาไหม้ของสารเบนซีนที่คล้ายคลึงกันในรูปแบบทั่วไป
ในที่สุดนางคิมิยะก็ได้รับสารประกอบเช่นเบนซินในปี พ.ศ. 2376 โดยไม่อาจเพิกถอนได้ เบนซินเป็นสารประกอบที่มีอารมณ์ร้อน ใครๆ ก็สามารถพูดได้ว่าระเบิดได้ พวกเขารู้ได้อย่างไร?
เรื่องราว
Johann Glauber ในปี 1649 หันมาสนใจสารประกอบที่ก่อตัวขึ้นสำเร็จเมื่อนักเคมีกำลังแปรรูปน้ำมันดินจากถ่านหิน แต่มันก็อยากจะไม่เปิดเผยตัวตน
ประมาณ 170 ปีต่อมา หรือถ้าให้เจาะจงกว่านี้อีกมาก ในช่วงกลางทศวรรษที่ 20 ของศตวรรษที่ 19 โดยบังเอิญ เบนซินถูกสกัดออกมาจากก๊าซที่ให้แสงสว่าง ซึ่งก็คือจากคอนเดนเสทที่ปล่อยออกมา มนุษยชาติเป็นหนี้ความพยายามดังกล่าวกับ Michael Faraday นักวิทยาศาสตร์จากอังกฤษ
กระบองสำหรับการซื้อเบนซีนถูกยึดครองโดย Eilgard Mitscherlich ชาวเยอรมัน สิ่งนี้เกิดขึ้นระหว่างการประมวลผลเกลือแคลเซียมปราศจากน้ำของกรดเบนโซอิก บางทีนั่นอาจเป็นเหตุผลว่าทำไมสารประกอบจึงได้รับชื่อเช่นนี้ - เบนซิน นักวิทยาศาสตร์เรียกมันว่าน้ำมันเบนซิน ธูป ถ้าแปลจากภาษาอาหรับ
เบนซินเผาไหม้อย่างสวยงามและสดใส จากการสังเกตเหล่านี้ Auguste Laurent แนะนำให้เรียกมันว่า "เฟน" หรือ "เบนซิน" สดใส แวววาว - ถ้าแปลมาจากภาษากรีก
จากแนวคิดเรื่องธรรมชาติของการสื่อสารทางอิเล็กทรอนิกส์และคุณสมบัติของเบนซีน นักวิทยาศาสตร์ได้เตรียมโมเลกุลของสารประกอบในรูปของภาพต่อไปนี้ นี่คือรูปหกเหลี่ยม วงกลมถูกจารึกไว้ในนั้น ข้อมูลข้างต้นแสดงให้เห็นว่าเบนซีนมีเมฆอิเล็กตรอนที่สมบูรณ์ ซึ่งล้อมรอบอะตอมคาร์บอนหกอะตอม (โดยไม่มีข้อยกเว้น) อย่างปลอดภัยในวัฏจักร ไม่พบพันธะไบนารีที่ยึดแน่น
ก่อนหน้านี้เบนซินถูกใช้เป็นตัวทำละลาย แต่โดยพื้นฐานแล้วอย่างที่พวกเขาพูดกัน เขาไม่ได้เป็นสมาชิก ไม่เข้าร่วม ไม่เกี่ยวข้อง แต่นี่คือศตวรรษที่ 19 การเปลี่ยนแปลงที่สำคัญเกิดขึ้นในศตวรรษที่ 20 คุณสมบัติของเบนซีนแสดงถึงคุณสมบัติอันทรงคุณค่าที่ช่วยให้น้ำมันเบนซินได้รับความนิยมมากขึ้น ค่าออกเทนซึ่งพบว่าสูงทำให้สามารถใช้เป็นองค์ประกอบเชื้อเพลิงในการเติมเชื้อเพลิงรถยนต์ได้ การกระทำนี้เป็นแรงผลักดันให้เกิดการถอนเบนซีนอย่างกว้างขวาง การสกัดจะดำเนินการเป็นผลิตภัณฑ์รองของการผลิตเหล็กโค้ก
เมื่ออายุสี่สิบเศษ เบนซินเริ่มถูกนำมาใช้ในด้านเคมีในการผลิตสารที่ระเบิดอย่างรวดเร็ว ศตวรรษที่ 20 เต็มไปด้วยความจริงที่ว่าอุตสาหกรรมการกลั่นน้ำมันผลิตเบนซีนได้มากจนเริ่มนำไปใช้ในอุตสาหกรรมเคมี
ลักษณะของเบนซีน
ไฮโดรคาร์บอนไม่อิ่มตัวมีความคล้ายคลึงกับเบนซินมาก ตัวอย่างเช่น ซีรีส์เอทิลีนไฮโดรคาร์บอนแสดงลักษณะเฉพาะของตัวเองว่าเป็นไฮโดรคาร์บอนไม่อิ่มตัว มีลักษณะเป็นปฏิกิริยาการเติม เบนซินเข้าสู่ทั้งหมดนี้ได้อย่างง่ายดายด้วยอะตอมที่อยู่ในระนาบเดียวกัน และตามความเป็นจริง - เมฆอิเล็กตรอนคอนจูเกต

หากมีวงแหวนเบนซีนอยู่ในสูตร เราก็สามารถสรุปเบื้องต้นได้ว่ามันคือเบนซีน ซึ่งมีสูตรโครงสร้างที่มีลักษณะเช่นนี้ทุกประการ
คุณสมบัติทางกายภาพ
เบนซินเป็นของเหลวที่ไม่มีสี แต่มีกลิ่นที่น่าเสียใจ น้ำมันเบนซินจะละลายเมื่ออุณหภูมิถึง 5.52 องศาเซลเซียส เดือดที่ 80.1 ความหนาแน่น 0.879 g/cm3 มวลโมลาร์ 78.11 g/mol เมื่อเผาจะเกิดควันมาก ก่อให้เกิดสารประกอบที่ระเบิดได้เมื่ออากาศเข้าไป หิน (น้ำมันเบนซิน อีเทอร์และอื่น ๆ) รวมกับสารที่อธิบายไว้โดยไม่มีปัญหา สร้างสารประกอบอะซีโอโทรปิกกับน้ำ การทำความร้อนก่อนการระเหยเริ่มต้นที่ 69.25 องศา (เบนซิน 91%) ที่อุณหภูมิ 25 องศาเซลเซียส สามารถละลายในน้ำได้ 1.79 กรัม/ลิตร
คุณสมบัติทางเคมี
เบนซินทำปฏิกิริยากับซัลเฟอร์และ กรดไนตริก- และยังมีอัลคีน ฮาโลเจน คลอโรอัลเคนอีกด้วย ปฏิกิริยาการทดแทนคือสิ่งที่เป็นลักษณะเฉพาะของมัน อุณหภูมิความดันส่งผลต่อการทะลุผ่านของวงแหวนเบนซีนซึ่งเกิดขึ้นภายใต้สภาวะที่ค่อนข้างรุนแรง
เราสามารถพิจารณาสมการปฏิกิริยาของเบนซีนแต่ละสมการได้อย่างละเอียดยิ่งขึ้น
1. การทดแทนด้วยไฟฟ้า โบรมีนเมื่อมีตัวเร่งปฏิกิริยาจะทำปฏิกิริยากับคลอรีน เป็นผลให้เราได้รับคลอโรเบนซีน:
С6H6+3Cl2 → C6H5Cl + HCl
2. ปฏิกิริยาฟรีเดล-คราฟต์ หรือ อัลคิเลชันของเบนซีน การปรากฏตัวของอัลคิลเบนซีนเกิดขึ้นเนื่องจากการรวมกับอัลเคนซึ่งเป็นอนุพันธ์ของฮาโลเจน:
C6H6 + C2H5Br → C6H5C2H5 + HBr
3. การทดแทนด้วยไฟฟ้า ที่นี่เกิดปฏิกิริยาของไนเตรตและซัลโฟเนชัน สมการเบนซีนจะมีลักษณะดังนี้:
C6H6 + H2SO4 → C6H5SO3H + H2O
C6H6 + HNO3 → C6H5NO2 + H2O
4. เบนซินเมื่อเผาไหม้:
2C6H6 + 15O2 → 12CO2 + 6H2O
ที่ เงื่อนไขบางประการแสดงลักษณะเฉพาะของไฮโดรคาร์บอนอิ่มตัว เมฆพีอิเล็กตรอนซึ่งอยู่ในโครงสร้างของสสารที่เป็นปัญหา อธิบายปฏิกิริยาเหล่านี้
ขึ้นอยู่กับเทคโนโลยีพิเศษ ประเภทต่างๆเบนซิน นี่คือบริเวณที่มีป้ายกำกับว่าปิโตรเลียมเบนซีน ตัวอย่างเช่น บริสุทธิ์และมีความบริสุทธิ์สูง สำหรับการสังเคราะห์ ฉันต้องการแยกบันทึกความคล้ายคลึงกันของเบนซีนออกจากกัน และโดยเฉพาะอย่างยิ่งคือคุณสมบัติทางเคมีของพวกมัน เหล่านี้คืออัลคิลเบนซีน

ความคล้ายคลึงกันของเบนซีนจะตอบสนองได้ง่ายกว่ามาก แต่ปฏิกิริยาข้างต้นของเบนซีนหรือที่คล้ายคลึงกันนั้นเกิดขึ้นพร้อมกับความแตกต่างบางประการ
ฮาโลเจนของอัลคิลเบนซีน
รูปแบบของสมการมีดังนี้:
C6H5-CH3 + Br = C6H5-CH2Br + HBr
ไม่พบแนวโน้มของโบรมีนในวงแหวนเบนซีน มันออกมาเป็นโซ่จากด้านข้าง แต่ด้วยตัวเร่งปฏิกิริยาเกลือ Al(+3) โบรมีนจึงเข้าสู่วงแหวนได้ง่าย
ไนเตรชันของอัลคิลเบนซีน
ต้องขอบคุณกรดซัลฟูริกและไนตริกที่ทำให้เบนซีนและอัลคิลเบนซีนถูกไนเตรต อัลคิลเบนซีนที่ทำปฏิกิริยา ได้รับผลิตภัณฑ์สองในสามที่นำเสนอ - เหล่านี้คือพาราและออร์โธไอโซเมอร์ คุณสามารถเขียนสูตรใดสูตรหนึ่งได้:
C6H5 - CH3 + 3HNO3 → C6H2CH3 (NO2)3
ออกซิเดชัน
สิ่งนี้เป็นที่ยอมรับไม่ได้สำหรับน้ำมันเบนซิน แต่อัลคิลเบนซีนทำปฏิกิริยาทันที ตัวอย่างเช่น กรดเบนโซอิก สูตรได้รับด้านล่าง:
C6H5CH3 + [O] → C6H5COOH
อัลคิลเบนซีนและเบนซีน การไฮโดรจิเนชันของพวกมัน
เมื่อมีเครื่องขยายเสียง ไฮโดรเจนเริ่มทำปฏิกิริยากับเบนซีน ส่งผลให้เกิดการก่อตัวของไซโคลเฮกเซนตามที่กล่าวไว้ข้างต้น ในทำนองเดียวกัน อัลคิลเบนซีนจะถูกแปลงเป็นอัลคิลไซโคลเฮกเซนอย่างง่ายดาย เพื่อให้ได้อัลคิลไซโคลเฮกเซน จำเป็นต้องเติมไฮโดรเจนให้กับอัลคิลเบนซีนที่ต้องการ นี่เป็นขั้นตอนที่จำเป็นในการผลิตผลิตภัณฑ์บริสุทธิ์ และนี่ไม่ใช่ปฏิกิริยาทั้งหมดของเบนซีนและอัลคิลเบนซีน
การผลิตเบนซีน อุตสาหกรรม
รากฐานของการผลิตดังกล่าวขึ้นอยู่กับการประมวลผลส่วนประกอบต่างๆ ได้แก่ โทลูอีน แนฟทา น้ำมันดิน ซึ่งถูกปล่อยออกมาระหว่างการแตกร้าวของถ่านหิน และอื่นๆ ดังนั้นเบนซินจึงถูกผลิตขึ้นในสถานประกอบการปิโตรเคมีและโลหะวิทยา สิ่งสำคัญคือต้องรู้วิธีรับเบนซินที่มีความบริสุทธิ์ในระดับต่างๆ เนื่องจากหลักการและวัตถุประสงค์การผลิตขึ้นอยู่กับยี่ห้อของสารนี้โดยตรง
ส่วนแบ่งของสิงโตนั้นผลิตโดยการปฏิรูปเทอร์โมคะตาไลติกของส่วนคอสโตไบโอไลต์ซึ่งเดือดที่ 65 องศาโดยมีผลสารสกัดการกลั่นด้วยไดเมทิลฟอร์มาไมด์
เมื่อผลิตเอทิลีนและโพรพิลีนจะได้ผลิตภัณฑ์ของเหลวที่เกิดขึ้นระหว่างการสลายตัวของสารประกอบอนินทรีย์และอินทรีย์ภายใต้อิทธิพลของความร้อน น้ำมันเบนซินถูกแยกออกจากพวกเขา แต่น่าเสียดายที่ตัวเลือกนี้สำหรับการสกัดเบนซีนมีแหล่งที่มาไม่มากนัก ดังนั้นสารที่เราสนใจจึงถูกสกัดโดยการปฏิรูป ด้วยวิธีนี้ทำให้ปริมาตรของเบนซีนเพิ่มขึ้น

โดยดีลคิเลชั่นที่อุณหภูมิ 610-830 องศาโดยมีเครื่องหมายบวกเมื่อมีไอน้ำที่เกิดจากการเดือดของน้ำและไฮโดรเจนจะได้เบนซีนจากโทลูอีน มีตัวเลือกอื่น - ตัวเร่งปฏิกิริยา เมื่อตรวจพบซีโอไลต์หรือตัวเร่งปฏิกิริยาออกไซด์ภายใต้อุณหภูมิ 227-627 องศา
มีอีกวิธีหนึ่งที่เก่ากว่าในการพัฒนาเบนซีน การใช้การดูดซับโดยตัวดูดซับที่มีต้นกำเนิดจากสารอินทรีย์ จะถูกแยกออกจากผลลัพธ์สุดท้ายของถ่านโค้ก ผลิตภัณฑ์นี้เป็นผลิตภัณฑ์ไอระเหยและผ่านการระบายความร้อนล่วงหน้า ตัวอย่างเช่น มีการใช้น้ำมัน ซึ่งมีแหล่งที่มาคือปิโตรเลียมหรือถ่านหิน เมื่อทำการกลั่นด้วยไอน้ำ สารดูดซับจะถูกแยกออกจากกัน การบำบัดด้วยไฮโดรทรีตติ้งช่วยกำจัดสารส่วนเกินออกจากน้ำมันเบนซินดิบ
วัตถุดิบถ่านหิน
ในทางโลหะวิทยา เมื่อใช้ถ่านหิน หรือเพื่อให้แม่นยำยิ่งขึ้น การกลั่นแบบแห้ง จะได้โค้ก ในระหว่างขั้นตอนนี้ การจ่ายอากาศจะถูกจำกัด อย่าลืมว่าถ่านหินถูกให้ความร้อนที่อุณหภูมิ 1,200-1,500 องศาเซลเซียส
สารเคมีถ่านหินเบนซีนจำเป็นต้องทำให้บริสุทธิ์อย่างทั่วถึง จำเป็นต้องกำจัดเมทิลไซโคลเฮกเซนและเอ็น-เฮปเทนซึ่งเป็นเพื่อนของมันออกไป ก็ควรถูกยึดเช่นกัน น้ำมันเบนซินเผชิญกับกระบวนการแยกและทำให้บริสุทธิ์ซึ่งจะดำเนินการมากกว่าหนึ่งครั้ง
วิธีที่อธิบายไว้ข้างต้นเป็นวิธีที่เก่าแก่ที่สุด แต่เมื่อเวลาผ่านไปก็จะสูญเสียตำแหน่งที่สูงไป
เศษส่วนน้ำมัน
0.3-1.2% - นี่คือตัวบ่งชี้องค์ประกอบของฮีโร่ของเราในน้ำมันดิบ ตัวชี้วัดน้อยในการลงทุนเงินและความพยายาม วิธีที่ดีที่สุดคือใช้ขั้นตอนทางอุตสาหกรรมในการประมวลผลเศษส่วนปิโตรเลียม นั่นก็คือการปฏิรูปตัวเร่งปฏิกิริยา เมื่อมีแอมพลิฟายเออร์อลูมิเนียม - แพลตตินัม - รีเนียมเปอร์เซ็นต์ของคาร์โบไฮเดรตอะโรมาติกจะเพิ่มขึ้นและตัวบ่งชี้ที่กำหนดความสามารถของเชื้อเพลิงที่จะไม่จุดไฟตามธรรมชาติในระหว่างการบีบอัดเพิ่มขึ้น
เรซินไพโรไลซิส
หากเราสกัดผลิตภัณฑ์ปิโตรเลียมของเราจากวัตถุดิบที่ไม่เป็นของแข็ง กล่าวคือ โดยไพโรไลซิสของโพรพิลีนและเอทิลีนที่เกิดขึ้นระหว่างการผลิต วิธีการนี้จะเป็นที่ยอมรับมากที่สุด พูดให้ถูกก็คือ เบนซินจะถูกปล่อยออกมาจากไพโรคอนเดนเสท การสลายตัวของสัดส่วนบางอย่างจำเป็นต้องมีการบำบัดด้วยไฮโดรทรีต ในระหว่างการทำความสะอาด กำมะถันและส่วนผสมที่ไม่อิ่มตัวจะถูกกำจัดออก ผลลัพธ์เบื้องต้นประกอบด้วยไซลีน โทลูอีน และเบนซีน โดยใช้การกลั่นแบบสกัดแยกกลุ่ม BTK เพื่อผลิตเบนซิน

ไฮโดรดีอัลคิเลชันของโทลูอีน
ตัวละครหลักของกระบวนการ ซึ่งก็คือการไหลของไฮโดรเจนและโทลูอีน จะถูกป้อนให้ร้อนเข้าไปในเครื่องปฏิกรณ์ โทลูอีนผ่านเตียงตัวเร่งปฏิกิริยา ในระหว่างกระบวนการนี้ หมู่เมทิลจะถูกแยกออกเป็นเบนซีน วิธีการทำความสะอาดบางอย่างมีความเหมาะสมที่นี่ ผลลัพธ์ที่ได้คือสารบริสุทธิ์สูง (สำหรับไนเตรต)
ความไม่สมส่วนของโทลูอีน
อันเป็นผลมาจากการปฏิเสธคลาสเมทิลทำให้เกิดเบนซีนและไซลีนถูกออกซิไดซ์ มีการสังเกตทรานส์อัลคิเลชันในกระบวนการนี้ ผลการเร่งปฏิกิริยาเกิดขึ้นเนื่องจากแพลเลเดียม แพลตตินัม และนีโอไดเมียมซึ่งอยู่บนอะลูมิเนียมออกไซด์
ทาลูอีนและไฮโดรเจนถูกจ่ายให้กับเครื่องปฏิกรณ์โดยมีตัวเร่งปฏิกิริยาเบดที่เสถียร จุดประสงค์คือเพื่อป้องกันไม่ให้ไฮโดรคาร์บอนตกตะกอนบนระนาบตัวเร่งปฏิกิริยา กระแสที่ออกจากเครื่องปฏิกรณ์จะถูกทำให้เย็นลง และไฮโดรเจนจะถูกนำกลับมารีไซเคิลอย่างปลอดภัยเพื่อนำไปรีไซเคิล สิ่งที่เหลืออยู่จะถูกกลั่นสามครั้ง ในระยะเริ่มแรก สารประกอบที่ไม่มีอะโรมาติกจะถูกกำจัดออก สกัดเบนซินเป็นขั้นตอนที่สอง และขั้นตอนสุดท้ายคือการแยกไซลีน
การตัดอะเซทิลีน
ต้องขอบคุณผลงานของนักเคมีกายภาพชาวฝรั่งเศส Marcelin Berthelot ที่ทำให้เบนซีนเริ่มผลิตจากอะเซทิลีน แต่สิ่งที่โดดเด่นคือค็อกเทลหนักๆ ที่ประกอบด้วยองค์ประกอบอื่นๆ มากมาย คำถามคือจะลดอุณหภูมิปฏิกิริยาได้อย่างไร คำตอบได้รับเฉพาะในช่วงปลายทศวรรษที่สี่สิบของศตวรรษที่ 20 เท่านั้น V. Reppe พบตัวเร่งปฏิกิริยาที่เหมาะสม ซึ่งกลายเป็นนิกเกิล ไตรเมอไรเซชั่นเป็นทางเลือกเดียวในการรับเบนซีนจากอะเซทิลีน

เบนซีนเกิดขึ้นจากถ่านกัมมันต์ ที่ระดับความร้อนสูง อะเซทิลีนจะไหลผ่านถ่านหิน เบนซินจะถูกปล่อยออกมาหากอุณหภูมิไม่ต่ำกว่า 410 องศา ในขณะเดียวกันก็เกิดไฮโดรคาร์บอนอะโรมาติกหลายชนิดด้วย ดังนั้นคุณจึงต้องมีอุปกรณ์ที่ดีที่สามารถทำความสะอาดอะเซทิลีนได้อย่างมีประสิทธิภาพ ด้วยวิธีการที่ใช้แรงงานเข้มข้นเช่นการตัดขอบ ทำให้มีการใช้อะเซทิลีนจำนวนมาก เพื่อให้ได้เบนซีน 15 มล. ให้ใช้อะเซทิลีน 20 ลิตร คุณสามารถดูว่ามันมีลักษณะอย่างไรและปฏิกิริยาจะใช้เวลาไม่นาน
3C2H2 → C6H6 (สมการเซลินสกี้)
3CH → CH = (เสื้อ, กท) = C6H6.
น้ำมันเบนซินใช้ที่ไหน?
เบนซินเป็นผลิตผลทางเคมีที่ได้รับความนิยมพอสมควร โดยเฉพาะอย่างยิ่งมักสังเกตเห็นว่ามีการใช้เบนซีนในการผลิตคิวมีน ไซโคลเฮกเซน และเอทิลเบนซีนอย่างไร ในการสร้างสไตรีน คุณไม่สามารถทำได้หากไม่มีเอทิลเบนซีน แหล่งที่มาของวัสดุเพื่อผลิตคาโปรแลคตัม จะใช้ไซโคลเฮกเซน เมื่อทำเทอร์โมพลาสติกเรซิน จะใช้คาโปรแลคตัม สารที่อธิบายไว้เป็นสิ่งที่ขาดไม่ได้ในการผลิตสีและสารเคลือบเงาต่างๆ
เบนซินมีอันตรายแค่ไหน?
เบนซินเป็นสารพิษ การแสดงความรู้สึกไม่สบายซึ่งมาพร้อมกับอาการคลื่นไส้และเวียนศีรษะอย่างรุนแรงเป็นสัญญาณของการเป็นพิษ แม้แต่ความตายก็ไม่สามารถตัดออกได้ ความรู้สึกยินดีที่ไม่อาจพรรณนาได้ก็ไม่น้อยไปกว่าเสียงระฆังที่น่าตกใจสำหรับพิษของเบนซีน
เบนซินเข้า. สถานะของเหลวทำให้เกิดการระคายเคืองต่อผิวหนัง ไอระเหยของเบนซินทะลุผ่านได้ง่ายแม้ผ่านสภาพสมบูรณ์ ผิว- ด้วยการสัมผัสกับสารในระยะสั้นในปริมาณเล็กน้อย แต่เป็นประจำ ผลที่ไม่พึงประสงค์จะเกิดขึ้นไม่นาน นี่อาจเป็นความเสียหายของไขกระดูกและมะเร็งเม็ดเลือดขาวเฉียบพลันชนิดต่างๆ

นอกจากนี้สารยังทำให้เกิดการเสพติดในมนุษย์ เบนซินทำตัวเหมือนยาเสพติด ควันบุหรี่ทำให้เกิดผลิตภัณฑ์ที่มีลักษณะคล้ายน้ำมันดิน เมื่อพวกเขาศึกษาสิ่งนี้ พวกเขาได้ข้อสรุปว่าเนื้อหานั้นไม่ปลอดภัยสำหรับมนุษย์ นอกเหนือจากการมีนิโคตินแล้ว ยังค้นพบการมีอยู่ของคาร์โบไฮเดรตอะโรมาติก เช่น เบนโซไพรีนอีกด้วย คุณสมบัติที่โดดเด่นเบนโซไพรีนเป็นสารก่อมะเร็ง พวกมันมีผลเสียมาก ตัวอย่างเช่นทำให้เกิดมะเร็ง
แม้จะกล่าวข้างต้นแล้ว เบนซีนก็เป็นวัตถุดิบเริ่มต้นในการผลิตต่างๆ ยาพลาสติก ยางสังเคราะห์ และแน่นอนว่ารวมถึงสีย้อมด้วย นี่เป็นผลิตผลทางเคมีและสารประกอบอะโรมาติกที่พบบ่อยที่สุด
โครงสร้างวงจรของเบนซีนถูกเสนอครั้งแรกโดย F.A. เกคูเลในปี ค.ศ. 1865

Friedrich August Kekule von Stradonitz - นักเคมีชาวเยอรมันผู้มีชื่อเสียงแห่งศตวรรษที่ 19 ในปี พ.ศ. 2397 เขาได้ค้นพบสิ่งแรก สารประกอบอินทรีย์ประกอบด้วยกรดซัลเฟอร์ - ไทโออะซิติก (กรดไทโอเอทาโนอิก) นอกจากนี้เขายังได้สร้างโครงสร้างของสารประกอบไดโซโซอีกด้วย Olnako ที่สุดของเขา ผลงานที่มีชื่อเสียงในการพัฒนาเคมีคือการสร้างโครงสร้างของเบนซีน (พ.ศ. 2409) Kekulé แสดงให้เห็นว่าพันธะคู่ของเบนซีนสลับกันรอบวงแหวน (ความคิดที่เกิดขึ้นครั้งแรกกับเขาในความฝัน) ต่อมาเขาแสดงให้เห็นว่าการจัดเรียงพันธะคู่ที่เป็นไปได้ทั้งสองแบบนั้นเหมือนกัน และวงแหวนเบนซีนนั้นเป็นลูกผสมระหว่างโครงสร้างทั้งสองนี้ ดังนั้นเขาจึงคาดการณ์แนวคิดเรื่องการสั่นพ้อง (mesomerism) ซึ่งปรากฏในทฤษฎี พันธะเคมีในช่วงต้นทศวรรษ 1930
หากเบนซีนมีโครงสร้างดังกล่าวจริงๆ อนุพันธ์ที่มีการเปลี่ยนตัว 1,2 ของมันควรมีไอโซเมอร์สองตัว ตัวอย่างเช่น,

อย่างไรก็ตาม ไม่มีเบนซีนที่ถูกแทนที่ 1,2 ตัวใดเลยที่สามารถแยกออกเป็นไอโซเมอร์สองตัวได้
ดังนั้น Kekule จึงเสนอแนะในเวลาต่อมาว่าโมเลกุลของเบนซีนมีอยู่เป็นสองโครงสร้างที่เปลี่ยนสภาพเป็นกันอย่างรวดเร็ว:

โปรดทราบว่าการแสดงแผนผังของโมเลกุลเบนซีนและอนุพันธ์ของพวกมันมักจะไม่ได้ระบุอะตอมไฮโดรเจนที่ติดอยู่กับอะตอมคาร์บอนของวงแหวนเบนซีน
ในเคมีสมัยใหม่ โมเลกุลของเบนซีนถือเป็นลูกผสมแบบเรโซแนนซ์ของรูปแบบเรโซแนนซ์แบบจำกัดทั้งสองรูปแบบนี้ (ดูหัวข้อ 2.1) คำอธิบายอีกประการหนึ่งของโมเลกุลเบนซีนนั้นขึ้นอยู่กับการพิจารณาของมัน วงโคจรของโมเลกุล- แมลง. 3.1 พบว่าอิเล็กตรอนที่อยู่ในวงโคจรของพันธะจะถูกแบ่งตำแหน่งระหว่างอะตอมคาร์บอนทั้งหมดของวงแหวนเบนซีนและก่อตัวเป็นเมฆอิเล็กตรอน ตามการแสดงนี้ โมเลกุลของเบนซีนสามารถแสดงตามอัตภาพได้ดังต่อไปนี้:
ข้อมูลการทดลองยืนยันการมีอยู่ของโครงสร้างดังกล่าวในเบนซีน หากเบนซีนมีโครงสร้างตามที่ Kekulé เสนอไว้แต่แรก โดยมีพันธะคู่คอนจูเกตสามพันธะ เบนซินก็ควรจะเกิดปฏิกิริยาเพิ่มเติม เช่น แอลคีน อย่างไรก็ตาม ตามที่กล่าวไว้ข้างต้น เบนซินไม่ได้รับปฏิกิริยาการเติม นอกจากนี้ เบนซินยังมีความเสถียรมากกว่าการมีพันธะคู่ที่แยกออกจากกันสามพันธะ แมลง. 5.3 แสดงให้เห็นว่าเอนทัลปีของเบนซีนไฮโดรจิเนชันเพื่อสร้างไซโคลเฮกเซนมีค่าลบมากกว่า
ตารางที่ 18.3 ความยาวของพันธะคาร์บอน-คาร์บอนชนิดต่างๆ


ข้าว. 18.6. โครงสร้างทางเรขาคณิตของโมเลกุลเบนซีน
มีค่ามากกว่าเอนทาลปีของการไฮโดรจิเนชันของไซโคลเฮกซีนถึงสามเท่า ความแตกต่างระหว่างปริมาณเหล่านี้มักเรียกว่าเอนทัลปีของการแยกส่วน พลังงานเรโซแนนซ์ หรือพลังงานการทำให้เสถียรของเบนซีน
พันธะคาร์บอน-คาร์บอนทั้งหมดในวงแหวนเบนซีนคือ ความยาวเท่ากันซึ่งน้อยกว่าความยาว การเชื่อมต่อ C-Cในอัลเคน แต่ยาวกว่าความยาวของพันธะ C=C ในอัลคีน (ตารางที่ 18.3) สิ่งนี้เป็นการยืนยันว่าพันธะคาร์บอน-คาร์บอนในเบนซีนเป็นลูกผสมระหว่างพันธะเดี่ยวและพันธะคู่
โมเลกุลของเบนซีนมีโครงสร้างแบน ดังแสดงในรูปที่ 1 18.6.
คุณสมบัติทางกายภาพ
เบนซีนภายใต้สภาวะปกติเป็นของเหลวไม่มีสีซึ่งกลายเป็นน้ำแข็งที่อุณหภูมิ 5.5 °C และเดือดที่ 80 °C มีกลิ่นหอมเฉพาะตัว แต่ดังที่ได้กล่าวมาแล้วมีความเป็นพิษสูง เบนซินไม่ผสมกับน้ำ และในระบบเบนซีน น้ำจะก่อตัวเป็นชั้นบนของสองชั้น อย่างไรก็ตาม มันสามารถละลายได้ในตัวทำละลายอินทรีย์ที่ไม่มีขั้ว และเป็นตัวทำละลายที่ดีสำหรับสารประกอบอินทรีย์อื่นๆ
คุณสมบัติทางเคมี
แม้ว่าเบนซีนจะเกิดปฏิกิริยาเติมบางอย่าง (ดูด้านล่าง) แต่ก็ไม่ได้แสดงพฤติกรรมทั่วไปของแอลคีน ปฏิกิริยา- ตัวอย่างเช่น ไม่เปลี่ยนสีน้ำโบรมีนหรือสารละลายไอออน ยิ่งกว่านั้นน้ำมันเบนซินไม่ใช่
เข้าสู่ปฏิกิริยาเติมด้วย กรดแก่เช่น กรดไฮโดรคลอริกหรือกรดซัลฟิวริก
ในเวลาเดียวกัน เบนซินมีส่วนร่วมในปฏิกิริยาทดแทนอิเล็กโทรฟิลิกจำนวนหนึ่ง ผลิตภัณฑ์ของปฏิกิริยาประเภทนี้ได้แก่ สารประกอบอะโรมาติกเนื่องจากในปฏิกิริยาเหล่านี้ระบบเบนซีนแบบแยกส่วนจะถูกเก็บรักษาไว้ กลไกทั่วไปในการแทนที่อะตอมไฮโดรเจนบนวงแหวนเบนซีนด้วยอิเล็กโทรฟิลมีอธิบายไว้ในส่วน 17.3. ตัวอย่างของการทดแทนเบนซีนด้วยไฟฟ้าด้วยไฟฟ้า ได้แก่ ปฏิกิริยาไนเตรชัน ฮาโลเจน ซัลโฟเนชัน และปฏิกิริยาฟรีเดล-คราฟต์
ไนเตรชัน เบนซีนสามารถไนเตรตได้ (กลุ่มที่เติมเข้าไป) โดยการบำบัดด้วยส่วนผสมของกรดไนตริกและกรดซัลฟิวริกเข้มข้น:

ไนโตรเบนซีน
เงื่อนไขของปฏิกิริยานี้และกลไกของมันได้อธิบายไว้ในส่วนนี้ 17.3.
ไนโตรเบนซีนเป็นของเหลวสีเหลืองอ่อนที่มีกลิ่นอัลมอนด์เฉพาะตัว เมื่อเบนซีนถูกไนเตรต นอกจากไนโตรเบนซีนแล้ว ยังเกิดผลึกของ 1,3-ไดไนโตรเบนซีนด้วย ซึ่งเป็นผลจากปฏิกิริยาต่อไปนี้:

ฮาโลเจน หากผสมเบนซีนกับคลอรีนหรือโบรมีนในที่มืด จะไม่เกิดปฏิกิริยาใดๆ อย่างไรก็ตามเมื่อมีตัวเร่งปฏิกิริยาที่มีคุณสมบัติของกรดลูอิสจะเกิดปฏิกิริยาการทดแทนอิเล็กโทรฟิลิกในสารผสมดังกล่าว ตัวเร่งปฏิกิริยาทั่วไปสำหรับปฏิกิริยาเหล่านี้คือเหล็ก (III) โบรไมด์และอะลูมิเนียมคลอไรด์ การทำงานของตัวเร่งปฏิกิริยาเหล่านี้คือสร้างโพลาไรเซชันในโมเลกุลฮาโลเจน ซึ่งจากนั้นจะก่อตัวเป็นสารเชิงซ้อนด้วยตัวเร่งปฏิกิริยา:
แม้ว่าจะไม่มีหลักฐานโดยตรงว่าไอออนอิสระเกิดขึ้นในกรณีนี้ก็ตาม กลไกของเบนซีนโบรมีนโดยใช้เหล็ก (III) โบรไมด์เป็นตัวพาไอออนสามารถแสดงได้ดังนี้

ซัลโฟเนชั่น เบนซีนสามารถทำให้เกิดซัลโฟเนตได้ (แทนที่อะตอมไฮโดรเจนด้วยหมู่ซัลโฟ) โดยการรีฟลักซ์ส่วนผสมกับกรดซัลฟิวริกเข้มข้นเป็นเวลาหลายชั่วโมง แต่สามารถให้ความร้อนเบนซินอย่างระมัดระวังโดยผสมกับกรดซัลฟิวริกที่เป็นควัน สูบบุหรี่ กรดซัลฟิวริกประกอบด้วยซัลเฟอร์ไตรออกไซด์ กลไกของปฏิกิริยานี้สามารถแสดงได้ด้วยแผนภาพ

ปฏิกิริยาของฟรีเดล-คราฟต์ ปฏิกิริยาของฟรีเดล-คราฟต์ เดิมเรียกว่าปฏิกิริยาการควบแน่นระหว่างสารประกอบอะโรมาติกและอัลคิลเฮไลด์เมื่อมีตัวเร่งปฏิกิริยาอะลูมิเนียมคลอไรด์ปราศจากน้ำ
ในปฏิกิริยาการควบแน่น รีเอเจนต์สองโมเลกุล (หรือรีเอเจนต์หนึ่งตัว) รวมกันจนเกิดเป็นโมเลกุลของสารประกอบใหม่ ในขณะที่โมเลกุลของสารประกอบธรรมดาบางชนิด เช่น น้ำหรือไฮโดรเจนคลอไรด์ จะถูกแยกออก (กำจัด) ออกจากพวกมัน
ในปัจจุบัน ปฏิกิริยาของฟรีเดล-คราฟต์เรียกว่าการทดแทนอิเล็กโทรฟิลิกของสารประกอบอะโรมาติก โดยที่คาร์โบเคชันหรือสารเชิงซ้อนที่มีโพลาไรซ์สูงจะมีอะตอมคาร์บอนที่มีประจุบวกเล่นบทบาทของอิเล็กโทรฟิลิก สารอิเล็กโทรฟิลิกมักเป็นอัลคิลเฮไลด์หรือคลอไรด์บางชนิด กรดคาร์บอกซิลิกแม้ว่ามันอาจเป็นอัลคีนหรือแอลกอฮอล์ก็ได้ อะลูมิเนียมคลอไรด์ปราศจากน้ำมักใช้เป็นตัวเร่งปฏิกิริยาสำหรับปฏิกิริยาเหล่านี้ ปฏิกิริยาของฟรีเดล-คราฟต์มักแบ่งออกเป็น 2 ประเภท ได้แก่ อัลคิเลชันและเอซิเลชัน
อัลคิเลชั่น ในปฏิกิริยาฟรีเดล-คราฟต์ประเภทนี้ อะตอมไฮโดรเจนหนึ่งอะตอมหรือมากกว่าบนวงแหวนเบนซีนจะถูกแทนที่ด้วยหมู่อัลคิล ตัวอย่างเช่น เมื่อส่วนผสมของเบนซีนและคลอโรมีเทนถูกให้ความร้อนอย่างอ่อนโยนโดยมีอะลูมิเนียมคลอไรด์ปราศจากน้ำ จะเกิดเมทิลเบนซีนขึ้น คลอโรมีเทนมีบทบาทเป็นสารอิเล็กโทรฟิลิกในปฏิกิริยานี้ มันถูกโพลาไรซ์ด้วยอะลูมิเนียมคลอไรด์ในลักษณะเดียวกับที่เกิดขึ้นกับโมเลกุลฮาโลเจน:
กลไกของปฏิกิริยาที่อยู่ระหว่างการพิจารณาสามารถนำเสนอได้ดังนี้

ควรสังเกตว่าในปฏิกิริยาการควบแน่นระหว่างเบนซีนและคลอโรมีเทน โมเลกุลไฮโดรเจนคลอไรด์จะถูกกำจัด โปรดทราบด้วยว่า การดำรงอยู่ที่แท้จริงเมทิลคาร์โบเคชันในรูปของไอออนอิสระเป็นที่น่าสงสัย
อัลคิเลชันของเบนซีนกับคลอโรมีเทนต่อหน้าตัวเร่งปฏิกิริยา - อะลูมิเนียมคลอไรด์ปราศจากน้ำไม่ส่งผลให้เกิดการก่อตัวของเมทิลเบนซีน ในปฏิกิริยานี้ เกิดอัลคิเลชันเพิ่มเติมของวงแหวนเบนซีน ซึ่งนำไปสู่การก่อตัวของ 1,2-ไดเมทิลเบนซีน:

อะไซเลชั่น ในปฏิกิริยาฟรีเดล-คราฟต์ประเภทนี้ อะตอมไฮโดรเจนบนวงแหวนเบนซีนจะถูกแทนที่ด้วยหมู่อะซิล ส่งผลให้เกิดคีโตนอะโรมาติก
หมู่เอซิลมีสูตรทั่วไป
ชื่อที่เป็นระบบของสารประกอบอะซิลเกิดขึ้นโดยการแทนที่ส่วนต่อท้ายและลงท้ายด้วย -ova ในชื่อของกรดคาร์บอกซิลิกที่เกี่ยวข้อง ซึ่งสารประกอบอะซิลนี้เป็นอนุพันธ์ โดยมีคำต่อท้าย -(o) yl ตัวอย่างเช่น

เอซิเลชันของเบนซีนดำเนินการโดยใช้คลอไรด์หรือแอนไฮไดรด์ของกรดคาร์บอกซิลิกใดๆ ต่อหน้าตัวเร่งปฏิกิริยา อะลูมิเนียมคลอไรด์ปราศจากน้ำ ตัวอย่างเช่น

ปฏิกิริยานี้คือการควบแน่นซึ่งโมเลกุลไฮโดรเจนคลอไรด์ถูกกำจัดออกไป โปรดทราบด้วยว่าชื่อ "ฟีนิล" มักใช้เพื่ออ้างถึงวงแหวนเบนซีนในสารประกอบโดยที่เบนซีนไม่ใช่กลุ่มหลัก:

ปฏิกิริยาการเติม แม้ว่าเบนซีนจะมีลักษณะเฉพาะมากที่สุดโดยปฏิกิริยาการแทนที่อิเล็กโทรฟิลิก แต่ก็ยังผ่านปฏิกิริยาการเติมบางอย่างด้วย เราได้พบหนึ่งในนั้นแล้ว มันเกี่ยวกับเกี่ยวกับการเติมไฮโดรเจนของเบนซีน (ดูหัวข้อ 5.3) เมื่อส่วนผสมของเบนซีนและไฮโดรเจนถูกส่งผ่านบนพื้นผิวของตัวเร่งปฏิกิริยานิกเกิลบดละเอียดที่อุณหภูมิ 150-160 °C จะเกิดปฏิกิริยาทั้งหมดตามลำดับ ซึ่งจบลงด้วยการก่อตัวของไซโคลเฮกเซน สมการปริมาณสัมพันธ์โดยรวมสำหรับปฏิกิริยานี้สามารถแสดงได้ดังนี้:

ภายใต้อิทธิพลของรังสีอัลตราไวโอเลตหรือโดยตรง แสงแดดเบนซินยังทำปฏิกิริยากับคลอรีนอีกด้วย ปฏิกิริยานี้เกิดขึ้นผ่านกลไกอนุมูลที่ซับซ้อน ผลิตภัณฑ์ขั้นสุดท้ายคือ 1,2,3,4,5,6-hexachlorocyclohexane:

ปฏิกิริยาที่คล้ายกันเกิดขึ้นระหว่างเบนซีนและโบรมีนภายใต้อิทธิพลของรังสีอัลตราไวโอเลตหรือแสงแดด
ออกซิเดชัน. เบนซีนและวงแหวนเบนซีนในสารประกอบอะโรมาติกอื่นๆ พูดโดยทั่วไปว่าทนทานต่อการเกิดออกซิเดชันแม้โดยตัวออกซิไดซ์ที่แรงเช่นสารละลายที่เป็นกรดหรือด่างของโพแทสเซียมเปอร์แมงกาเนต อย่างไรก็ตาม เบนซินและสารประกอบอะโรมาติกอื่นๆ จะเผาไหม้ในอากาศหรือออกซิเจนเพื่อสร้างเปลวไฟที่มีควันมาก ซึ่งเป็นเรื่องปกติของไฮโดรคาร์บอนที่มีปริมาณคาร์บอนสัมพัทธ์สูง

ความคล้ายคลึงกันของเบนซีนสามารถทำปฏิกิริยาในสองทิศทางโดยมีส่วนร่วมของแกนอะโรมาติกและโซ่ด้านข้าง (หมู่อัลคิล) ขึ้นอยู่กับลักษณะของรีเอเจนต์
1.ปฏิกิริยาต่อวงแหวนอะโรมาติก
เนื่องจากผลของผู้บริจาคของกลุ่มอัลคิล ปฏิกิริยา S E ArH จึงดำเนินต่อไป ออร์โธ- และ คู่-ตำแหน่งของวงแหวนอะโรมาติกในขณะที่สภาวะจะรุนแรงกว่าเบนซีน
ก) ฮาโลเจน

b) ไนเตรต


สังเกตว่าเมื่อจำนวนกลุ่มตัวรับ (-NO2) เพิ่มขึ้น อุณหภูมิของปฏิกิริยาไนเตรชันจะเพิ่มขึ้น
c) ซัลโฟเนชัน

ปฏิกิริยาส่วนใหญ่ก่อให้เกิด n-ไอโซเมอร์
d) อัลคิเลชัน

จ) อะคิเลชัน

2. ปฏิกิริยาลูกโซ่ด้านข้าง
ชิ้นส่วนอัลคิลของโมเลกุลเบนซีนจะเข้าสู่ปฏิกิริยา S R ที่เกี่ยวข้องกับอะตอมของคาร์บอน α - ตำแหน่ง (ตำแหน่งเบนซิล)


การเกิดออกซิเดชันของสารเบนซีนที่คล้ายคลึงกันทั้งหมดด้วย KMnO 4 /100°C ทำให้เกิดกรดเบนโซอิก
สนามกีฬาที่อัดแน่น

เอรีนควบแน่นเป็นระบบอะโรมาติก (n=2 และ 3) ระดับความอะโรมาติกของเอรีนที่ควบแน่นนั้นต่ำกว่าเบนซีน มีลักษณะพิเศษคือปฏิกิริยาทดแทนอิเล็กโทรฟิลิก ปฏิกิริยาการเติม และปฏิกิริยาออกซิเดชัน ซึ่งเกิดขึ้นภายใต้สภาวะที่รุนแรงกว่าเบนซีน
ปฏิกิริยาของแนฟทาลีน
ปฏิกิริยา S E ArH สำหรับแนฟทาลีนดำเนินการตามส่วนใหญ่ α - ตำแหน่ง ยกเว้นซัลโฟเนชัน การเติม Ad E ด้วยอิเล็กโทรฟิลิกเกิดขึ้นที่ตำแหน่ง 1,4 โดยแนฟทาลีนแสดงคุณสมบัติของคอนจูเกตไดอีน
1. ปฏิกิริยาการทดแทนด้วยไฟฟ้าส อี อาร์เอช


2. ปฏิกิริยาของการเติมอิเล็กโทรฟิลิก รีดิวซ์ และออกซิเดชัน


ปฏิกิริยาของแอนทราซีนและฟีแนนทรีน
ปฏิกิริยาของการแทนที่ด้วยอิเล็กโทรฟิลิก, S E ArH และการเติมอิเล็กโทรฟิลิก, Ad E สำหรับแอนทราซีนเกิดขึ้นส่วนใหญ่ที่ตำแหน่ง 9 และ 10 (ดูแผนภาพด้านล่าง)

ปฏิกิริยาของการแทนที่ด้วยอิเล็กโทรฟิลิก S E ArH และการเติมอิเล็กโทรฟิลิก Ad E สำหรับฟีแนนทรีนเกิดขึ้นส่วนใหญ่ที่ตำแหน่ง 9 และ 10 สำหรับแอนทราซีน (ดูแผนภาพด้านล่าง)

ปฏิกิริยาออกซิเดชันและการรีดักชันของแอนทราซีนและฟีแนนทรีน


โครงสร้างของยาบางชนิดที่มีแนฟทาลีน แอนทราซีนและฟีแนนทรีน
แนฟธิซิน(แนฟาโซลีน, ซาโนริน)

ผลของหลอดเลือดหดตัว(รักษาโรคจมูกอักเสบ ไซนัสอักเสบ)
(ชื่อเรื่องเน้นโครงสร้างเดิมให้สังเกตเลข)
นาฟติฟิน

ต้านเชื้อราการกระทำ (รักษาโรคผิวหนัง)
นภเมธร

ต้านการอักเสบลดไข้ยาแก้ปวด(รักษาโรคข้อเข่าเสื่อม โรคข้ออักเสบรูมาตอยด์)
นาโดล

(คำว่า cis ในกรณีนี้หมายถึงตำแหน่งสัมพัทธ์ของหมู่ไฮดรอกซิล)
ความดันโลหิตตก(ลดความดันโลหิต) และ ผลต้านการเต้นของหัวใจ
มอร์ฟีน โคเดอีน

ทดสอบคำถามสำหรับบท “ARENAS”
1. คุณสมบัติอะไรของเบนซีนที่แตกต่างจากสารประกอบไม่อิ่มตัวอื่น ๆ - อัลคีน, อัลไคน์? คำว่า "สารประกอบอะโรมาติก" หมายถึงอะไร?
2. เขียน สูตรโครงสร้างสารประกอบ: ก) เอทิลเบนซีน; b) 1,3-ไดเมทิลเบนซีน ( ม -ไซลีน); c) 1,3,5-ไตรเมทิลเบนซีน (เมซิทิลีน); d) ไอโซโพรพิลเบนซีน (คิวมีน); จ) 3-ฟีนิลเพนเทน; f) ไวนิลเบนซีน (สไตรีน); g) ฟีนิลอะเซทิลีน; ชม) ความมึนงง -ไดฟีนิลเอทิลีน ( ความมึนงง -stilbene)
3. อธิบายลักษณะโครงสร้างของสารประกอบที่มีกลิ่นอะโรมาติก กำหนดกฎของHückel สารประกอบใดต่อไปนี้เป็นอะโรมาติก:

4. เปรียบเทียบอัตราส่วนของไซโคลเฮกซีนและเบนซีนกับรีเอเจนต์ต่อไปนี้ภายใต้เงื่อนไขที่กำหนด : ก) พี่ 2 (ชม 2 โอ้ 20 ค); ข) KMnO 4 (ชม 2 อ.0 ค); ค) น 2 ดังนั้น 4 (สรุป), 20 ซี; ง) ฮ 2 (ปด, 30 ค); จ) โอ้ 3 แล้วฮ 2 O(สังกะสี); ฉ) HBr
5. เขียนสูตรโครงสร้างของเบนซีนที่ถูกทดแทนเดี่ยวที่เกิดขึ้นในปฏิกิริยาของเบนซีนด้วยรีเอเจนต์ต่อไปนี้: หนึ่ง 2 ดังนั้น 4 (สรุป); ข) HNO 3 - เอ็น 2 ดังนั้น 4 (สรุป); ค) พี่ 2 /เฟ; ง) Cl 2 /อัลคลู 3 - จ) ช 3 Br/อัลบรา 3 - จ) ช 3 COCl/AlСl 3 . ตั้งชื่อปฏิกิริยาและผลิตภัณฑ์ของพวกเขา ระบุว่าอิเล็กโทรไลต์เบนซีนทำปฏิกิริยาใดในแต่ละกรณี
6. ให้รูปแบบทั่วไปสำหรับปฏิกิริยาของเบนซีนกับรีเอเจนต์อิเล็กโทรฟิลิก ( อี + - ตั้งชื่อคอมเพล็กซ์ระดับกลาง ขั้นตอนใดมักกำหนดอัตราการเกิดปฏิกิริยา ให้กราฟการเปลี่ยนแปลงพลังงานศักย์ของปฏิกิริยาที่กำลังพิจารณา
7. กำหนดแนวคิดต่อไปนี้: ก) สถานะการเปลี่ยนแปลง; b) การเชื่อมต่อระดับกลาง; c) -ซับซ้อน; ง)-ซับซ้อน อันไหนเหมือนกัน? แสดงแนวคิดเหล่านี้โดยใช้ตัวอย่างของเบนซีนโบรมีนเมื่อมีตัวเร่งปฏิกิริยา ก.พ 3 .
8. ใช้ตัวอย่างปฏิกิริยาของเอเธนและเบนซีนกับโบรมีน เปรียบเทียบกลไกของการเติมอิเล็กโตรฟิลิกในอัลคีนกับกลไกการแทนที่อิเล็กโทรฟิลิกในชุดอะโรมาติก ความแตกต่างที่สังเกตได้ในระยะใดและเพราะเหตุใด
9. ใช้เอฟเฟกต์อุปนัยและเมโซเมอร์เพื่ออธิบายปฏิสัมพันธ์ขององค์ประกอบทดแทนกับวงแหวนเบนซีนในสารประกอบที่ระบุ:

ติดป้ายกำกับองค์ประกอบย่อยที่บริจาคอิเล็กตรอน (ED) และองค์ประกอบย่อยที่ถอนอิเล็กตรอน (EA)
10. เขียนแผนการสำหรับโมโนไนเตรตของสารประกอบ: ก) ฟีนอล; b) กรดเบนซีนซัลโฟนิก; c) ไอโซโพรพิลเบนซีน; ง) คลอโรเบนซีน อัตราการทดแทนสัมพัทธ์ของสารประกอบใดควรสูงที่สุด เพราะเหตุใด
11. การก่อตัวของผลิตภัณฑ์ที่ควรคาดหวังในระหว่างการโมโนซัลโฟเนชันของสารประกอบ: a) โทลูอีน; ข) ไนโตรเบนซีน; c) กรดเบนโซอิก; ง) โบรโมเบนซีน? สารประกอบใดควรซัลโฟเนตง่ายที่สุด? ทำไม
12. จัดเรียงสารประกอบต่อไปนี้เพื่อเพิ่มความไวปฏิกิริยาเมื่อโบรมีนกลายเป็นวงแหวนเบนซีน: ก) เบนซิน; ข) ฟีนอล; c) เบนซาลดีไฮด์; ง) เอทิลเบนซีน ให้คำอธิบาย.
13. ตั้งชื่อไฮโดรคาร์บอนดังต่อไปนี้:

14. เขียนปฏิกิริยาของเบนซีนกับรีเอเจนต์ต่อไปนี้ : ก) Cl 2 (เฟ); ข) 3Cl 2 (แสงสว่าง); ค) เอชเอ็นโอ 3 (ชม 2 ดังนั้น 4 - ทำ 2 (อากาศ) (วี 2 เกี่ยวกับ 5 , 450 ค); จ) 3O 3 แล้วเอ็น 2 O(สังกะสี); จ) ฮ 2 ดังนั้น 4 (โอเลียม); ก) 3H 2 (นี, 200 ค,พี ). ปฏิกิริยาการเติมในเบนซีนมีคุณสมบัติอย่างไร?
15. เขียนปฏิกิริยาของโทลูอีนกับรีเอเจนต์ที่ระบุ : ก) 3ชม 2 (นี, 200 C, 9806.7 กิโลปาสคาล); ข) KMnO 4 วี เอ็น 2 เกี่ยวกับ; ค*) ค 2 , แสงสว่าง; ง*) Cl 2 (เฟ); จ*) ช 3 Cl(อัลCl 3 - จ*) ช 3 COCl (AlCl 3 - ก) HNO 3 (ชม 2 ดังนั้น 4 ). สำหรับปฏิกิริยาที่มีเครื่องหมายดอกจัน ให้กำหนดกลไก
16. เขียนปฏิกิริยาไนเตรตของเอทิลเบนซีนภายใต้เงื่อนไขที่ระบุ: ก) HNO 65% 3 +ฮ 2 ดังนั้น 4 (สรุป); ข) 10% HNO 3 , เครื่องทำความร้อน, ความดัน นำกลไกต่างๆ.
17. เปรียบเทียบอัตราส่วนของไอโซโพรพิลเบนซีนต่อโบรมีน: ก) ต่อหน้า อัลบรา 3 - b) ภายใต้แสงสว่างและความร้อน ให้ปฏิกิริยาและกลไกของมัน
18.สารประกอบใดที่เกิดขึ้นจากเอทิลเบนซีนและ n -ไซลีนภายใต้การกระทำของสารออกซิไดซ์ที่ระบุ: ก) โอ้ 3 แล้วฮ 2 O(สังกะสี); ข) KMnO 4 ใน H 2 เกี่ยวกับ,ที - ค) เค 2 Cr 2 โอ 7 ใน H 2 ดังนั้น 4 , ที ?
19. สามารถแยกแยะสารประกอบคู่ต่อไปนี้โดยปฏิกิริยาใด: ก) เอทิลเบนซีน และ ม -ไซลีน; b) เอทิลเบนซีนและสไตรีน; c) สไตรีนและฟีนิลอะเซทิลีน ช) โอ - และ n -ไซลีน?
20. สารประกอบใดเป็นผลผลิตของปฏิกิริยาต่อไปนี้

21. ขึ้นอยู่กับเบนซีนและรีเอเจนต์อื่นๆ จะได้สารประกอบด้านล่าง: ก) n -ถู -บิวทิลโทลูอีน; b) เอทิล- n -โทลิลคีโตน; c) อะลิลเบนซีน; ช) n -กรดโบรโมเบนโซอิก
22. จงตั้งชื่อสารประกอบหลักที่เกิดขึ้นจากปฏิกิริยาต่อไปนี้:

ไฮโดรคาร์บอนอย่างง่าย เป็นของอะโรมาติกไฮโดรคาร์บอนซึ่งเป็นสารอินทรีย์ประเภทหนึ่ง
สารนี้เป็นของเหลวใส ไม่มีสี และมีกลิ่นเฉพาะตัวหวาน เบนซีนจัดเป็นไฮโดรคาร์บอนไม่อิ่มตัว มีการเสนอสูตรวงแหวนเบนซีนอันโด่งดัง ผู้ได้รับรางวัลโนเบลในวิชาเคมี - Linus Pauling เขาเป็นคนที่เสนอให้วาดภาพเบนซินเป็นรูปหกเหลี่ยมโดยมีวงกลมอยู่ข้างใน ภาพนี้ให้ความเข้าใจเกี่ยวกับการไม่มีพันธะคู่และการมีอยู่ของเมฆอิเล็กตรอนเพียงก้อนเดียว ซึ่งครอบคลุมอะตอมของคาร์บอนทั้ง 6 อะตอม
สูตร
การได้รับน้ำมันเบนซิน
แหล่งธรรมชาติ
แหล่งธรรมชาติในการรับเบนซีนคือถ่านหิน กระบวนการทำถ่านโค้กถูกค้นพบโดย Michael Faraday เมื่อปี 1825 เขาศึกษาก๊าซส่องสว่างที่ใช้ในโคมไฟถนนและสามารถแยกและอธิบายเบนซินได้ ปัจจุบันนี้ในทางปฏิบัติแล้ว เบนซินไม่ได้มาจากน้ำมันถ่านหินโดยใช้วิธีนี้ มีหลายวิธีที่มีประสิทธิผลมากขึ้นในการได้รับมัน
แหล่งที่มาของการได้รับเทียม
- การปฏิรูปตัวเร่งปฏิกิริยาประดิษฐ์ของน้ำมันเบนซินเศษส่วนปิโตรเลียมน้ำมันเบนซินใช้สำหรับการผลิต ในกระบวนการนี้มันจะถูกสร้างขึ้น จำนวนมากโทลูอีน โทลูอีนเป็นที่ต้องการของตลาดไม่มากนัก ดังนั้นเบนซีนจึงถูกผลิตจากโทลูอีนเพิ่มเติมด้วย เบนซีนได้มาจากเศษส่วนของน้ำมันหนักโดยวิธีไพโรไลซิสผ่านกระบวนการดีลคิเลชันของส่วนผสมของโทลูอีนและไซลีน
- การเตรียมโดยวิธี Reppeจนถึงปี ค.ศ. 1948 เบนซีนได้มาจากวิธี Berthelot โดยการส่งอะเซทิลีนไปเหนือถ่านกัมมันต์ที่อุณหภูมิ 400°C ผลผลิตของเบนซินมีมาก แต่ผลลัพธ์ที่ได้คือส่วนผสมของสารหลายองค์ประกอบที่ยากต่อการทำให้บริสุทธิ์ ในปีพ.ศ. 2491 Reppe ได้เปลี่ยนถ่านกัมมันต์เป็นนิกเกิล ผลที่ได้คือน้ำมันเบนซิน กระบวนการนี้เรียกว่า การตัดแต่งอะเซทิลีน– อะเซทิลีนสามโมเลกุลถูกแปลงเป็นเบนซีนเดียว:
3C 2 H 2 → C 6 H 6
คุณสมบัติของเบนซีน
คุณสมบัติทางกายภาพ
เมื่อเผาเขม่าจำนวนมากจะถูกปล่อยออกมาเนื่องจากไฮโดรคาร์บอนไม่อิ่มตัว (ขาดไฮโดรเจน 8 อะตอมเพื่อให้เป็นไปตามสูตรมาตรฐานสำหรับไฮโดรคาร์บอนอิ่มตัว) ที่ อุณหภูมิต่ำเบนซินกลายเป็นมวลผลึกสีขาว
คุณสมบัติทางเคมี
เบนซีนเกิดปฏิกิริยาทดแทนเมื่อมีตัวเร่งปฏิกิริยา - โดยปกติจะเป็นเกลือ Al(3+) หรือ Fe(3+):
- ฮาโลเจน – ปฏิกิริยาเชิงคุณภาพสำหรับน้ำมันเบนซินที่มี Br 2:
C 6 H 6 + Br 2 = C 6 H 5 Br + HBr
- ไนเตรชันคือการทำปฏิกิริยากับกรดไนตริก ใน เคมีอินทรีย์กระบวนการนี้มาพร้อมกับการกำจัดกลุ่ม OH:
C 6 H 6 + HO-NO 2 → C 6 H 5 NO 2 + H 2 O
- ตัวเร่งปฏิกิริยาอัลคิเลชันนำไปสู่การผลิตเบนซีนที่คล้ายคลึงกัน - อัลคิลเบนซีน:
ค 6 H 6 + C 2 H 5 Cl → C 6 H 5 C 2 H 5 + HCl
เบนซีนคล้ายคลึงกันที่มีปฏิกิริยารุนแรงแตกต่างจากเบนซีนในตัวมันเอง ปฏิกิริยาแตกต่างออกไปและบ่อยครั้งในที่มีแสง:
- ฮาโลเจน C 6 H 5 -CH 3 + Br 2 (ในแสง) = C 6 H 5 -CH 2 Br + HBr;
- ไนเตรต – C 6 H 5 -CH 3 + 3HNO 3 → C 6 H 2 CH 3 (NO 2) 3
ปฏิกิริยาออกซิเดชันของเบนซีนมีความซับซ้อนมากและไม่ใช่เรื่องปกติสำหรับสารนี้ ออกซิเดชันเป็นเรื่องปกติสำหรับโฮโมล็อก ตัวอย่างเช่น นี่คือปฏิกิริยาในการผลิตกรดเบนโซอิก:
C 6 H 5 CH 3 + [O] → C 6 H 5 COOH
กระบวนการเผาไหม้ของสารเกิดขึ้นตามรูปแบบมาตรฐานสำหรับสารอินทรีย์ทั้งหมด:
C n H 2n-6 + (3n-3)\2 O 2 → nCO 2 + (n-3)H 2 O
ปฏิกิริยาไฮโดรจิเนชัน ปฏิกิริยามีความซับซ้อน โดยต้องใช้ตัวเร่งปฏิกิริยา ความดัน และอุณหภูมิ ปฏิกิริยาของเบนซีนกับไฮโดรเจนทำให้เกิดไซโคลเฮกเซน:
ค 6 ชม. 6 + 3 ชม. 2 → ค 6 ชม. 12
และในการทำปฏิกิริยากับอัลคิลเบนซีน - เมทิลไซโคลเฮกเซนโดยที่อะตอมไฮโดรเจนหนึ่งอะตอมถูกแทนที่ด้วยกลุ่มหัวรุนแรง -CH 3:
ค 6 ชั่วโมง 5 CH 3 + 3H 2 → C 6 H 11 -CH 3
การใช้น้ำมันเบนซิน
เบนซินในรูปบริสุทธิ์แทบไม่เคยใช้เลย ผลิตขึ้นเพื่อผลิตสารประกอบสำคัญอื่นๆ เช่น เอทิลเบนซีน ซึ่งได้มาจากสไตรีนและโพลีสไตรีน
เบนซินส่วนใหญ่ใช้ในการผลิตฟีนอล ซึ่งจำเป็นในการผลิตไนลอน สีย้อม ยาฆ่าแมลง และยารักษาโรค ไม่สามารถรับยาแอสไพรินที่มีชื่อเสียงได้หากไม่มีส่วนร่วมของฟีนอล
ไซโคลเฮกเซนจากเบนซีนจำเป็นสำหรับการผลิตพลาสติกและเส้นใยเทียม ไนโตรเบนซีนใช้ในการผลิตอะนิลีน ซึ่งใช้สำหรับการผลิตยาง สีย้อม และสารกำจัดวัชพืช
บทความที่เกี่ยวข้อง
-
การสังเคราะห์กลไกลูกเบี้ยวแบบไดนามิก ตัวอย่างกฎการเคลื่อนที่แบบไซน์ซอยด์ของกลไกลูกเบี้ยว
กลไกลูกเบี้ยวเป็นกลไกที่มีคู่จลนศาสตร์ที่สูงกว่า ซึ่งมีความสามารถในการรับประกันว่าการเชื่อมต่อเอาท์พุตยังคงอยู่ และโครงสร้างประกอบด้วยอย่างน้อยหนึ่งลิงค์ที่มีพื้นผิวการทำงานที่มีความโค้งแปรผัน กลไกลูกเบี้ยว...
-
สงครามยังไม่เริ่มแสดงทั้งหมดพอดคาสต์ Glagolev FM
บทละครของ Semyon Alexandrovsky ที่สร้างจากบทละครของ Mikhail Durnenkov เรื่อง "The War Has not Started Yet" จัดแสดงที่โรงละคร Praktika อัลลา เชนเดอโรวา รายงาน ในช่วงสองสัปดาห์ที่ผ่านมา นี่เป็นการฉายรอบปฐมทัศน์ที่มอสโกครั้งที่สองโดยอิงจากข้อความของ Mikhail Durnenkov....
-
การนำเสนอในหัวข้อ "ห้องระเบียบวิธีใน dhow"
- การตกแต่งสำนักงานในสถาบันการศึกษาก่อนวัยเรียน การป้องกันโครงการ "การตกแต่งสำนักงานปีใหม่" สำหรับปีโรงละครสากล ในเดือนมกราคม A. Barto Shadow อุปกรณ์ประกอบฉากโรงละคร: 1. หน้าจอขนาดใหญ่ (แผ่นบนแท่งโลหะ) 2. โคมไฟสำหรับ ช่างแต่งหน้า...
-
วันที่รัชสมัยของ Olga ใน Rus
หลังจากการสังหารเจ้าชายอิกอร์ ชาว Drevlyans ตัดสินใจว่าต่อจากนี้ไปเผ่าของพวกเขาจะเป็นอิสระ และพวกเขาไม่ต้องแสดงความเคารพต่อเคียฟมาตุส ยิ่งไปกว่านั้น เจ้าชาย Mal ของพวกเขายังพยายามแต่งงานกับ Olga ดังนั้นเขาจึงต้องการยึดบัลลังก์ของ Kyiv และด้วยตัวคนเดียว...
-
ดาวน์โหลดฟรีและไม่ต้องลงทะเบียน
ตัวอักษร O – A ในราก -RAST-, -RASH-, -ROST- บทเรียนภาษารัสเซียในชั้นประถมศึกษาปีที่ 5 จัดทำโดยครูภาษาและวรรณคดีรัสเซียของ Nizhne-Solotinskaya OOSH N.A. Loktionova
-
เป้าหมายที่ควรรู้: ในกรณีใดบ้างที่สระ O – ตัวสำรองใน...
การนำเสนอ - นิทานคืออะไร?
