องค์ประกอบของการกระจายตัวและประสบการณ์ของอนุภาค ฟิสิกส์อะตอม การทดลองของรัทเทอร์ฟอร์ด เรื่อง การกระเจิงของอนุภาคแอลฟา การทดลองของรัทเธอร์ฟอร์ด: แบบจำลองนิวเคลียร์ของอะตอม
บทเรียนฟิสิกส์ในเกรด 11
เรื่อง:
"การทดลองการกระเจิงของอนุภาคแอลฟาของรัทเทอร์ฟอร์ด"
เป้าหมายและวัตถุประสงค์ของบทเรียน:
ทางการศึกษา:
อธิบายกลไกการทดลองของรัทเทอร์ฟอร์ด
ทางการศึกษา:
พัฒนาความเป็นอิสระทางปัญญาของนักเรียน
มีส่วนสนับสนุนการศึกษาคุณธรรมและสุนทรียศาสตร์
ทางการศึกษา:
พัฒนาความสามารถในการเน้นหลักสำคัญเปรียบเทียบข้อเท็จจริงที่กำลังศึกษาและแสดงความคิดอย่างมีเหตุผล
ความคืบหน้าของบทเรียน:
ฉัน.องค์กร ช่วงเวลา.
ยืนตรงข้างโต๊ะและทำความสะอาดตัวเอง กล่าวสวัสดีกับอาจารย์ จากนั้นนั่งเงียบ ๆ บนที่นั่งของคุณและรักษาความสงบเรียบร้อยในห้องเรียน
การกำหนดหัวข้อและวัตถุประสงค์ของบทเรียน
ครั้งที่สอง การทำซ้ำ
สเปกตรัมเส้น
1.คำว่าอะตอมหมายถึงอะไร2.นักวิทยาศาสตร์คนใดค้นพบกฎของการทำซ้ำคุณสมบัติขององค์ประกอบทางเคมีเป็นระยะ?
3.อะตอมแบ่งแยกไม่ได้หรือไม่?
4.จะเกิดอะไรขึ้นกับก๊าซทำให้บริสุทธิ์เมื่อถูกความร้อนถึง อุณหภูมิสูง?
5. เส้นหลากสีที่คั่นด้วยช่องว่างมืดชื่ออะไร
6.ก๊าซแต่ละชนิดมีอะไรบ้าง?
7.ก๊าซชนิดใดมีสเปกตรัมที่ง่ายที่สุด?
8.สเปกตรัมของก๊าซข้อใดประกอบด้วย 4 เส้น
9. นักวิทยาศาสตร์คนใดเลือกสูตรเส้นสเปกตรัมสำหรับบริเวณที่มองเห็นได้
10. ทฤษฎีของใครที่ทำให้สามารถรวมสูตรของบริเวณที่มองเห็น, อัลตราไวโอเลต และอินฟราเรด ให้เป็นสูตรทั่วไปสูตรเดียวได้
ฟิซมินุตกาตามวิดีโอ
ที่สาม. วัสดุใหม่
§ 7.2 การทดลองของรัทเทอร์ฟอร์ด เรื่อง การกระเจิงของอนุภาคแอลฟา
โดยการศึกษาการกระเจิงของอนุภาคแอลฟาขณะผ่านแผ่นทองคำเออร์เนสต์รัทเทอร์ฟอร์ดได้ข้อสรุปว่าประจุบวกของอะตอมทั้งหมดกระจุกตัวอยู่ที่ศูนย์กลางในนิวเคลียสที่มีมวลมากและกะทัดรัด และอนุภาคที่มีประจุลบ (อิเล็กตรอน) จะหมุนรอบนิวเคลียสนี้

แบบจำลองนี้แตกต่างโดยพื้นฐานจากแบบจำลองอะตอมของทอมสันซึ่งแพร่หลายในขณะนั้น

โจเซฟ จอห์นทอมสันเสนอแบบจำลองของอะตอมในรูปของพุดดิ้ง (พาย) ซึ่งมีประจุบวกเติมเต็มปริมาตรอะตอมทั้งหมดอย่างสม่ำเสมอ และอิเล็กตรอนก็กระจายไปด้วย

ต่อมาแบบจำลองของรัทเทอร์ฟอร์ดถูกเรียกว่าแบบจำลองดาวเคราะห์ของอะตอม (มันคล้ายกันมากกับ ระบบสุริยะ: แกนกลางหนักคือดวงอาทิตย์ และอิเล็กตรอนที่หมุนรอบแกนกลางคือดาวเคราะห์)
ในปี 1912 อี. รัทเทอร์ฟอร์ดและผู้ร่วมงานของเขาได้ทำการทดลองเรื่องการกระเจิงของอนุภาคแอลฟาในสสาร

แผนการทดลองของรัทเทอร์ฟอร์ด
เมื่อไม่มีฟอยล์ วงกลมสว่างก็ปรากฏขึ้นบนหน้าจอ ซึ่งประกอบด้วยแสงแวววาวที่เกิดจากลำแสงอนุภาคอัลฟ่าบางๆ แต่เมื่อวางแผ่นฟอยล์สีทองบาง ๆ ที่มีความหนาประมาณ 0.1 μm (ไมครอน) ในเส้นทางของอนุภาคอัลฟ่า ภาพที่สังเกตได้บนหน้าจอก็เปลี่ยนไปอย่างมาก กล่าวคือ แสงวาบแต่ละครั้งไม่เพียงปรากฏอยู่นอกวงกลมก่อนหน้าเท่านั้น แต่ยังอาจปรากฏขึ้นอีกด้วย สังเกตจากด้านตรงข้ามของแผ่นทองคำเปลว
ด้วยการนับจำนวนการแวววาวต่อหน่วยเวลาในตำแหน่งต่างๆ บนหน้าจอ จึงเป็นไปได้ที่จะสร้างการกระจายตัวเชิงพื้นที่ของอนุภาคแอลฟาที่กระจัดกระจาย จำนวนอนุภาคแอลฟาจะลดลงอย่างรวดเร็วตามมุมการกระเจิงที่เพิ่มขึ้น
ภาพที่สังเกตบนหน้าจอนำไปสู่ข้อสรุปว่าอนุภาคอัลฟ่าส่วนใหญ่ทะลุผ่านแผ่นฟอยล์สีทองโดยไม่มีการเปลี่ยนแปลงทิศทางการเคลื่อนที่ที่เห็นได้ชัดเจน อย่างไรก็ตาม อนุภาคบางส่วนเบี่ยงเบนไปในมุมกว้างจากทิศทางเดิมของอนุภาคแอลฟา (ประมาณ 135โอ...150 โอ ) และยังถูกโยนกลับด้วยซ้ำ การศึกษาพบว่าเมื่ออนุภาคอัลฟาผ่านฟอยล์ ทุก ๆ 10,000 อนุภาคที่ตกกระทบ จะมีเพียงอนุภาคเดียวเท่านั้นที่ถูกเบี่ยงเบนด้วยมุมมากกว่า 10โอ จากทิศทางการเคลื่อนที่เดิม อนุภาคอัลฟาจำนวนมากเบี่ยงเบนไปจากทิศทางเดิมเช่นเดียวกับข้อยกเว้นที่หาได้ยาก
ความจริงที่ว่าอนุภาคแอลฟาจำนวนมากผ่านฟอยล์โดยไม่เบี่ยงเบนไปจากทิศทางการเคลื่อนที่ แสดงให้เห็นว่าอะตอมไม่ใช่ของแข็ง เนื่องจากมวลของอนุภาคอัลฟ่ามากกว่ามวลของอิเล็กตรอนเกือบ 8,000 เท่า อิเล็กตรอนที่รวมอยู่ในอะตอมของฟอยล์จึงไม่สามารถเปลี่ยนอนุภาคอัลฟ่าได้อย่างเห็นได้ชัด การกระเจิงของอนุภาคอัลฟ่าอาจเกิดจากอนุภาคที่มีประจุบวกของอะตอม - นิวเคลียสของอะตอม
IV. การเสริมกำลัง
การพิจารณาตัวอย่าง
วี- การสะท้อนกลับ
วันนี้คุณชอบบทเรียนของเราไหม..จำอะไรได้บ้าง?..
วี- D/Z ทำซ้ำ §7.1 เรียนรู้ §7.2
โครงสร้างอะตอมมีความซับซ้อน สิ่งนี้ได้รับการยืนยันจากการค้นพบปรากฏการณ์ต่างๆ เช่น อิเล็กตรอน รังสีเอกซ์ และกัมมันตภาพรังสี จากผลการวิจัยทางทฤษฎีและการทดลองต่างๆ มากมาย ก ทฤษฎีโครงสร้างอะตอม- เออร์เนสต์นักฟิสิกส์ชาวอังกฤษมีส่วนสนับสนุนที่สำคัญอย่างยิ่งต่อการสร้างทฤษฎีโครงสร้างอะตอม รัทเทอร์ฟอร์ด(พ.ศ. 2414 - 2480) ซึ่งทำการทดลองเพื่อศึกษาการผ่านของอนุภาคแอลฟาผ่านแผ่นโลหะบาง ๆ ที่เป็นทองคำและแพลทินัม
รัทเทอร์ฟอร์ดเสนอให้ตรวจสอบอะตอมของธาตุหนักในปี พ.ศ. 2449 ด้วยอนุภาคอัลฟาที่มีพลังงาน 4.05 MeV ซึ่งปล่อยออกมาจากนิวเคลียสของยูเรเนียมหรือเรเดียม ดังนั้นจึงเสนอให้ศึกษาการกระเจิง (การเปลี่ยนแปลงทิศทางการเคลื่อนที่) ของอนุภาคแอลฟาในสสาร
มวลของอนุภาคอัลฟ่ามีค่าประมาณ 8,000 เท่าของมวลอิเล็กตรอน ประจุบวกจะมีขนาดเท่ากับสองเท่าของประจุของอิเล็กตรอน 2e ความเร็วของอนุภาคแอลฟาคือ 1/15 ของความเร็วแสงหรือ 2 * 10 7 m/s อนุภาคอัลฟ่าเป็นอะตอมฮีเลียมที่แตกตัวเป็นไอออนอย่างสมบูรณ์
แผนภาพอย่างง่ายของการทดลองของรัทเทอร์ฟอร์ดแสดงไว้ในรูปที่ 1 1.1. อนุภาคอัลฟ่าถูกปล่อยออกมาโดยแหล่งกัมมันตภาพรังสี 1 วางอยู่ภายในกระบอกตะกั่ว 2 ที่มีช่องแคบ 3 ลำแสงอนุภาคอัลฟ่าแคบจากช่องนั้นตกลงบนฟอยล์ 4 ที่ทำจากวัสดุภายใต้การศึกษา ตั้งฉากกับพื้นผิวของฟอยล์ จากกระบอกตะกั่ว อนุภาคอัลฟ่าผ่านไปผ่านช่องเท่านั้น และส่วนที่เหลือถูกดูดซับโดยตะกั่ว อนุภาคอัลฟ่าที่ผ่านฟอยล์และกระจัดกระจายตกลงไปบนตะแกรงโปร่งแสง 5 ซึ่งถูกเคลือบด้วยสารเรืองแสง (ซิงค์ซัลเฟต) สารนี้สามารถเรืองแสงได้เมื่ออนุภาคอัลฟ่ากระทบกับมัน การชนกันของอนุภาคแต่ละอนุภาคกับหน้าจอมีแสงวาบเข้ามาด้วย แฟลชตัวนี้มีชื่อว่า แวววาว(จากภาษาละติน แวววาว - ประกายแสงวาบระยะสั้น) ด้านหลังหน้าจอมีกล้องจุลทรรศน์ 6 ตัว เพื่อป้องกันการกระจายตัวของอนุภาคอัลฟ่าในอากาศเพิ่มเติม อุปกรณ์ทั้งหมดจึงถูกวางในภาชนะที่มีสุญญากาศเพียงพอ
ข้าว. 1.1. รูปแบบการทดลองของรัทเทอร์ฟอร์ดอย่างง่าย
เมื่อไม่มีฟอยล์ วงกลมสว่างก็ปรากฏขึ้นบนหน้าจอ ซึ่งประกอบด้วยแสงแวววาวที่เกิดจากลำแสงอนุภาคอัลฟ่าบางๆ แต่เมื่อวางแผ่นฟอยล์สีทองบาง ๆ ที่มีความหนาประมาณ 0.1 μm (ไมครอน) ในเส้นทางของอนุภาคอัลฟ่า ภาพที่สังเกตได้บนหน้าจอก็เปลี่ยนไปอย่างมาก กล่าวคือ แสงวาบแต่ละครั้งไม่เพียงปรากฏอยู่นอกวงกลมก่อนหน้าเท่านั้น แต่ยังอาจปรากฏขึ้นอีกด้วย สังเกตจากด้านตรงข้ามของแผ่นทองคำเปลว
ด้วยการนับจำนวนการเรืองแสงวาบต่อหน่วยเวลาในตำแหน่งต่างๆ บนหน้าจอ จึงเป็นไปได้ที่จะสร้างการกระจายตัวของอนุภาคแอลฟาที่กระจัดกระจายในอวกาศได้ จำนวนอนุภาคแอลฟาจะลดลงอย่างรวดเร็วตามมุมการกระเจิงที่เพิ่มขึ้น
ภาพที่สังเกตบนหน้าจอนำไปสู่ข้อสรุปว่าอนุภาคอัลฟาส่วนใหญ่ผ่านแผ่นฟอยล์สีทองโดยไม่มีการเปลี่ยนแปลงทิศทางการเคลื่อนที่ที่เห็นได้ชัดเจน อย่างไรก็ตาม อนุภาคบางส่วนเบี่ยงเบนไปในมุมกว้างจากทิศทางเดิมของอนุภาคแอลฟา (ประมาณ 135 o ... 150 o) และยังถูกโยนกลับไปด้วยซ้ำ การวิจัยแสดงให้เห็นว่าเมื่ออนุภาคอัลฟ่าผ่านฟอยล์ ทุกๆ 10,000 อนุภาคที่ตกลงมา จะมีเพียงอนุภาคเดียวเท่านั้นที่เบี่ยงเบนมุมมากกว่า 10° จากทิศทางการเคลื่อนที่เดิม อนุภาคอัลฟาจำนวนมากเบี่ยงเบนไปจากทิศทางเดิมเช่นเดียวกับข้อยกเว้นที่หาได้ยาก
ความจริงที่ว่าอนุภาคแอลฟาจำนวนมากผ่านฟอยล์โดยไม่เบี่ยงเบนไปจากทิศทางการเคลื่อนที่ แสดงให้เห็นว่าอะตอมไม่ได้ก่อตัวอย่างต่อเนื่อง เนื่องจากมวลของอนุภาคอัลฟ่ามากกว่ามวลของอิเล็กตรอนเกือบ 8,000 เท่า อิเล็กตรอนที่เป็นส่วนหนึ่งของอะตอมฟอยล์จึงไม่สามารถเปลี่ยนวิถีการเคลื่อนที่ของอนุภาคแอลฟาได้อย่างเห็นได้ชัด การกระเจิงของอนุภาคอัลฟ่าอาจเกิดจากอนุภาคที่มีประจุบวกของอะตอม - นิวเคลียสของอะตอม
นิวเคลียสของอะตอม- นี่คือวัตถุขนาดเล็กที่มีมวลเกือบทั้งหมดและประจุบวกเกือบทั้งหมดของอะตอมกระจุกตัวอยู่
ยิ่งอนุภาคแอลฟาเข้าใกล้นิวเคลียสมากเท่าใด แรงปฏิกิริยาทางไฟฟ้าก็จะยิ่งมากขึ้นเท่านั้น และยิ่งมุมที่อนุภาคเบี่ยงเบนไปก็จะยิ่งมากขึ้นเท่านั้น ที่ระยะห่างจากนิวเคลียสเพียงเล็กน้อย อนุภาคอัลฟาที่มีประจุบวกจะพบกับแรงผลัก F อย่างมีนัยสำคัญจากนิวเคลียส ซึ่งถูกกำหนดโดยกฎของคูลอมบ์:
| ฉ= |
โดยที่ r คือระยะห่างจากนิวเคลียสถึงอนุภาคแอลฟา
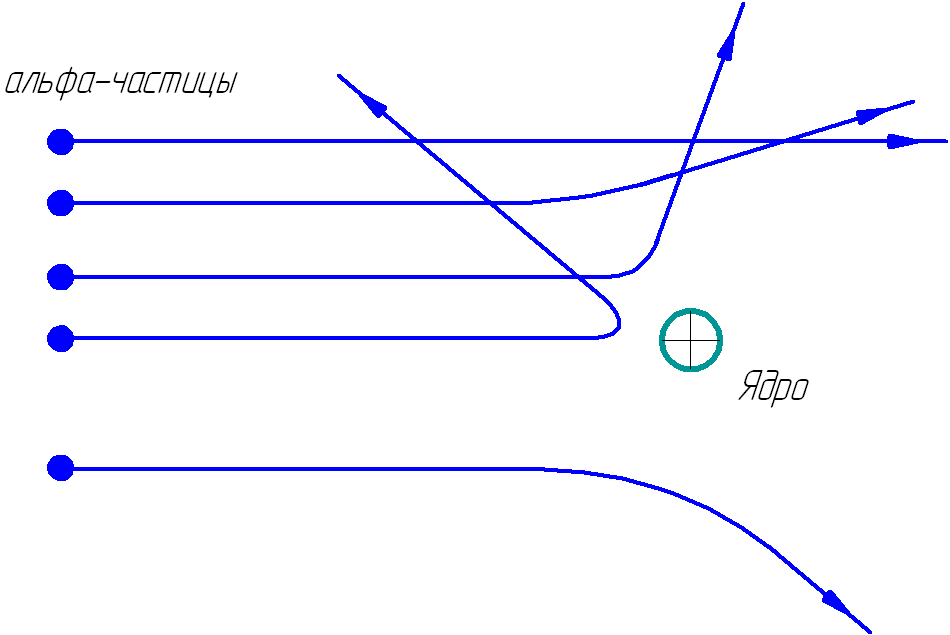
ε 0 – ค่าคงที่ทางไฟฟ้าในหน่วย SI;
p – จำนวนโปรตอนในนิวเคลียส e = 1.6*10-19 C – ค่าสัมบูรณ์ของประจุไฟฟ้าเบื้องต้น (ประจุอิเล็กตรอน) 2e – ประจุอนุภาคอัลฟ่า รูปที่ 1.2 แสดงวิถีการเคลื่อนที่ของอนุภาคแอลฟาที่บินไปในระยะห่างต่างๆ จากนิวเคลียสรัทเทอร์ฟอร์ดสามารถแนะนำสูตรที่เชื่อมโยงจำนวนอนุภาคอัลฟาที่กระจัดกระจายในมุมหนึ่งกับพลังงานของอนุภาคอัลฟ่าและโปรตอน p ในนิวเคลียสของอะตอม การตรวจสอบการทดลองของสูตรยืนยันความถูกต้องและแสดงให้เห็นว่าจำนวนโปรตอนในนิวเคลียสเท่ากับจำนวนอิเล็กตรอนในอะตอม Z และถูกกำหนดโดยเลขอะตอม
องค์ประกอบทางเคมี
(นั่นคือหมายเลขซีเรียลขององค์ประกอบใน
ด้วยการนับจำนวนอนุภาคแอลฟาที่กระจัดกระจายในมุมต่างๆ รัทเทอร์ฟอร์ดจึงสามารถประมาณขนาดเชิงเส้นของนิวเคลียสได้ เพื่อให้นิวเคลียสเชิงบวกส่งอนุภาคแอลฟากลับไป พลังงานศักย์ของการผลักกันของไฟฟ้าสถิต (คูลอมบ์) ที่ขอบเขตของนิวเคลียสของอะตอมจะต้องเท่ากับพลังงานจลน์ของอนุภาคแอลฟา:
| = |
ปรากฎว่าแกนมีเส้นผ่านศูนย์กลาง:
D i = 10 -13 ...10 -12 ซม. = 10 -15 ...10 -14 ม.
เส้นผ่านศูนย์กลางเชิงเส้นของอะตอมเอง:
D a = 10 -8 ซม. = 10 -10 ม
แบบจำลองดาวเคราะห์ของอะตอม
หลังจากวิเคราะห์การทดลองมากมาย รัทเทอร์ฟอร์ดเสนอในปี พ.ศ. 2454 แบบจำลองอะตอมของดาวเคราะห์ (แบบจำลองนิวเคลียร์อะตอม).
ตามแบบจำลองนี้ ที่ศูนย์กลางของอะตอมจะมีนิวเคลียสที่มีประจุบวก ซึ่งมีมวลเกือบทั้งหมดของอะตอมมีความเข้มข้น อิเล็กตรอนที่มีประจุลบโคจรรอบนิวเคลียส อิเล็กตรอนเคลื่อนที่ไปรอบนิวเคลียสในระยะทางที่ค่อนข้างไกล เหมือนกับดาวเคราะห์ที่โคจรรอบดวงอาทิตย์ จากการรวมตัวกันของอิเล็กตรอนเหล่านี้จะเกิดขึ้น เปลือกอิเล็กตรอน หรือ เมฆอิเล็กตรอน.
อะตอมโดยรวมมีความเป็นกลาง ดังนั้น ค่าสัมบูรณ์ของประจุลบรวมของอิเล็กตรอนจึงเท่ากับประจุบวกของนิวเคลียส: จำนวน Z*e ของโปรตอนในนิวเคลียสเท่ากับจำนวนอิเล็กตรอนในนิวเคลียส คลาวด์อิเล็กทรอนิกส์และเกิดขึ้นพร้อมกับเลขลำดับ (เลขอะตอม) Z ของอะตอมขององค์ประกอบทางเคมีที่กำหนดในระบบธาตุของ D.I.
ตัวอย่างเช่น อะตอมไฮโดรเจนมีเลขอะตอม Z = 1 ดังนั้น อะตอมไฮโดรเจนจึงประกอบด้วยนิวเคลียสบวกซึ่งมีประจุเท่ากับค่าสัมบูรณ์ของประจุอิเล็กตรอน อิเล็กตรอนตัวหนึ่งหมุนรอบนิวเคลียส นิวเคลียสของอะตอมไฮโดรเจนเรียกว่าโปรตอน อะตอมลิเธียมมีเลขอะตอม Z = 3 ดังนั้นอิเล็กตรอน 3 ตัวหมุนรอบนิวเคลียสของอะตอมลิเธียม
โปรแกรมคอมพิวเตอร์จำลองการทดลองคลาสสิกของรัทเทอร์ฟอร์ดในการตรวจอะตอมด้วยอนุภาคอัลฟา โดยอิงตามผลลัพธ์ที่ได้เสนอไว้ แบบจำลองดาวเคราะห์ของโครงสร้างอะตอม .
การทดลองวิจัยโดยตรงครั้งแรก โครงสร้างภายในอะตอมดำเนินการโดยอี. รัทเทอร์ฟอร์ดและผู้ร่วมงานของเขาอี. มาร์สเดนและเอช. ไกเกอร์ในปี พ.ศ. 2452-2454
รัทเทอร์ฟอร์ดเสนอให้ใช้การตรวจวัดอะตอมมิกโดยใช้อนุภาค α ซึ่งเกิดขึ้นระหว่างการสลายตัวของกัมมันตภาพรังสีของเรเดียมและองค์ประกอบอื่นๆ มวลของอนุภาคแอลฟามีค่าประมาณ 7300 เท่าของมวลอิเล็กตรอน และประจุบวกจะเท่ากับ 2 เท่าของประจุเบื้องต้น ในการทดลองของเขา รัทเทอร์ฟอร์ดใช้อนุภาคแอลฟาที่มีพลังงานจลน์ประมาณ 5 MeV (ความเร็วของอนุภาคดังกล่าวสูงมาก - ประมาณ 107 m/s แต่ก็ยังน้อยกว่าความเร็วแสงอย่างมีนัยสำคัญ)
อนุภาค α คืออะตอมฮีเลียมที่แตกตัวเป็นไอออนอย่างสมบูรณ์ พวกมันถูกค้นพบโดยรัทเทอร์ฟอร์ดในปี พ.ศ. 2442 ขณะศึกษาปรากฏการณ์กัมมันตภาพรังสี รัทเทอร์ฟอร์ดระดมยิงอะตอมของธาตุหนัก (ทอง เงิน ทองแดง ฯลฯ) ด้วยอนุภาคเหล่านี้ อิเล็กตรอนที่ประกอบเป็นอะตอมเนื่องจากมีมวลต่ำ จึงไม่สามารถเปลี่ยนวิถีการเคลื่อนที่ของอนุภาค α ได้อย่างเห็นได้ชัด การกระเจิงซึ่งก็คือการเปลี่ยนทิศทางการเคลื่อนที่ของอนุภาค α สามารถเกิดขึ้นได้จากส่วนที่หนักและมีประจุบวกของอะตอมเท่านั้น แผนภาพการทดลองของรัทเทอร์ฟอร์ดแสดงไว้ในรูปที่ 1 1.
จากแหล่งกำเนิดกัมมันตภาพรังสีที่อยู่ในภาชนะตะกั่ว อนุภาคอัลฟ่าถูกส่งไปยังฟอยล์โลหะบางๆ อนุภาคที่กระจัดกระจายตกลงบนตะแกรงที่ปกคลุมไปด้วยชั้นของผลึกซิงค์ซัลไฟด์ ซึ่งสามารถเรืองแสงได้เมื่อโดนอนุภาคที่มีประจุเร็ว สังเกตการแวววาว (กะพริบ) บนหน้าจอด้วยตาโดยใช้กล้องจุลทรรศน์ การสังเกตอนุภาค α ที่กระจัดกระจายในการทดลองของรัทเธอร์ฟอร์ดสามารถดำเนินการได้ในมุมที่ต่างกัน φ ไปยังทิศทางเดิมของลำแสง พบว่าอนุภาค α ส่วนใหญ่ทะลุผ่านชั้นโลหะบางๆ โดยมีการโก่งตัวเพียงเล็กน้อยหรือไม่มีเลย อย่างไรก็ตาม ชิ้นส่วนเล็กๆ ของอนุภาคจะเบี่ยงเบนไปในมุมที่มีนัยสำคัญเกิน 30° อนุภาคอัลฟาที่หายากมาก (ประมาณหนึ่งในหมื่น) ถูกเบี่ยงเบนไปในมุมใกล้ 180°
การทดลองของรัทเทอร์ฟอร์ดและเพื่อนร่วมงานของเขานำไปสู่ข้อสรุปว่าที่ใจกลางอะตอมจะมีนิวเคลียสที่มีประจุบวกหนาแน่น ซึ่งมีเส้นผ่านศูนย์กลางไม่เกิน 10 –14 –10 –15 เมตร นิวเคลียสนี้ครอบครองเพียง 10 –12 นิวเคลียส ปริมาตรรวมของอะตอมแต่ประกอบด้วย ทั้งหมดประจุบวกและอย่างน้อย 99.95% ของมวล ประจุของนิวเคลียสจะต้องเท่ากับประจุรวมของอิเล็กตรอนทั้งหมดที่ประกอบเป็นอะตอม
จากแนวคิดคลาสสิกเกี่ยวกับการเคลื่อนที่ของอนุภาคขนาดเล็ก Rutherford เสนอ แบบจำลองดาวเคราะห์ของอะตอม - ตามแบบจำลองนี้ ที่ศูนย์กลางของอะตอมจะมีนิวเคลียสที่มีประจุบวก ซึ่งมีมวลเกือบทั้งหมดของอะตอมมีความเข้มข้น อะตอมโดยรวมมีความเป็นกลาง อิเล็กตรอนหมุนรอบนิวเคลียสเช่นเดียวกับดาวเคราะห์ ภายใต้อิทธิพลของแรงคูลอมบ์จากนิวเคลียส อิเล็กตรอนไม่สามารถอยู่นิ่งได้ เนื่องจากพวกมันจะตกเข้าสู่นิวเคลียส
แบบจำลองดาวเคราะห์ของอะตอมที่รัทเธอร์ฟอร์ดเสนอถือเป็นก้าวสำคัญในการพัฒนาความรู้เกี่ยวกับโครงสร้างของอะตอม จำเป็นอย่างยิ่งที่จะต้องอธิบายการทดลองเกี่ยวกับการกระเจิงของอนุภาค α แต่กลับกลายเป็นว่าไม่สามารถอธิบายข้อเท็จจริงของการดำรงอยู่ของอะตอมได้ยาวนาน กล่าวคือ ความเสถียรของมัน ตามกฎหมายของไฟฟ้าไดนามิกแบบคลาสสิก ประจุที่เคลื่อนที่ด้วยความเร่งควรปล่อยคลื่นแม่เหล็กไฟฟ้าที่พาพลังงานออกไป ในช่วงเวลาสั้นๆ (ประมาณ 10–8 วินาที) อิเล็กตรอนทั้งหมดในอะตอมรัทเทอร์ฟอร์ดจะต้องสูญเสียพลังงานทั้งหมดและตกลงสู่นิวเคลียส ความจริงที่ว่าสิ่งนี้ไม่ได้เกิดขึ้นในสถานะเสถียรของอะตอมแสดงให้เห็นว่ากระบวนการภายในอะตอมไม่เป็นไปตามกฎคลาสสิก
ผู้ใช้มีโอกาส:
- สังเกตการกระจัดกระจายของอนุภาคบนแกนทองคำที่อยู่นิ่ง
- เปลี่ยนระยะการกระแทกและความเร็วเริ่มต้นของอนุภาค
- วัดมุมการกระเจิงของอนุภาค
- ศึกษาเส้นโค้งการกระเจิงเมื่อโจมตีนิวเคลียสของทองคำด้วยกระแสอนุภาคด้วยพลังงานที่กำหนดในโหมดอัตโนมัติ
อะตอมประกอบด้วยนิวเคลียสที่มีประจุบวกที่มีขนาดกะทัดรัดและมีมวลมาก และมีอิเล็กตรอนแสงที่มีประจุลบอยู่รอบๆ
เออร์เนสต์ รัทเธอร์ฟอร์ดเป็นนักวิทยาศาสตร์ที่มีเอกลักษณ์เฉพาะตัวในแง่ที่ว่าเขาได้ค้นพบสิ่งใหม่ๆ ที่สำคัญแล้ว หลังจากการรับ รางวัลโนเบล- ในปี 1911 เขาประสบความสำเร็จในการทดลองที่ไม่เพียงแต่ทำให้นักวิทยาศาสตร์สามารถมองลึกเข้าไปในอะตอมและรับข้อมูลเชิงลึกเกี่ยวกับโครงสร้างของมัน แต่ยังกลายเป็นแบบอย่างแห่งความสง่างามและความลึกของการออกแบบอีกด้วย
โดยใช้แหล่งธรรมชาติ รังสีกัมมันตภาพรังสีรัทเทอร์ฟอร์ดสร้างปืนใหญ่ที่สร้างกระแสอนุภาคที่พุ่งตรงและโฟกัส ปืนดังกล่าวเป็นกล่องตะกั่วที่มีช่องแคบ ภายในมีการวางสารกัมมันตภาพรังสีไว้ ด้วยเหตุนี้ อนุภาค (ในกรณีนี้คืออนุภาคอัลฟา ซึ่งประกอบด้วยโปรตอนสองตัวและนิวตรอนสองตัว) ที่ปล่อยออกมาจากสารกัมมันตภาพรังสีในทุกทิศทาง ยกเว้นอนุภาคหนึ่งถูกดูดซับโดยตะแกรงตะกั่ว และมีเพียงลำอนุภาคอัลฟาโดยตรงเท่านั้นที่ถูกปล่อยออกมาผ่านช่องนั้น . ไกลออกไปตามเส้นทางของลำแสงยังมีตะแกรงตะกั่วอีกหลายแห่งที่มีช่องแคบๆ ที่ตัดอนุภาคที่เบี่ยงเบนไปจากทิศทางที่กำหนดอย่างเคร่งครัด เป็นผลให้ลำแสงอนุภาคอัลฟ่าที่โฟกัสอย่างสมบูรณ์แบบบินไปยังเป้าหมาย และตัวเป้าหมายเองก็เป็นแผ่นฟอยล์สีทองบาง ๆ มันเป็นรังสีอัลฟ่าที่โจมตีเธอ หลังจากการชนกับอะตอมฟอยล์ อนุภาคอัลฟ่ายังคงเคลื่อนที่ต่อไปและชนแผ่นกรองเรืองแสงที่ติดตั้งอยู่ด้านหลังเป้าหมาย ซึ่งมีการบันทึกแสงวาบเมื่ออนุภาคอัลฟ่าชนเป้าหมาย จากนั้นผู้ทดลองสามารถตัดสินได้ว่าอนุภาคอัลฟ่าเบี่ยงเบนไปจากทิศทางในปริมาณเท่าใดและเท่าใด การเคลื่อนไหวเป็นเส้นตรงอันเป็นผลมาจากการชนกับอะตอมฟอยล์
มีการทดลองประเภทนี้มาก่อน แนวคิดหลักของพวกเขาคือการรวบรวมข้อมูลที่เพียงพอจากมุมโก่งตัวของอนุภาคเพื่อให้สามารถพูดบางสิ่งที่ชัดเจนเกี่ยวกับโครงสร้างของอะตอมได้ ในตอนต้นของศตวรรษที่ 20 นักวิทยาศาสตร์รู้อยู่แล้วว่าอะตอมประกอบด้วยอิเล็กตรอนที่มีประจุลบ อย่างไรก็ตาม แนวคิดที่มีอยู่ทั่วไปก็คือ อะตอมมีลักษณะคล้ายกริดละเอียดที่มีประจุบวกซึ่งเต็มไปด้วยอิเล็กตรอนลูกเกดที่มีประจุลบ แบบจำลองนี้เรียกว่า "แบบจำลองกริดลูกเกด" จากผลการทดลองดังกล่าว นักวิทยาศาสตร์สามารถเรียนรู้คุณสมบัติบางอย่างของอะตอม โดยเฉพาะอย่างยิ่ง การประมาณลำดับขนาดทางเรขาคณิตของพวกมัน
อย่างไรก็ตาม รัทเทอร์ฟอร์ดตั้งข้อสังเกตว่าไม่มีคนรุ่นก่อนๆ ของเขาคนใดที่พยายามทดสอบด้วยการทดลองว่าอนุภาคแอลฟาบางส่วนเบี่ยงเบนไปจากมุมที่กว้างมากหรือไม่ แบบจำลองตารางลูกเกดไม่อนุญาตให้มีองค์ประกอบโครงสร้างในอะตอมที่มีความหนาแน่นและหนักมากจนสามารถเบี่ยงเบนอนุภาคแอลฟาที่รวดเร็วในมุมที่มีนัยสำคัญ ดังนั้นจึงไม่มีใครสนใจที่จะทดสอบความเป็นไปได้นี้ รัทเทอร์ฟอร์ดขอให้นักเรียนคนหนึ่งของเขาติดตั้งอุปกรณ์ติดตั้งใหม่ในลักษณะที่สามารถสังเกตการกระเจิงของอนุภาคแอลฟาในมุมโก่งขนาดใหญ่ - เพียงเพื่อเคลียร์มโนธรรมของเขา และขจัดความเป็นไปได้นี้ออกไปโดยสิ้นเชิง เครื่องตรวจจับเป็นตะแกรงที่เคลือบด้วยโซเดียมซัลไฟด์ ซึ่งเป็นวัสดุที่ทำให้เกิดแสงวาบฟลูออเรสเซนต์เมื่ออนุภาคอัลฟากระทบกับมัน ลองนึกภาพความประหลาดใจที่ไม่เพียงแต่กับนักเรียนที่ทำการทดลองโดยตรงเท่านั้น แต่ยังรวมถึงตัว Rutherford เองด้วยเมื่อปรากฏว่าอนุภาคบางส่วนเบี่ยงเบนไปเป็นมุมสูงถึง 180°!
ภายในกรอบของแบบจำลองอะตอมที่สร้างขึ้น ไม่สามารถตีความผลลัพธ์ได้: ไม่มีอะไรในตารางลูกเกดที่สามารถสะท้อนอนุภาคอัลฟาที่ทรงพลัง เร็ว และหนักได้ รัทเทอร์ฟอร์ดถูกบังคับให้สรุปว่าในอะตอม มวลส่วนใหญ่มีความเข้มข้นอยู่ในอะตอมอันเหลือเชื่อ เรื่องหนาแน่นซึ่งอยู่ที่ใจกลางของอะตอม และอะตอมที่เหลือกลับกลายเป็นว่ามีความหนาแน่นน้อยกว่าที่คิดไว้มาก นอกจากนี้ยังเป็นไปตามพฤติกรรมของอนุภาคแอลฟาที่กระจัดกระจายซึ่งอยู่ในศูนย์กลางความหนาแน่นยิ่งยวดของอะตอม ซึ่งรัทเทอร์ฟอร์ดเรียกว่า แกนประจุไฟฟ้าบวกทั้งหมดของอะตอมก็มีความเข้มข้นเช่นกัน เนื่องจากมีเพียงแรงผลักไฟฟ้าเท่านั้นที่สามารถทำให้เกิดการกระเจิงของอนุภาคในมุมที่มากกว่า 90°
หลายปีต่อมา รัทเทอร์ฟอร์ดชอบใช้การเปรียบเทียบนี้เกี่ยวกับการค้นพบของเขา ในประเทศหนึ่งทางตอนใต้ของทวีปแอฟริกา เจ้าหน้าที่ศุลกากรได้รับคำเตือนว่าอาวุธจำนวนมากกำลังจะถูกลักลอบขนเข้าประเทศเพื่อกลุ่มกบฏ และอาวุธเหล่านั้นจะถูกซ่อนอยู่ในกองฝ้าย และบัดนี้ หลังจากขนถ่ายลงแล้ว เจ้าหน้าที่ศุลกากรก็หันหน้าไปทางโกดังที่เต็มไปด้วยกองฝ้าย เขาจะทราบได้อย่างไรว่าก้อนใดมีปืนไรเฟิล เจ้าหน้าที่ศุลกากรแก้ไขปัญหาได้ง่ายๆ: เขาเริ่มยิงไปที่มัดฟาง และหากกระสุนแฉลบจากมัดใดๆ เขาก็ระบุได้ว่ามัดมัดนั้นเป็นอาวุธที่ลักลอบนำเข้าตามสัญลักษณ์นี้ ดังนั้น Rutherford เมื่อเห็นว่าอนุภาคอัลฟาสะท้อนกลับจากฟอยล์สีทองได้อย่างไร ก็พบว่ามีโครงสร้างที่หนาแน่นกว่ามากซ่อนอยู่ภายในอะตอมมากกว่าที่คาดไว้
รูปภาพของอะตอมที่ Rutherford วาดโดยอิงจากผลการทดลองของเขาเป็นที่รู้จักกันดีสำหรับเราในปัจจุบัน อะตอมประกอบด้วยนิวเคลียสที่มีความหนาแน่นสูงมากซึ่งมีประจุบวกและมีอิเล็กตรอนแสงที่มีประจุลบอยู่รอบๆ ต่อมา นักวิทยาศาสตร์ได้ให้พื้นฐานทางทฤษฎีที่เชื่อถือได้สำหรับภาพนี้ ( ซม.บอร์ อะตอม) แต่ทั้งหมดเริ่มต้นด้วยการทดลองง่ายๆ กับตัวอย่างเล็กๆ ของวัสดุกัมมันตภาพรังสีและแผ่นฟอยล์สีทอง
ดูเพิ่มเติมที่:
เออร์เนสต์ รัทเทอร์ฟอร์ด บารอนรัทเทอร์ฟอร์ดแห่งเนลสันที่ 1 พ.ศ. 2414-2480
นักฟิสิกส์ชาวนิวซีแลนด์ เกิดในเนลสัน ลูกชายของชาวนาช่างฝีมือ ได้รับทุนไปศึกษาต่อที่มหาวิทยาลัยเคมบริดจ์ ประเทศอังกฤษ หลังจากสำเร็จการศึกษา เขาได้รับการแต่งตั้งให้เป็นมหาวิทยาลัย McGill ของแคนาดา ซึ่งเขาได้ก่อตั้งกฎพื้นฐานของปรากฏการณ์กัมมันตภาพรังสีร่วมกับ Frederick Soddy (พ.ศ. 2420-2509) ซึ่งเขาได้รับรางวัลโนเบลสาขาเคมีในปี พ.ศ. 2451 ในไม่ช้านักวิทยาศาสตร์ก็ย้ายไปที่มหาวิทยาลัยแมนเชสเตอร์ซึ่งภายใต้การนำของเขา Hans Geiger (พ.ศ. 2425-2488) ได้ประดิษฐ์เครื่องนับ Geiger อันโด่งดังของเขาเริ่มค้นคว้าโครงสร้างของอะตอมและในปี พ.ศ. 2454 ก็ได้ค้นพบการมีอยู่ของนิวเคลียสของอะตอม ในช่วงสงครามโลกครั้งที่หนึ่ง เขามีส่วนร่วมในการพัฒนาโซนาร์ (เรดาร์อะคูสติก) เพื่อตรวจจับเรือดำน้ำของศัตรู ในปี พ.ศ. 2462 เขาได้รับแต่งตั้งเป็นศาสตราจารย์ด้านฟิสิกส์และเป็นผู้อำนวยการห้องทดลองคาเวนดิชแห่งมหาวิทยาลัยเคมบริดจ์ และในปีเดียวกันนั้นก็ได้ค้นพบการสลายตัวของนิวเคลียสอันเป็นผลมาจากการทิ้งระเบิดด้วยอนุภาคหนัก พลังงานสูง- รัทเทอร์ฟอร์ดยังคงอยู่ในตำแหน่งนี้ไปจนวาระสุดท้ายของชีวิต ขณะเดียวกันก็เป็นประธานาธิบดีของราชวงศ์เป็นเวลาหลายปี สังคมวิทยาศาสตร์- เขาถูกฝังไว้ที่เวสต์มินสเตอร์แอบบีย์ ถัดจากนิวตัน ดาร์วิน และฟาราเดย์
ข้อสรุปจากการทดลองการกระเจิงอนุภาคแอลฟาของรัทเทอร์ฟอร์ด: 1. มีนิวเคลียสของอะตอม กล่าวคือ วัตถุขนาดเล็กที่มีมวลเกือบทั้งหมดของอะตอมและประจุบวกทั้งหมดกระจุกตัวอยู่ 2. มวลเกือบทั้งหมดของอะตอมกระจุกตัวอยู่ในนิวเคลียส 3. อนุภาคเชิงลบ - อิเล็กตรอน - หมุนรอบนิวเคลียสในวงโคจรปิด 4. ประจุลบของอิเล็กตรอนทั้งหมดจะกระจายไปทั่วทั้งปริมาตรของอะตอม แบบจำลองนิวเคลียร์ของอะตอม:
สไลด์ 9จากการนำเสนอ “การทดลองของรัทเทอร์ฟอร์ด แบบจำลองอะตอม”- ขนาดของไฟล์เก็บถาวรพร้อมการนำเสนอคือ 174 KBฟิสิกส์ ชั้นประถมศึกษาปีที่ 9
สรุปการนำเสนออื่น ๆ“โครงสร้างของอะตอมของธาตุ” - ผู้ค้นพบปรากฏการณ์กัมมันตภาพรังสี โครงสร้าง. อะตอมคือ "แบ่งแยกไม่ได้" รัทเทอร์ฟอร์ดทำการทดลองหลายครั้งเพื่อศึกษาโครงสร้างและองค์ประกอบของอะตอม ทอมสันเสนอแบบจำลองโครงสร้างของอะตอมรุ่นแรกๆ ในปี พ.ศ. 2446 Henri Becquerel ค้นพบปรากฏการณ์กัมมันตภาพรังสี อนุภาคทำให้เกิดแสงวาบบนหน้าจอ สองเหตุการณ์ในช่วงปลายศตวรรษที่ 19 นำไปสู่แนวคิดเรื่องโครงสร้างอะตอมที่ซับซ้อน โครงสร้างของอะตอม แบบจำลองดาวเคราะห์ (นิวเคลียร์)
"ห้องคลาวด์" - วัตถุประสงค์ของอุปกรณ์ หลักการของหุ่นยนต์ การปรับปรุง. ความจุ. ผู้ประดิษฐ์อุปกรณ์ ความหมาย. กล้อง. วิลสัน. ห้องวิลสัน. อุปกรณ์.
“ความปลอดภัยด้านพลังงานนิวเคลียร์” - จากประวัติศาสตร์ พลังงานนิวเคลียร์- ปฏิกิริยาการสลายตัวของนิวเคลียสยูเรเนียม แผนภาพแสดงการทำงานของเครื่องปฏิกรณ์นิวเคลียร์ที่กำลังเดือด ความปลอดภัย. แผนผังของเครื่องปฏิกรณ์นิวเคลียร์ที่กำลังเดือด โรงไฟฟ้านิวเคลียร์มีความสามารถในการผลิตพลังงานมากขึ้น โรงไฟฟ้านิวเคลียร์ อันตรายจากพลังงานนิวเคลียร์ โรงไฟฟ้านิวเคลียร์บนแผนที่ของรัสเซีย เครื่องปฏิกรณ์นิวเคลียร์- พลังงานนิวเคลียร์ ฟิวชั่น- ประโยชน์และโทษของพลังงานนิวเคลียร์ เรือตัดน้ำแข็งนิวเคลียร์
“ฟิสิกส์ “การเคลื่อนไหว”” - ปฏิสัมพันธ์ของร่างกาย กลศาสตร์. กฎการอนุรักษ์ในกลศาสตร์ โครงสร้างของอะตอม ความเฉื่อยและมวลของร่างกาย ความเร็วที่ การเคลื่อนไหวที่ไม่สม่ำเสมอ- พิกัดเปลี่ยนแปลงอย่างไร เคลื่อนที่เป็นเส้นตรง การเคลื่อนที่ด้วยความเร่งสม่ำเสมอ- พื้นฐานของไดนามิก งานแห่งกำลัง. กฎข้อที่ 2 ของนิวตัน การล้มของร่างกายอย่างอิสระ พื้นฐานของฟิสิกส์ ศึกษาคุณสมบัติของสสาร เวกเตอร์ กฎข้อที่ 3 ของนิวตัน ระยะเวลาและความถี่ของการไหลเวียน การเร่งความเร็ว ฟิสิกส์เป็นวิทยาศาสตร์ที่แน่นอน
“การแกว่งของลูกตุ้มทางคณิตศาสตร์” - แผนการสอน การใช้งานจริงการสั่นของลูกตุ้ม กาลิเลโอ กาลิเลอี (ค.ศ. 1564-1642) ฮอยเกนส์ คริสเตียน (1629 – 1695) ร่างกายใดก็ตามสามารถเคลื่อนไหวแบบแกว่งไปมาได้ การทดลองทำเป็นวงกลมแคบๆ ภาพประกอบ การสั่นสะเทือนทางกลโดยใช้ตัวอย่างลูกตุ้มฟูโกต์ อาคารเก่าของมหาวิทยาลัยปิซา ลูกตุ้มจริงถือได้ว่าเป็นคณิตศาสตร์หากความยาวของด้ายมากกว่าขนาดของลำตัวที่แขวนอยู่มาก
“ First Cosmic Velocity” - แก้ปัญหา ความเร่งของการตกอย่างอิสระ ความเร็วที่ต้องมอบให้กับวัตถุจึงจะกลายเป็นดาวเทียม ความรู้เบื้องต้นเกี่ยวกับดาวเทียมประดิษฐ์ ความเร็วหลบหนีครั้งแรก เงื่อนไขที่ร่างกายกลายเป็นปัญญาประดิษฐ์ ดาวเทียมประดิษฐ์โลก. กำหนดความเร็วหนีแรกสำหรับการปล่อยดาวเทียม แก้ไขปัญหา. การปฏิวัติของดาวเคราะห์รอบดวงอาทิตย์
บทความที่เกี่ยวข้อง
-
การตั้งถิ่นฐานของทหาร Pushkin เกี่ยวกับ Arakcheevo
Alexey Andreevich Arakcheev (2312-2377) - รัฐบุรุษและผู้นำทางทหารของรัสเซียนับ (2342) ปืนใหญ่ (2350) เขามาจากตระกูลขุนนางของ Arakcheevs เขามีชื่อเสียงโด่งดังภายใต้การนำของพอลที่ 1 และมีส่วนช่วยในกองทัพ...
-
การทดลองทางกายภาพง่ายๆ ที่บ้าน
สามารถใช้ในบทเรียนฟิสิกส์ในขั้นตอนการกำหนดเป้าหมายและวัตถุประสงค์ของบทเรียน การสร้างสถานการณ์ปัญหาเมื่อศึกษาหัวข้อใหม่ การใช้ความรู้ใหม่เมื่อรวบรวม นักเรียนสามารถใช้การนำเสนอ “การทดลองเพื่อความบันเทิง” เพื่อ...
-
การสังเคราะห์กลไกลูกเบี้ยวแบบไดนามิก ตัวอย่างกฎการเคลื่อนที่แบบไซน์ซอยด์ของกลไกลูกเบี้ยว
กลไกลูกเบี้ยวเป็นกลไกที่มีคู่จลนศาสตร์ที่สูงกว่า ซึ่งมีความสามารถในการรับประกันว่าการเชื่อมต่อเอาท์พุตยังคงอยู่ และโครงสร้างประกอบด้วยอย่างน้อยหนึ่งลิงค์ที่มีพื้นผิวการทำงานที่มีความโค้งแปรผัน กลไกลูกเบี้ยว...
-
สงครามยังไม่เริ่มแสดงทั้งหมดพอดคาสต์ Glagolev FM
บทละครของ Semyon Alexandrovsky ที่สร้างจากบทละครของ Mikhail Durnenkov เรื่อง "The War Has not Started Yet" จัดแสดงที่โรงละคร Praktika อัลลา เชนเดอโรวา รายงาน ในช่วงสองสัปดาห์ที่ผ่านมา นี่คือการฉายรอบปฐมทัศน์ที่มอสโกครั้งที่สองโดยอิงจากข้อความของ Mikhail Durnenkov....
-
การนำเสนอในหัวข้อ "ห้องระเบียบวิธีใน dhow"
- การตกแต่งสำนักงานในสถาบันการศึกษาก่อนวัยเรียน การป้องกันโครงการ "การตกแต่งสำนักงานปีใหม่" สำหรับปีสากลแห่งการละคร ในเดือนมกราคม A. Barto Shadow อุปกรณ์ประกอบฉากโรงละคร: 1. หน้าจอขนาดใหญ่ (แผ่นบนแท่งโลหะ) 2. โคมไฟสำหรับ ช่างแต่งหน้า...
-
วันที่รัชสมัยของ Olga ใน Rus
หลังจากการสังหารเจ้าชายอิกอร์ ชาว Drevlyans ตัดสินใจว่าต่อจากนี้ไปเผ่าของพวกเขาจะเป็นอิสระ และพวกเขาไม่ต้องแสดงความเคารพต่อเคียฟมาตุส ยิ่งไปกว่านั้น เจ้าชาย Mal ของพวกเขายังพยายามแต่งงานกับ Olga ดังนั้นเขาจึงต้องการยึดบัลลังก์ของเคียฟและเพียงลำพัง...
