Элемент рассеивания а частиц опыт. Атомная физика. Опыт Резерфорда по рассеянию альфа-частиц. Опыты Резерфорда: ядерная модель атома
Урок физики в 11 классе
Тема:
"Опыт Резерфорда по рассеиванию альфа – частиц"
Цели и задачи урока:
Образовательные:
Разъяснить механизм опытов Резерфорда
Воспитательные:
развивать познавательную самостоятельность учащихся;
способствовать их нравственному и эстетическому воспитанию.
Развивающие:
развивать умения выделять главное, существенное, сравнивать изучаемые факты, логически излагать мысли.
Ход урока:
I .Орг. момент.
Встань ровно рядом со своей партой и приведи себя в порядок. Поздоровайся с учителем. Затем тихо сядь на своё место и соблюдай порядок в классе.
Постановка темы и цели урока.
II. Повторение
Линейчатые спектры
1.Что означает слово атом?2.Кто из ученых открыл закон периодической повторяемости свойств химических элементов?
3.Является ли атом не делимым?
4.Что происходит с разряженными газами при нагревании до высокой температуры?
5.Как называются разноцветные линии, разделенные темными промежутками?
6.Что присуще каждому газу?
7.Спектр какого газа является самым простым?
8.Спектр какого газа состоит из 4 линий?
9.Кто из ученых подобрал формулу спектральных линий для видимой области?
10.Чья теория позволила соединить формулы видимой, ультрафиолетовой и инфракрасной области в одну общую формулу?
Физминутка по видеоролику.
III . Новый материал
§ 7.2. Опыт Резерфорда по рассеиванию альфа – частиц.
Изучая рассеяние альфа-частиц при прохождении через золотую фольгу, Эрнест Резерфорд пришел к выводу, что весь положительный заряд атомов сосредоточен в их центре в очень массивном и компактном ядре. А отрицательно заряженные частицы (электроны) обращаются вокруг этого ядра.

Эта модель коренным образом отличалась от широко распространенной в то время модели атома Томсона.

Джозеф Джон Томсон предложил модель атома в виде пудинга (пирога), в котором положительный заряд равномерно заполнял весь объем атома, а электроны были вкраплены в него.

Несколько позже модель Резерфорда получила название планетарной модели атома (она действительно похожа на Солнечную систему: тяжелое ядро - Солнце, а обращающиеся вокруг него электроны - планеты).
В 1912 г. Э.Резерфорд и его сотрудники поставили опыт по рассеянию альфа-частиц в веществе.

Схема опытов Резерфорда.
В отсутствие фольги на экране возникал светлый кружок, состоящий из сцинтилляций, вызванных тонким пучком альфа-частиц. Но когда на пути движения альфа-частиц помещали тонкую золотую фольгу толщиной примерно 0,1 мк (микрон), то наблюдаемая на экране картинка сильно менялась: отдельные вспышки появлялись не только за пределами прежнего кружка, но их можно было даже наблюдать с противоположной стороны золотой фольги.
Подсчитывая число сцинтилляций в единицу времени в разных местах экрана, можно установить распределение в пространстве рассеянных альфа-частиц. Число альфа-частиц быстро убывает с увеличением угла рассеяния.
Наблюдаемая на экране картина позволила заключить, что большинство альфа-частиц проходит сквозь золотую фольгу без заметного изменения направления их движения. Однако некоторые частицы отклонялись на большие углы от первоначального направления альфа-частиц (порядка 135 о …150 о ) и даже отбрасывались назад. Исследования показали, что при прохождении альфа-частиц сквозь фольгу примерно на каждые 10000 падающих частиц только одна отклоняется на угол более 10 о от первоначального направления движения. Лишь в виде редкого исключения одна из огромного числа альфа-частиц отклоняется от своего первоначального направления.
Тот факт, что многие альфа-частицы проходили сквозь фольгу, не отклоняясь от своего направления движения, говорит о том, что атом не является сплошным образованием. Так как масса альфа-частицы почти в 8000 раз превосходит массу электрона, то электроны, входящие в состав атомов фольги, не могут заметно изменить альфа-частиц. Рассеяние альфа-частиц может вызывать положительно заряженная частица атома – атомное ядро.
IV .Закрепление
Рассмотрение примеров.
V
. Рефлексия
Понравился ли Вам наш сегодняшний урок?.. Что запомнилось?..
VI . Д/З повторить§7.1, учить §7.2
Строение атома является сложным. Это подтверждают открытия таких явлений, как электрон, рентгеновские лучи и радиоактивность. В результате теоретических исследований и многочисленных опытов была построена теория строения атома . Особенно важный вклад в создание теории строения атома внёс английский физик Эрнест Резерфорд (1871 – 1937), который проводил опыты по изучению прохождения альфа-частиц через тонкие металлические пластины золота и платины.
Резерфорд в 1906 году предложил провести зондирование атомов тяжёлых элементов альфа-частиц с энергией 4,05 МэВ, которые испускались ядром урана или радия. Таким образом предлагалось изучить рассеяние (изменение направления движения) альфа-частиц в веществе.
Масса альфа-частицы примерно в 8000 раз больше массы электрона. Положительный заряд равен по модулю удвоенному заряду электрона 2е. Скорость альфа-частицы составляет 1/15 скорости света или 2 * 10 7 м/с. Альфа-частица – это полностью ионизированный атом гелия.
Упрощенная схема опытов Резерфорда изображена на рис. 1.1. Альфа-частицы испускались радиоактивным источником 1, помещённым внутри свинцового цилиндра 2 с узким каналом 3. Узкий пучок альфа-частиц из канала падал на фольгу 4 из исследуемого материала, перпендикулярно к поверхности фольги. Из свинцового цилиндра альфа-частицы проходили только через канал, а остальные поглощались свинцом. Прошедшие сквозь фольгу и рассеянные ею альфа-частицы попадали на полупрозрачный экран 5, который был покрыт люминесцирующим веществом (сульфатом цинка). Это вещество было способно светиться при ударе об него альфа-частицы. Столкновение каждой частицы с экраном сопровождалось вспышкой света. Эта вспышка называется сцинтилляция (от латинского scintillation – сверкание, кратковременная вспышка света). За экраном находился микроскоп 6. Чтобы не происходило дополнительного рассеяния альфа-частиц в воздухе, весь прибор размещался в сосуде с достаточным вакуумом.
Рис. 1.1. Упрощённая схема опытов Резерфорда.
В отсутствие фольги на экране возникал светлый кружок, состоящий из сцинтилляций, вызванных тонким пучком альфа-частиц. Но когда на пути движения альфа-частиц помещали тонкую золотую фольгу толщиной примерно 0,1 мк (микрон), то наблюдаемая на экране картинка сильно менялась: отдельные вспышки появлялись не только за пределами прежнего кружка, но их можно было даже наблюдать с противоположной стороны золотой фольги.
Подсчитывая число сцинтилляций в единицу времени в разных местах экрана, можно установить распределение в пространстве рассеянных альфа-частиц. Число альфа-частиц быстро убывает с увеличением угла рассеяния.
Наблюдаемая на экране картина позволила заключить, что большинство альфа-частиц проходит сквозь золотую фольгу без заметного изменения направления их движения. Однако некоторые частицы отклонялись на большие углы от первоначального направления альфа-частиц (порядка 135 о …150 о) и даже отбрасывались назад. Исследования показали, что при прохождении альфа-частиц сквозь фольгу примерно на каждые 10000 падающих частиц только одна отклоняется на угол более 10 о от первоначального направления движения. Лишь в виде редкого исключения одна из огромного числа альфа-частиц отклоняется от своего первоначального направления.
Тот факт, что многие альфа-частицы проходили сквозь фольгу, не отклоняясь от своего направления движения, говорит о том, что атом не является сплошным образованием. Так как масса альфа-частицы почти в 8000 раз превосходит массу электрона, то электроны, входящие в состав атомов фольги, не могут заметно изменить траекторию альфа-частиц. Рассеяние альфа-частиц может вызывать положительно заряженная частица атома – атомное ядро.
Атомное ядро – это тело малых размеров, в котором сконцентрированы почти вся масса и почти весь положительный заряд атома.
Чем ближе альфа-частица подходила к ядру, тем больше была сила электрического взаимодействия и тем на больший угол частица отклонялась. На малых расстояниях от ядра положительно-заряженная альфа-частица испытывает значительную силу отталкивания F от ядра, которую определяют по закону Кулона:
| F = |
где r – расстояние от ядра до альфа-частицы; ε 0 – электрическая постоянная в единицах измерения СИ; p – число протонов в ядре; е = 1,6*10-19 Кл – абсолютное значение элементарного электрического заряда (заряда электрона); 2e – заряд альфа-частицы
На рисунке 1.2 показаны траектории альфа-частиц, пролетающих на различных расстояниях от ядра.
Резерфорд смог ввести формулу, связывающую количество рассеянных на определённый угол альфа-частиц с энергией альфа-частиц и протонов р в ядре атома. Опытная проверка формулы подтвердила её справедливость и показала, что количество протонов в ядре равно числу внутриатомных электронов Z и определяется атомным номером химического элемента (то есть порядковым номером элемента в периодической системе Д.И.Менделеева):
p = Z
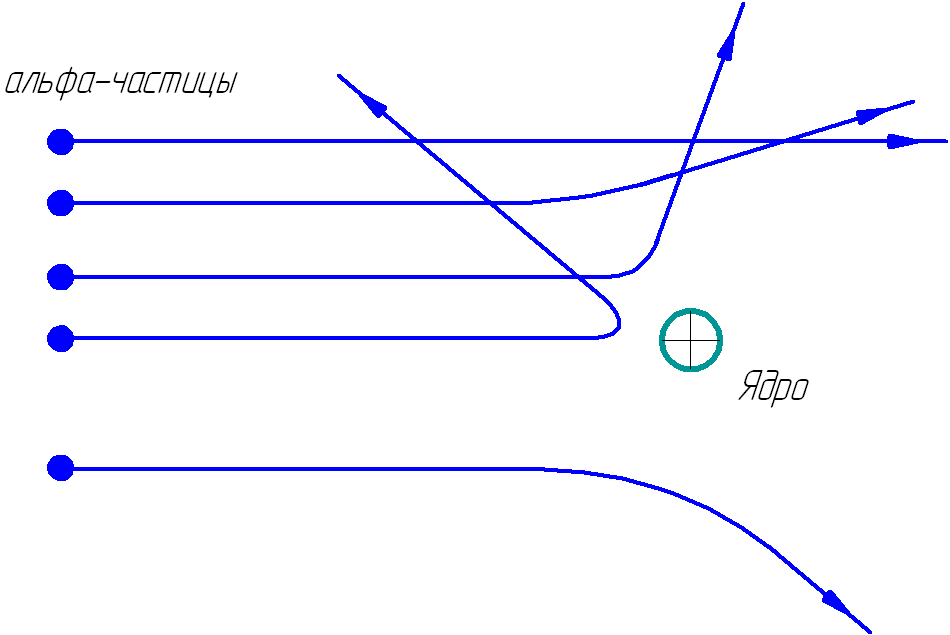
Рис. 1.2. Траектории альфа-частиц.
Подсчитывая количество альфа-частиц, рассеянных на различные углы, Резерфорд смог оценить линейные размеры ядра. Чтобы положительное ядро могло отбросить альфа-частицу назад, потенциальная энергия электростатического (кулоновского) отталкивания у границ ядра атома должна равняться кинетической энергии альфа-частицы:
| = |
Оказалось, что ядро имеет диаметр:
D я = 10 -13 …10 -12 см = 10 -15 …10 -14 м
Линейный диаметр самого атома:
D a = 10 -8 см = 10 -10 м
Планетарная модель атома
После анализа многочисленных опытов, Резерфордом в 1911 году была предложена планетарная модель атома (ядерная модель атома).
Согласно этой модели в центре атома находится положительно заряженное ядро, в котором сосредоточена почти вся масса атома. Вокруг ядра вращаются по орбитам отрицательно заряженные электроны. Электроны движутся вокруг ядра на относительно больших расстояниях, подобно тому, как планеты вращаются вокруг солнца. Из совокупности этих электронов образуется электронная оболочка или электронное облако .
Атом в целом нейтрален, следовательно, абсолютное значение суммарного отрицательного заряда электронов равно положительному заряду ядра: число Z*e протонов в ядре равно числу электронов в электронном облаке и совпадает с порядковым номером (атомным номером) Z атома данного химического элемента в периодической системе Д.И.Менделеева.
Например, атом водорода имеет порядковый номер Z = 1, следовательно, атом водорода состоит из положительного ядра с зарядом, равным абсолютному значению заряда электрона. Вокруг ядра вращается один электрон. Ядро атома водорода названо протоном. Атом лития имеет порядковый номер Z = 3, следовательно, вокруг ядра атома лития вращаются 3 электрона.
Компьютерная программа моделирует классический опыт Резерфорда по зондированию атома с помощью α-частиц, на основе результатов которого была предложена планетарная модель строения атома .
Первые прямые эксперименты по исследованию внутренней структуры атомов были выполнены Э. Резерфордом и его сотрудниками Э. Марсденом и Х. Гейгером в 1909–1911 годах.
Резерфорд предложил применить зондирование атома с помощью α-частиц, которые возникают при радиоактивном распаде радия и некоторых других элементов. Масса α-частиц приблизительно в 7300 раз больше массы электрона, а положительный заряд равен удвоенному элементарному заряду. В своих опытах Резерфорд использовал α-частицы с кинетической энергией около 5 МэВ (скорость таких частиц очень велика – порядка 107 м/с, но все же значительно меньше скорости света).
α-частицы – это полностью ионизированные атомы гелия. Они были открыты Резерфордом в 1899 году при изучении явления радиоактивности. Этими частицами Резерфорд бомбардировал атомы тяжелых элементов (золото, серебро, медь и др.). Электроны, входящие в состав атомов, вследствие малой массы не могут заметно изменить траекторию α-частицы. Рассеяние, то есть изменение направления движения α-частиц, может вызвать только тяжелая положительно заряженная часть атома. Схема опыта Резерфорда представлена на рис. 1.
От радиоактивного источника, заключенного в свинцовый контейнер, α-частицы направлялись на тонкую металлическую фольгу. Рассеянные частицы попадали на экран, покрытый слоем кристаллов сульфида цинка, способных светиться под ударами быстрых заряженных частиц. Сцинтилляции (вспышки) на экране наблюдались глазом с помощью микроскопа. Наблюдения рассеянных α-частиц в опыте Резерфорда можно было проводить под различными углами φ к первоначальному направлению пучка. Было обнаружено, что большинство α-частиц проходит через тонкий слой металла, практически не испытывая отклонения. Однако небольшая часть частиц отклоняется на значительные углы, превышающие 30°. Очень редкие α-частицы (приблизительно одна на десять тысяч) испытывали отклонение на углы, близкие к 180°.
Опыты Резерфорда и его сотрудников привели к выводу, что в центре атома находится плотное положительно заряженное ядро, диаметр которого не превышает 10 –14 –10 –15 м. Это ядро занимает только 10 –12 часть полного объема атома, но содержит весь положительный заряд и не менее 99,95 % его массы. Заряд ядра должен быть равен суммарному заряду всех электронов, входящих в состав атома.
Опираясь на классические представления о движении микрочастиц, Резерфорд предложил планетарную модель атома . Согласно этой модели, в центре атома располагается положительно заряженное ядро, в котором сосредоточена почти вся масса атома. Атом в целом нейтрален. Вокруг ядра, подобно планетам, под действием кулоновских сил со стороны ядра вращаются электроны. Находиться в состоянии покоя электроны не могут, так как они упали бы на ядро.
Планетарная модель атома, предложенная Резерфордом, явилась крупным шагом вперед в развитии знаний о строении атома. Она была совершенно необходимой для объяснения опытов по рассеянию α-частиц, однако оказалась неспособной объяснить сам факт длительного существования атома, т. е. его устойчивость. По законам классической электродинамики, движущийся с ускорением заряд должен излучать электромагнитные волны, уносящие энергию. За короткое время (порядка 10 –8 с) все электроны в атоме Резерфорда должны растратить всю свою энергию и упасть на ядро. То, что этого не происходит в устойчивых состояниях атома, показывает, что внутренние процессы в атоме не подчиняются классическим законам.
Пользователь имеет возможность:
- наблюдать рассеяние частиц на неподвижном ядре золота;
- изменять прицельное расстояние и начальную скорость частицы;
- измерять угол рассеяния частицы;
- исследовать кривую рассеяния при бомбардировке ядра золота потоком частиц с заданной энергией в автоматическом режиме.
Атом состоит из компактного и массивного положительно заряженного ядра и отрицательно заряженных легких электронов вокруг него.
Эрнест Резерфорд — уникальный ученый в том плане, что свои главные открытия он сделал уже после получения Нобелевской премии. В 1911 году ему удался эксперимент, который не только позволил ученым заглянуть вглубь атома и получить представление о его строении, но и стал образцом изящества и глубины замысла.
Используя естественный источник радиоактивного излучения, Резерфорд построил пушку, дававшую направленный и сфокусированный поток частиц. Пушка представляла собой свинцовый ящик с узкой прорезью, внутрь которого был помещен радиоактивный материал. Благодаря этому частицы (в данном случае альфа-частицы, состоящие из двух протонов и двух нейтронов), испускаемые радиоактивным веществом во всех направлениях, кроме одного, поглощались свинцовым экраном, и лишь через прорезь вылетал направленный пучок альфа-частиц. Далее на пути пучка стояло еще несколько свинцовых экранов с узкими прорезями, отсекавших частицы, отклоняющиеся от строго заданного направления. В результате к мишени подлетал идеально сфокусированный пучок альфа-частиц, а сама мишень представляла собой тончайший лист золотой фольги. В нее-то и ударял альфа-луч. После столкновения с атомами фольги альфа-частицы продолжали свой путь и попадали на люминесцентный экран, установленный позади мишени, на котором при попадании на него альфа-частиц регистрировались вспышки. По ним экспериментатор мог судить, в каком количестве и насколько альфа-частицы отклоняются от направления прямолинейного движения в результате столкновений с атомами фольги.
Эксперименты подобного рода проводились и раньше. Основная их идея состояла в том, чтобы по углам отклонения частиц накопить достаточно информации, по которой можно было бы сказать что-либо определенное о строении атома. В начале ХХ века ученые уже знали, что атом содержит отрицательно заряженные электроны. Однако преобладало представление, что атом представляет собой что-то похожее на положительно заряженную тонкую сетку, заполненную отрицательно заряженными электронами-изюминами, — модель так и называлась «модель сетки с изюмом». По результатам подобных опытов ученым удалось узнать некоторые свойства атомов — в частности, оценить порядок их геометрических размеров.
Резерфорд, однако, заметил, что никто из его предшественников даже не пробовал проверить экспериментально, не отклоняются ли некоторые альфа-частицы под очень большими углами. Модель сетки с изюмом просто не допускала существования в атоме столь плотных и тяжелых элементов структуры, что они могли бы отклонять быстрые альфа-частицы на значительные углы, поэтому никто и не озабочивался тем, чтобы проверить такую возможность. Резерфорд попросил одного из своих студентов переоборудовать установку таким образом, чтобы можно было наблюдать рассеяние альфа-частиц под большими углами отклонения, — просто для очистки совести, чтобы окончательно исключить такую возможность. В качестве детектора использовался экран с покрытием из сульфида натрия — материала, дающего флуоресцентную вспышку при попадании в него альфа-частицы. Каково же было удивление не только студента, непосредственно проводившего эксперимент, но и самого Резерфорда, когда выяснилось, что некоторые частицы отклоняются на углы вплоть до 180°!
В рамках устоявшейся модели атома полученный результат не мог быть истолкован: в сетке с изюмом попросту нет ничего такого, что могло бы отразить мощную, быструю и тяжелую альфа-частицу. Резерфорд вынужден был заключить, что в атоме большая часть массы сосредоточена в невероятно плотном веществе, расположенном в центре атома. А вся остальная часть атома оказывалась на много порядков менее плотной, нежели это представлялось раньше. Из поведения рассеянных альфа-частиц вытекало также, что в этих сверхплотных центрах атома, которые Резерфорд назвал ядрами , сосредоточен также и весь положительный электрический заряд атома, поскольку только силами электрического отталкивания может быть обусловлено рассеяние частиц под углами больше 90°.
Годы спустя Резерфорд любил приводить по поводу своего открытия такую аналогию. В одной южноафриканской стране таможню предупредили, что в страну собираются провезти крупную партию контрабандного оружия для повстанцев, и оружие будет спрятано в тюках хлопка. И вот перед таможенником после разгрузки оказывается целый склад, забитый тюками с хлопком. Как ему определить, в каких именно тюках спрятаны винтовки? Таможенник решил задачу просто: он стал стрелять по тюкам, и, если пули рикошетили от какого-либо тюка, он по этому признаку и выявлял тюки с контрабандным оружием. Так и Резерфорд, увидев, как альфа-частицы рикошетируют от золотой фольги, понял, что внутри атома скрыта гораздо более плотная структура, чем предполагалось.
Картина атома, нарисованная Резерфордом по результатам опыта, нам сегодня хорошо знакома. Атом состоит из сверхплотного, компактного ядра, несущего на себе положительный заряд, и отрицательно заряженных легких электронов вокруг него. Позже ученые подвели под эту картину надежную теоретическую базу (см. Атом Бора), но началось всё с простого эксперимента с маленьким образцом радиоактивного материала и куском золотой фольги.
См. также:
Ernest Rutherford, First Baron Rutherford of Nelson, 1871-1937
Новозеландский физик. Родился в Нельсоне, в семье фермера-ремесленника. Выиграл стипендию для получения образования в Кембриджском университете в Англии. После его окончания получил назначение в канадский университет Мак-Гилл (McGill University), где совместно с Фредериком Содди (Frederick Soddy, 1877-1966) установил основные закономерности явления радиоактивности, за что в 1908 году был удостоен Нобелевской премии по химии. Вскоре ученый перебрался в Манчестерский университет, где под его руководством Ханс Гейгер (Hans Geiger, 1882-1945) изобрел свой знаменитый счетчик Гейгера, занялся исследованиями строения атома и в 1911 году открыл существование атомного ядра. В годы Первой мировой войны занимался разработкой сонаров (акустических радаров) для обнаружения подводных лодок противника. В 1919 году был назначен профессором физики и директором Кавендишской лаборатории Кембриджского университета и в том же году открыл распад ядра в результате бомбардировки тяжелыми частицами высоких энергий. На этом посту Резерфорд оставался до конца жизни, одновременно являясь на протяжении многих лет президентом Королевского научного общества. Похоронен в Вестминстерском аббатстве рядом с Ньютоном, Дарвином и Фарадеем.
Выводы из опыта по рассеиванию альфа-частиц Резерфорда: 1. Существует атомное ядро, т.е. тело малых размеров, в котором сконцентрирована почти вся масса атома и весь положительный заряд. 2. В ядре сконцентрирована почти вся масса атома. 3. Вокруг ядра по замкнутым орбитам вращаются отрицательные частицы- электроны. 4. отрицательный заряд всех электронов распределён по всему объёму атома. Ядерная модель атома:
Слайд 9 из презентации «Опыт Резерфорда, модель атома» . Размер архива с презентацией 174 КБ.Физика 9 класс
краткое содержание других презентаций«Строение атома элемента» - Кто открыл явление радиоактивности. Строение. Атом – «неделимый». Резерфорд провел ряд опытов по исследованию строения и состава атомов. Томсон предложил в 1903 г одну из первых моделей строения атома. Анри Беккерель открывает явление радиоактивности. Частица вызывала на экране вспышку. Два события в конце 19 века привели к мысли о сложном строении атома. Строение атома. Планетарная (ядерная) модель.
«Камера Вильсона» - Назначение прибора. Принцип роботы. Усовершенствование. Емкость. Изобретатель прибора. Значение. Камера. Вильсон. Камера Вильсона. Устройство.
«Безопасность атомной энергетики» - Из истории атомной энергетики. Реакция распада ядер урана. Схема работы кипящего ядерного реактора. Безопасность. Схема кипящего ядерного реактора. АЭС имеют больше возможностей в производстве энергии. Атомные электростанции. Вред атомной энергетики. Атомные электростанции на карте России. Ядерный реактор. Атомная энергетика. Термоядерный синтез. Польза и вред атомной энергетики. Атомные ледоколы.
«Физика «Движение»» - Взаимодействие тел. Механика. Закон сохранения в механике. Строение атома. Инертность и масса тел. Скорость при неравномерном движении. Как изменяются координаты. Перемещение при прямолинейном равноускоренном движении. Основы динамики. Работа силы. 2 закон Ньютона. Свободное падение тел. Основы физики. Изучении свойств материи. Вектор. 3 закон Ньютона. Период и частота обращения. Ускорение. Физика-это точная наука.
«Колебания математического маятника» - План урока. Практическое использование колебаний маятника. Галилео Галилей (1564-1642). Гюйгенс Христиан (1629 – 1695). Любое ли тело может совершать колебательные движения. Опыт был выполнен в узком кругу. Иллюстрация механических колебаний на примере маятника Фуко. Старое здание Пизанского университета. Реальный маятник можно считать математическим, если длина нити много больше размеров подвешенного на ней тела.
«Первая космическая скорость» - Решите задачи. Ускорение свободного падении. Скорость, которую необходимо сообщить телу, чтобы оно стало спутником. Представление об ИСЗ. Первая космическая скорость. Условия, при которых тело становится ИСЗ. Искусственные спутники Земли. Определить первую космическую скорость для запуска спутника. Решите задачу. Обращение планет вокруг Солнца.
Похожие статьи
-
Мир культуры. Загадочный падишах. акбар великий Джалал уд-дин Мухаммад Акбар
бакалавр истории по направлению "История"Волгоградский государственный университетмагистрант кафедры истории России ИИМОСТ ВолГУНаучный руководитель: Рамазанов С.П., доктор исторических наук, профессор, Волгоградский государственный...
-
Либерия Изобразительное искусство и ремесла
Официальное название - Республика Либерия (Republic of Liberia).Расположена в западной части Африки. Площадь 111,4 тыс. км2, численность населения 3,3 млн чел. (2002). Государственный язык - английский. Столица - г. Монровия (1,3 млн чел.,...
-
Гибель колонны 245 мсп в аргунском ущелье
Сложившееся в 1991 году двоевластие в Чечне, объявившей себя суверенной республикой, привело к противостоянию с федеральным правительством и внутренним конфликтам в борьбе за власть, закончившимся введением войск РФ в декабре 1994-го. Так...
-
Обозначение времени в английском языке?
Всем кто интересуется изучением английского языка, приходилось сталкиваться со странными обозначениями p. m. и a. m , и вообще, везде, где упоминается о времени, почему-то используется всего 12 часовой формат . Наверное, для нас живущих...
-
Кто такие приписные крестьяне?
В крестьянских сословиях исторического промежутка 18−19 вв. представлены самые разные социальные группы. Но на фоне остальных особое внимание обращают на себя посессионные и, конечно, приписные крестьяне. Именно они составляли в те времена...
-
Стихотворение Некрасова Н
В августе, около "Малых Вежей", С старым Мазаем я бил дупелей.Как-то особенно тихо вдруг стало, На небе солнце сквозь тучу играло.Тучка была небольшая на нём, А разразилась жестоким дождём!Прямы и светлы, как прутья стальные, В землю...
